2021-2022學年甘肅省定西市臨洮縣高二(下)開學化學試卷
發布:2025/1/1 22:30:2
一、選擇題(本題共17小題,每小題只有一個正確選項,每小題3分,共51分)
-
1.下列說法不正確的是( )
A.生活中使用的漂白粉和肥皂都是混合物 B.煙、霧、豆漿、有色玻璃都是膠體 C.汽油屬于混合物,而液氯、冰醋酸均屬于純凈物 D.蔗糖、硝酸鉀和硫酸鋇分別屬于非電解質、強電解質和弱電解質 組卷:35引用:4難度:0.9 -
2.對于Zn(s)+H2SO4(aq)═ZnSO4(aq)+H2(g)△H<0的化學反應下列敘述不正確的是( )
A. 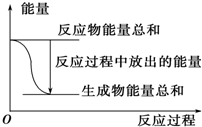
反應過程中能量關系可用如圖表示B.△H的值與反應方程式的計量系數有關 C.若將該反應設計成原電池,鋅為負極 D.若將其設計為原電池,當有32.5g鋅溶解時,正極放出氣體一定為11.2L 組卷:12引用:7難度:0.9 -
3.利用如圖裝置電解制備LiOH,兩電極區電解液分別為LiOH和LiCl溶液.下列說法錯誤的是( )
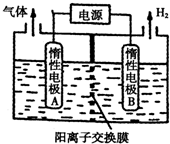
A.惰性電極A為陽極,惰性電極B為陰極 B.電解過程中Li+向A電極遷移 C.陽極電極反應式為:2Cl--2e-═Cl2↑ D.B極區電解液為LiOH溶液 組卷:8引用:3難度:0.5 -
4.在一定溫度下的定容容器中,當反應A(s)+2B(g)?C(g)+D(g)達到平衡狀態后,下列哪些物理量不再發生變化( )
①混合氣體的壓強
②混合氣體的密度
③B的物質的量濃度
④氣體總物質的量
⑤混合氣體的平均相對分子質量
⑥v(C)與v(D)的比值A.②③⑤ B.①②③ C.②③④⑥ D.①②③④⑤⑥ 組卷:16引用:4難度:0.7 -
5.下列各組對比實驗,均能觀察到左邊試管產生氣體的速率比右邊的快,其中一定能證明Fe3+催化過氧化氫分解的能力強于Cu2+的是( )
A. 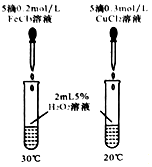
B. 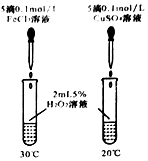
C. 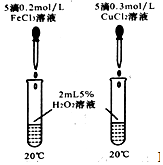
D. 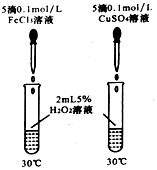 組卷:18引用:1難度:0.7
組卷:18引用:1難度:0.7 -
6.現有反應4HCl(g)+O2(g)═2Cl2(g)+2H2O(g),已知2molO2被還原時,放出akJ的熱量,且知斷開1molO=O鍵需要吸收bkJ的熱量,斷開1 molCl-Cl鍵需要吸收c kJ的熱量。則斷開1 mol H-O鍵比斷開1molH-Cl鍵所需能量高( )
A.(b-a-2c)/4kJ B.(a+2b-4c)/8 kJ C.(a+b-2c)/4 kJ D.(2b-a-4c)/8 kJ 組卷:20引用:3難度:0.7 -
7.下列說法中,正確的是( )
A.水的離子積KW隨溫度、外加酸(堿)濃度的改變而改變 B.能自發進行的化學反應,一定是△H<0、△S>0 C.對已達化學平衡的反應,僅改變濃度,若平衡移動,則平衡常數(K)一定改變 D.Ksp只與難溶電解質的性質和溫度有關,而與溶液中的離子濃度無關 組卷:8引用:3難度:0.5
三、填空題(本題共4小題,共41分)
-
21.甲醇是重要的化工原料,又可作為燃料。工業上利用合成氣(主要成分為CO、CO2和H2)在催化劑的作用下合成甲醇,發生的主反應如下:
①CO(g)+2H2 (g)?CH3OH(g)△H1;
②CO2(g)+3H2 (g)?CH3OH(g)+H2O(B)△H=-58kJ/mol;
③CO2(g)+H2(g)?CO(g)+H2O(g)△H═+41kJ/mol。
回答下列問題:
(1)已知反應①中相關的化學鍵鍵能數據如下表:
則x=化學鍵 H-H C-O C≡O H-O C-H E/(kJ?mol-1) 436 343 1076 465 x 。
(2)合成氣組成=2.60時,體系中的CO平衡轉化率(α)與溫度和壓強的關系如圖甲所示。(CO)值隨溫度升高而n(H2)n(CO+CO2)(填“增大”或“減小”),其原因是;圖中的壓強由大到小為,其判斷理由是。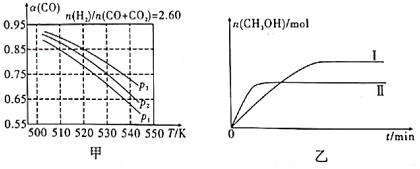
(3)若將1molCO2和2molH2充入容積為2L的恒容密閉容器中,在兩種不同溫度下發生反應②.測得CH3OH的物質的量隨時間的變化如圖乙所示。
①曲線Ⅰ、Ⅱ對應的平衡常數大小關系為K1KⅡ(填“>”“=”或“<”)。
②一定溫度下,下列能判斷該反應達到化學平衡狀態的是(填序號)。
a.容器中壓強不變
b.甲醇和水蒸氣的體積比保持不變
c.v正(H2)=3v逆(CH3OH)
d.2個C=0斷裂的同時有6個H-H斷裂
③若5min后反應達到平衡狀態,H2的轉化率為90%,則用CO2表示的平均反應速率為,該溫度下的平衡常數為;若容器容積不變,下列措施可增加甲醇產率的是。(填序號)。
a.縮小反應容器的容積
b.仗用合適的催化劑
c.充入He
d.按原比例再充入CO2和H2組卷:38引用:3難度:0.5 -
22.以CH3OH燃料電池為電源電解法制取ClO2.二氧化氯(ClO2)為一種黃綠色氣體,是國際上公認的高效、廣譜、快速、安全的殺菌消毒劑.
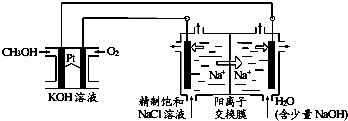
①CH3OH燃料電池放電過程中,通入O2的電極附近溶液的pH(填“增大”、“減小”或“不變”),負極反應式為.
②圖中電解池用石墨作電極,在一定條件下電解飽和食鹽水制取ClO2.陽極產生ClO2的反應式為.
③電解一段時間,從陰極處收集到的氣體比陽極處收集到氣體多6.72L時(標準狀況,忽略生成的氣體溶解),停止電解,通過陽離子交換膜的陽離子為mol.組卷:28引用:4難度:0.5


