2013-2014學(xué)年湖南省長(zhǎng)沙市長(zhǎng)郡中學(xué)高一(上)化學(xué)周末作業(yè)(11月份)
發(fā)布:2024/4/20 14:35:0
一、選擇題(共15小題,每小題3分,滿分45分)
-
1.下列離子方程式正確的是( )
A.鈉與水反應(yīng):Na+2H2O=Na++2OH-+H2↑ B.硅酸鈉溶液與醋酸溶液混合:SiO32-+2H+=H2SiO3↓ C.0.01mol/LNH4Al(SO4)2溶液與0.02mol/LBa(OH)2溶液等體積混合:
NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3?H2OD.濃硝酸中加入過量鐵粉并加熱:Fe+3NO3-+6H+ Fe3++3NO2↑+3H2O△組卷:133引用:9難度:0.7 -
2.下列離子方程式正確的是( )
A.碳酸鈣跟醋酸反應(yīng):CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑ B.向次氯酸鈣溶液中通入過量二氧化硫Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO C.向硫酸氫鈉溶液中滴入氫氧化鋇溶液至中性H++SO42-+Ba2++OH-=BaSO4↓+H2O D.將氫氧化鐵粉末加入氫碘酸:Fe(OH)3+3H=Fe3++3H2O 組卷:29引用:1難度:0.9 -
3.常溫下,下列各組離子在指定溶液中一定能大量共存的是( )
A.1.0 mol?L-1的 KNO3 溶液:H+、Fe2+、Cl-、 SO2-4B.石蕊呈紅色的溶液: 、Ba2+、NH+4、Cl-AlO-2C.pH=12 的溶液:K+、Na+、CH3COO-、Br- D.與鋁反應(yīng)產(chǎn)生大量氫氣的溶液:Na+、K+、 、CO2-3NO-3組卷:114引用:60難度:0.9 -
4.Cl2通入70℃的NaOH溶液中能同時(shí)發(fā)生兩個(gè)自身氧化還原反應(yīng),反應(yīng)后測(cè)得溶液中NaClO與NaClO3的物質(zhì)的量之比為4:1,則該溶液中NaCl與NaClO的物質(zhì)的量之比為( )
A.9:4 B.5:1 C.11:2 D.1:1 組卷:79引用:19難度:0.7 -
5.Na2Sx在堿性溶液中可被NaClO氧化為Na2SO4,而NaClO被還原為NaCl,若反應(yīng)中Na2Sx與NaClO的物質(zhì)的量之比為1:16,則x值是( )
A.2 B.3 C.4 D.5 組卷:317引用:41難度:0.9 -
6.在濃鹽酸中H3AsO3與SnCl2反應(yīng)的離子方程式為:3SnCl2+12Cl-+2H3AsO3+6H+═2As+3SnCl62-+6M,關(guān)于該反應(yīng)的說法中正確的組合是( )
①氧化劑是H3AsO3 ②還原性:Cl->As ③每生成7.5g As,還原劑失去的電子為0.3mol ④M為OH- ⑤SnCl62-是氧化產(chǎn)物.A.①③⑤ B.①②④⑤ C.①②③④ D.①③ 組卷:340引用:34難度:0.9
二、填空題(共4小題,每小題3分,滿分12分)
-
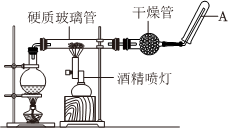 18.在常溫下,F(xiàn)e與水并不起反應(yīng),但在高溫下,F(xiàn)e與水蒸氣可發(fā)生反應(yīng).應(yīng)用下列裝置,在硬質(zhì)玻璃管中放入還原鐵粉和石棉絨的混合物,加熱,并通入水蒸氣,就可以完成高溫下“Fe與水蒸氣的反應(yīng)實(shí)驗(yàn)”.
18.在常溫下,F(xiàn)e與水并不起反應(yīng),但在高溫下,F(xiàn)e與水蒸氣可發(fā)生反應(yīng).應(yīng)用下列裝置,在硬質(zhì)玻璃管中放入還原鐵粉和石棉絨的混合物,加熱,并通入水蒸氣,就可以完成高溫下“Fe與水蒸氣的反應(yīng)實(shí)驗(yàn)”.
請(qǐng)回答該實(shí)驗(yàn)中的問題.
(1)寫出該反應(yīng)的反應(yīng)方程式:;并指明該氧化還原反應(yīng)的還原劑是,氧化劑是.若該反應(yīng)生成的氫氣在標(biāo)況下為11.2L時(shí),轉(zhuǎn)移的電子數(shù)目為
(2)該實(shí)驗(yàn)進(jìn)行之前的一步操作是,操作方法是:
(3)圓底燒瓶中盛裝的水,該裝置受熱后的主要作用是;燒瓶底部放置了幾片碎瓷片,碎瓷片的作用是.
(4)酒精燈和酒精噴燈點(diǎn)燃的順序是,為什么?.組卷:30引用:1難度:0.1 -
19.將質(zhì)量為1.15g鈉用刺了孔的鋁箔包裹后放入水中,共收集到1.232L(標(biāo)準(zhǔn)狀況)氣體.請(qǐng)回答下列問題:
(1)1.15g鈉與水反應(yīng),理論上生成氣體的體積(標(biāo)準(zhǔn)狀況)為L.
(2)反應(yīng)后溶液的體積為100mL,則溶液中NaOH的物質(zhì)的量濃度為多少?組卷:31引用:1難度:0.1


