2020-2021學年黑龍江省哈爾濱九中高三(上)開學化學試卷
發布:2024/12/30 11:0:3
一、選擇題(共25小題,每小題2分,滿分50分)
-
1.下列有關物質分類或歸類中,正確的是( )
①混合物:鹽酸、漂白粉、氯水、水銀
②化合物:CaCl2、NaOH、HCl、HD
③電解質:明礬、石膏、冰醋酸、氯化銀
④同素異形體:C60、C70、金剛石、石墨.A.只有①③ B.只有②③ C.只有③④ D.只有④ 組卷:125引用:10難度:0.9 -
2.在全國人民眾志成城抗擊新冠病毒期間,使用的“84消毒液”的主要有效成分是( )
A.NaOH B.NaCl C.NaClO D.Na2CO3 組卷:558引用:22難度:0.7 -
3.下列詩句中所涉及的化學現象描述錯誤的是( )
A.“春蠶到死絲方盡”中的“絲”的主要成分是蛋白質 B.“落日川渚寒,愁云繞天起”中的“云”屬于膠體 C.“爆竹聲中一歲除”涉及了氧化還原反應 D.“日照香爐生紫煙”描述了碘的升華 組卷:15引用:2難度:0.7 -
4.設阿伏加德羅常數的值為NA,下列說法不正確的是( )
A.0.1mol C6H14中含有的共用電子對數為1.9NA B.10g質量分數為46%的乙醇溶液中所含氧原子的總數為0.4NA C.標準狀況下,2.24 L己烷中含有的分子數為0.1NA D.1mol苯乙烯( 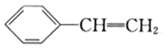 )中含有的碳碳雙鍵數為NA組卷:19引用:2難度:0.6
)中含有的碳碳雙鍵數為NA組卷:19引用:2難度:0.6 -
5.下列實驗操作中正確的是( )
A.配制一定物質的量濃度的H2SO4溶液時,用量筒量取一定體積的濃硫酸倒入燒杯后,再用蒸餾水洗滌量筒2~3次,并將洗滌液一并倒入燒杯中稀釋 B.100gH2SO4溶液的物質的量濃度為18.4mol?L-1,用水稀釋到物質的量濃度為9.2mol?L-1,需要水100g C.配制一定物質的量濃度的氯化鉀溶液:準確稱取一定質量的氯化鉀固體,放入1000mL的容量瓶中,加入1000mL溶解,振蕩搖勻 D.將10g CuSO4溶解在90g水中,配制溶質質量分數為10%的CuSO4溶液 組卷:43引用:5難度:0.9 -
6.能正確表示下列反應的離子方程式的是( )
A.Cl2通入NaOH溶液:Cl2+OH-═Cl-+ClO-+H2O B.NaHCO3溶液中加入稀HCl:CO32-+2H+═CO2↑+H2O C.AlCl3溶液中加入過量稀氨水:Al3++4NH3?H2O═AlO2-+4NH4++2H2O D.Cu溶于稀HNO3:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O 組卷:2135引用:59難度:0.9 -
7.常溫下,下列各組離子在指定溶液中能大量共存的是( )
A.0.1mol?L-1氨水溶液:Na+、K+、OH-、NO3- B.0.1mol?L-1鹽酸溶液:Na+、K+、SO42-、SiO32- C.0.1mol?L-1KMnO4溶液:NH4+、Na+、NO3-、I- D.0.1mol?L-1AgNO3溶液:NH4+、Mg2+、Cl-、SO42- 組卷:1411引用:20難度:0.5 -
8.某種飛船是以N2H4和N2O4為動力源,化學方程式為2N2H4+N2O4═3N2+4H2O,反應溫度可高達2700℃,對于該反應,下列說法正確的是( )
A.N2H4分子中所有原子可能共平面 B.N2O4是還原劑 C.N2既是氧化產物又是還原產物 D.每轉移16NA電子則會生成標況下67.2L N2 組卷:34引用:2難度:0.8 -
9.下列敘述不涉及氧化還原反應的是( )
A.谷物發酵釀造食醋 B.小蘇打用作食品膨松劑 C.含氯消毒劑用于環境消毒 D.大氣中NO2參與酸雨形成 組卷:657引用:16難度:0.5
二、解答題(共3小題,滿分37分)
-
28.磺酰氯(SO2Cl2)是一種有機氯化劑,也是鋰電池正極活性物質。已知磺酰氯是一種無色液體,熔點-54.1℃,沸點69.1℃,遇水發生劇烈水解,且產生白霧。
(1)實驗室制備Cl2的離子反應方程式為。
(2)SO2Cl2水解的方程式為。
(3)某學習小組的同學依據反應:SO2(g)+Cl2(g)?SO2Cl2(g),設計制備磺酰氯裝置如圖。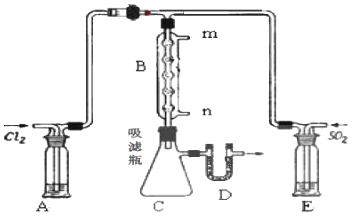
①A中所用的試劑為。
②實驗室用Na2SO3和硫酸制備SO2,可選用的氣體發生裝置是。(選填編號)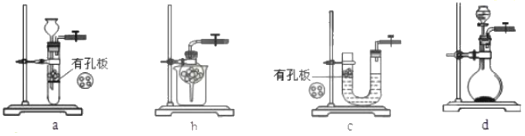
③B處反應管內五球中玻璃棉上的活性炭的作用為催化劑,D處U形管中盛放的試劑為,其作用是:。
(4)從化學平衡移動角度分析,反應管通水冷卻的目的為。組卷:5引用:1難度:0.5
[化學一選修3:物質結構與性質]
-
29.鈦被譽為“21世紀的金屬”,可呈現多種化合價。其中以+4價的Ti最為穩定。回答下列問題:
(1)基態Ti原子的價電子軌道表示式為。
(2)已知電離能:I2(Ti)=1310kJ/mol,I2(K)=3051kJ/mol。I2(Ti)<I2(K),其原因為。
(3)鈦某配合物可用于催化環烯烴聚合,其結果如圖所示:
①鈦的配位數為,碳原子的雜化類型。
②該配合物中存在的化學鍵有(填字母標號)。
a.離子鍵 b.配位鍵 c.金屬鍵 d.共價鍵 e.氫鍵
(4)鈦與鹵素形成的化合物熔沸點如下表所示:
分析 TiCl4、TiBr4、TiI4的熔點和沸點呈現一定變化規律的原因是TiCl4 TiBr4 TiI4 熔點/℃ -24.1 38.3 155 沸點/℃ 136.5 233.5 377 。
(5)已知TiO2與濃硫酸反應生成硫酸氧鈦,硫酸氧鈦晶體中陽離子為鏈狀聚合形式的離子,結構如圖所示,該陽離子化學式為。陰離子的空間構型為。
(6)已知TiN晶體的晶胞結構如下圖所示,若該晶胞的密度ρg/cm3,阿伏加德羅常數值為NA則晶胞中Ti原子與N原子的最近距離為pm.(用含ρ、NA的代數式表示) 組卷:92引用:7難度:0.4
組卷:92引用:7難度:0.4


