2023年湖南省湘潭一中高考化學模擬試卷(五)
發(fā)布:2024/4/20 14:35:0
一、選擇題:本題共14小題,每小題3分,共42分。每小題只有一個選項符合題目要求。
-
1.下列關于物質的性質、用途等描述中不正確的是( )
A.SO2具有還原性,并且可以殺菌、消毒,在葡萄酒中添加適量的SO2能殺滅微生物并防止葡萄酒的氧化變質 B.乙烯是一種重要的化工原料,可用于制取聚乙烯等化工產(chǎn)品,工業(yè)上可通過石油的裂化獲得乙烯 C.Al(OH)3分解是吸熱反應且分解后生成Al2O3和水蒸氣是其作阻燃劑的主要原因 D.SiO2透明度高,折射率合適,光能夠發(fā)生全反射,故SiO2是制作光導纖維的主要原料 組卷:27引用:3難度:0.7 -
2.設NA為阿伏加德羅常數(shù)的值,下列說法正確的是( )
A.一定條件下,1mol H2與足量碘蒸氣充分反應,轉移電子數(shù)目為2NA B.1mol Cu和足量稀硝酸反應產(chǎn)生NA個NO分子 C.25℃時,pH=13的氨水中由水電離出的氫離子數(shù)目為10-13NA D.標準狀況下,22.4L氦氣所含的質子數(shù)為2NA 組卷:33引用:2難度:0.8 -
3.對于下列實驗,能正確描述其反應的離子方程式是( )
A.將閃鋅礦浸沒在足量的藍礬溶液:ZnS+Cu2+═CuS+Zn2+ B.向小蘇打溶液中滴加少量苛性鈉溶液:HCO3-+OH-═H2O+CO2↑ C.用醋酸溶液處理水垢中的碳酸鈣:CaCO3+2H+═Ca2++H2O+CO2↑ D.向明礬溶液中加入過量的氨水:Al3++4NH3?H2O═AlO2-+4NH4++2H2O 組卷:51引用:4難度:0.7 -
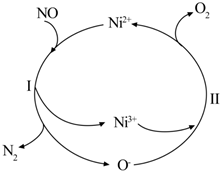 4.氮的氧化物是大氣污染物之一,如圖為科研人員探究消除氮氧化物的反應機理,下列說法錯誤的是( )
4.氮的氧化物是大氣污染物之一,如圖為科研人員探究消除氮氧化物的反應機理,下列說法錯誤的是( )A.整個過程中Ni2+作催化劑 B.過程Ⅰ中發(fā)生的化學反應為2Ni2++2NO=2Ni3++2O-+N2 C.過程中涉及的反應均為氧化還原反應 D.過程Ⅱ中氧化劑與還原劑的物質的量之比為1:2 組卷:144引用:3難度:0.6 -
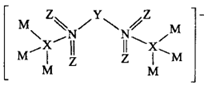 5.由W、X、Y、Z、M、N六種短周期元素組成的某種離子化合物是一種很好的二次電池的電解質。六種元素的原子序數(shù)依次增大,只有W是金屬元素,由非金屬元素構成的陰離子如圖所示,其中X元素形成的化合物種類繁多。下列說法正確的是( )
5.由W、X、Y、Z、M、N六種短周期元素組成的某種離子化合物是一種很好的二次電池的電解質。六種元素的原子序數(shù)依次增大,只有W是金屬元素,由非金屬元素構成的陰離子如圖所示,其中X元素形成的化合物種類繁多。下列說法正確的是( )A.元素N的含氧酸均是強酸 B.非金屬性強弱順序是M>Z>Y>X C.M元素的氫化物的水溶液可保存在玻璃瓶中 D.該陰離子中Y不滿足8電子穩(wěn)定結構 組卷:45引用:4難度:0.4 -
6.水合聯(lián)氨 (N2H4?H2O)是具有腐蝕性和強還原性的堿性液體,它是一種重要的化工試劑,其制備的反應原理為:NaClO+2NH3═N2H4?H2O+NaCl。下列裝置和操作能達到實驗目的的是( )
A B C D 



X是CaCl2 該裝置作為反應過程的安全瓶 制備水合聯(lián)氨時從a口通入NH3 用該裝吸收反應中過量的NH3 A.A B.B C.C D.D 組卷:34引用:4難度:0.5
二、非選擇題(共4個大題,58分)
-
17.綠色能源是未來能源發(fā)展的重要方向,氫能是重要的綠色能源,利用生物乙醇來制取氫氣的部分反應過程如圖所示。

(1)已知:反應①:CH3CH2OH(g)+3H2O(g)=2CO2(g)+6H2(g) ΔH1=+173.5kJ?mol-1
反應②:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2=-41.2kJ?mol-1
則反應Ⅰ的熱化學方程式為。
(2)反應Ⅱ在不同進氣比[n(CO):n(H2O)]、不同溫度下,測得相應的CO平衡轉化率見表(各點對應的其他反應條件都相同)。
①a點平衡混合物中H2的體積分數(shù)為平衡點 a b c d n(CO):n(H2O) 0.5 0.5 1 1 CO平衡轉化率/% 50 66.7 50 60 ,a、c兩點對應的反應溫度TaTc(填“<”“=”或“>”),d點對應的平衡常數(shù)K=。
②有利于提高CO平衡轉化率的是(填標號)。
A.增大壓強
B.降低溫度
C.增大進氣比[n(CO):n(H2O)]
D.分離出CO2
(3)反應Ⅱ在工業(yè)上稱為一氧化碳的催化變換反應,若用[K]表示催化劑,則反應歷程可用下式表示:
第一步:[K]+H2O(g)=[K]O+H2
第二步:[K]O+CO=[K]+CO2
第二步比第一步反應慢,則第二步反應的活化能比第一步反應。
(4)研究表明,CO催化變換反應的速率方程為υ=k(-yCO?yH2O)式中,yCO、yCO2?yH2Kp、yH2O、yCO2分別表示相應的物質的量分數(shù),Kp為平衡常數(shù),k為反應的速率常數(shù),溫度升高時k值增大。在氣體組成和催化劑一定的情況下,反應速率隨溫度變化的曲線如圖所示。溫度升高時,CO催化變換反應的KpyH2(填“增大”“減小”)。根據(jù)速率方程分析,T>Tm時υ逐漸減小的原因是。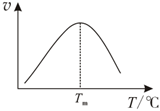 組卷:60引用:1難度:0.5
組卷:60引用:1難度:0.5 -
18.抗抑郁藥米那普侖(Milnacipran)中間體G的合成路線如圖:

回答下列問題:
(1)G的分子式是;G中的含氧官能團名稱為。
(2)寫出C的結構簡式;E→F的反應第一步是-CN水解生成-COOH,寫出第二步的化學方程式:。
(3)F→G的反應類型是。
(4)K與F互為同分異構體,滿足下列三個條件的K有種。
①能與NaHCO3反應
②屬于苯的三取代物,有兩個相同取代基,且不含甲基
③核磁共振氫譜中有5組峰,且峰面積之比為4:2:2:1:1
(5)結合題中信息,寫出用甲苯為原料,合成 的路線 (無機試劑任選)。組卷:16引用:3難度:0.5
的路線 (無機試劑任選)。組卷:16引用:3難度:0.5


