2021-2022學年黑龍江省哈爾濱九中高一(下)期末化學試卷
發布:2024/11/24 16:30:2
一、單項選擇題(每小題只有1個選項符合題意,每題2分)
-
1.蘇軾的《格物粗淡》中有這樣的記載:“紅柿摘下未熟,每籃用木瓜三枚放入,得氣即發,并無澀味。”按照現代科技觀點,該文中的“氣”是指( )
A.甲烷 B.乙烯 C.甲醛 D.乙酸 組卷:216引用:6難度:0.8 -
2.科學家利用聚偏氟乙烯(PVDF)和葡萄糖制備碳材料。PVDF的結構簡式如圖所示
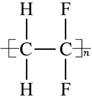 。下列說法正確的是( )
。下列說法正確的是( )A.葡萄糖中只含一種官能團 B.CH2═CF2是PVDF的鏈節 C.CH2═CF2和葡萄糖均能發生加聚反應 D.PVDF是混合物 組卷:23引用:2難度:0.7 -
3.下列有關化學用語表示正確的是( )
A.乙醇的結構簡式為:C2H6O B.羥基的電子式: 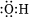
C.乙酸乙酯的分子式:C4H8O2 D.乙烯的球棍模型: 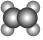 組卷:12引用:2難度:0.7
組卷:12引用:2難度:0.7 -
4.在2A+B?3C+4D反應中,表示該反應速率最快的是( )
A.v(A)=0.5mol/(L?s) B.v(B)=0.3mol/(L?s) C.v(C)=12mol/(L?min) D.v(D)=6mol/(L?min) 組卷:12引用:2難度:0.7 -
5.75%乙醇和84消毒液等是防疫期間常用物品,84消毒液的主要成分是次氯酸鈉。設NA為阿伏加德羅常數的值,下列說法正確的是( )
A.75%乙醇和84消毒液混合使用效果會更好 B.0.1mol/LNaClO溶液中n(HClO)+n(ClO-)=0.1mol C.1mol乙醇和丙三醇的混合物完全燃燒消耗O2大于3NA D.用氯氣和氫氧化鈉溶液反應制取74.5g次氯酸鈉消耗2.24L氯氣,轉移0.1NA電子 組卷:14引用:2難度:0.7 -
6.下列說法不正確的是( )
A.CH3OCHO與HCOOCH3互為同分異構體 B.乙酸和硬脂酸互為同系物 C. 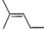 經催化加氫后生成物一氯代物有5種
經催化加氫后生成物一氯代物有5種D.白磷與紅磷互為同素異形體 組卷:12引用:2難度:0.7 -
7.“綠色化學”的理想狀態是反應物的原子全部轉化為目標產物。以下反應不符合綠色化學原則的是( )
A.工業生產環氧乙烷:2CH2=CH2+O2 2催化劑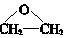
B.水煤氣合成甲醇:CO+2H2 CH3OH催化劑C.制取硫酸銅:Cu+2H2SO4(濃) CuSO4+SO2↑+2H2O△D.合成甲基丙烯酸甲酯:CH3C≡CH+CO+CH3OH CH2=C(CH3)COOCH3Pd組卷:78引用:5難度:0.9 -
8.下列說法中正確的是( )
A.在化學反應過程中,發生物質變化的同時不一定發生能量變化 B.生成物的總能量大于反應物的總能量,該反應為吸熱反應 C.一個化學反應能量變化多少與反應物和生成物的聚集狀態無關 D.破壞生成物全部化學鍵所需要的能量大于破壞反應物全部化學鍵所需要的能量時,該反應為吸熱反應 組卷:32引用:2難度:0.8 -
9.下列說法正確的是( )
A.糖類、蛋白質均屬于天然有機高分子化合物 B.FeCl3溶液和過量的KI溶液反應,可用淀粉溶液檢驗該反應是否為可逆反應 C.SO2可漂白紙漿,不可用于殺菌、消毒 D.實驗室用鋅和稀硫酸反應制氫氣,加入少量硫酸銅能加快反應速率 組卷:11引用:2難度:0.7
三、解答題(共4小題,滿分50分)
-
28.金屬礦物資源的利用有著非常重要的意義。
(1)金屬銅常用的冶煉方法是(填序號)。
A.熱分解法
B.熱還原法
C.電解法
D.濕法冶金
(2)工業上由黃銅礦(主要成分CuFeS2)冶煉銅的主要流程如圖: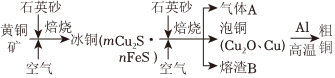
①氣體A中的大氣污染物可選用下列試劑中的吸收(填序號)。
a.濃H2SO4
b.稀HNO3
c.NaOH溶液
d.氨水
②用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈紅色,說明溶液中存在(填離子符號),檢驗溶液中還存在Fe2+的方法是(注明試劑、現象)。
③根據上述流程圖所示,由泡銅冶煉粗銅的化學反應方程式為。
(3)已知灼熱的氧化銅可以與氨反應得到氮氣和金屬銅,用圖中的裝置可以實現該反應。A中生成氨氣的化學方程式是,寫出C中發生反應的化學方程式:。試管D中收集到的物質是。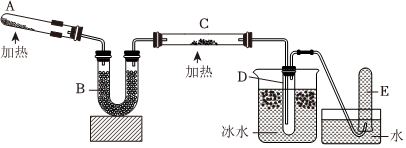 組卷:50引用:2難度:0.7
組卷:50引用:2難度:0.7 -
 29.乙酸乙酯是一種重要的化工原料,廣泛用于藥物染料、香料等工業。已知乙醇可以和氯化鈣反應生成微溶于水的CaCl2?6C2H5OH。
29.乙酸乙酯是一種重要的化工原料,廣泛用于藥物染料、香料等工業。已知乙醇可以和氯化鈣反應生成微溶于水的CaCl2?6C2H5OH。
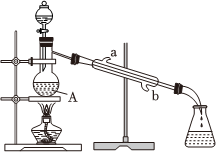
(一)實驗室合成乙酸乙酯的粗產品的步驟如下:制備乙酸乙酯粗產品:如圖所示的儀器裝置,在蒸餾燒瓶內將過量的乙醇與適量濃硫酸混合,然后經分液漏斗邊滴加乙酸,邊加熱蒸餾。得到含有乙醇、乙酸和水的乙酸乙酯粗產品。
(1)寫出蒸餾燒瓶中發生的化學反應方程式:。
(2)濃硫酸的作用是。
(3)冷凝水流經直形冷凝管時應從進入,從流出(填“a”或“b”)
(二)對乙酸乙酯進行精制
(4)為了除去粗產品其中的乙酸,可向產品中加入溶液,然后進行(填操作名稱)
(5)再向得到的有機物中加入飽和氯化鈣溶液,振蕩、分離,加入飽和氯化鈣溶液的目的是。
(6)最后,加入無水硫酸鈉除去其中的水分,再進行(填操作名稱),即可得到純凈的乙酸乙酯。
(7)用30g乙酸與46g乙醇反應合成乙酸乙酯,若實際產量是理論產量的70%,則實際得到乙酸乙酯的質量為g。組卷:28引用:2難度:0.6


