2019-2020學年浙江省金華市蘭溪外國語學校九年級(上)第一次月考化學試卷
發布:2024/11/29 17:0:2
一、選擇題
-
1.垃圾分一分,環境美十分。投放鋁制易拉罐的垃圾箱應貼以下哪個標識( )
A. 
可回收物B. 
廚余垃圾C. 
有害垃圾D. 
其他垃圾組卷:20引用:15難度:0.7 -
2.下列離子能在pH=1的無色溶液中大量共存的是( )
A.OH-、K+、NO3-、Ba2+ B.Cu2+、SO42-、Cl-、Na+ C.Na+、CO32-、Ca2+、Cl- D.Mg2+、SO42-、Al3+、NO3- 組卷:87引用:44難度:0.9 -
3.下列有關物質的分類正確的是( )
A.純堿、燒堿都屬于堿 B.塑料、羊毛屬于合成材料 C.淀粉、蛋白質屬于有機物 D.生石灰、熟石灰屬于氧化物 組卷:362引用:21難度:0.9 -
4.下列除雜質所用的試劑和方法不正確的是( )
選項 物質 雜質 除雜質所用的試劑和方法 A KOH K2CO3 Ca(OH)2溶液,過濾 B CO2 O2 反復通過灼熱的炭層 C CuO CaO 水,過濾、洗滌、干燥 D 銅粉 鐵粉 稀鹽酸,過濾、洗滌、干燥 A.A B.B C.C D.D 組卷:18引用:2難度:0.5 -
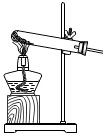 5.如圖是硫與鐵的反應實驗裝置:將硫粉與鐵粉混合后裝進試管里,然后用酒精燈加熱使其發生反應,停止加熱,仍能看到發出的光擴展至整支試管。下列說法正確的是( )
5.如圖是硫與鐵的反應實驗裝置:將硫粉與鐵粉混合后裝進試管里,然后用酒精燈加熱使其發生反應,停止加熱,仍能看到發出的光擴展至整支試管。下列說法正確的是( )A.鐵發生了還原反應 B.該反應的生成物在類別上屬于鹽 C.硫失去了電子 D.該反應是吸熱反應 組卷:17引用:2難度:0.6 -
6.類推是一種重要的學習方法,但如果不具體問題具體分析就會產生錯誤的結論。下列類推結論錯誤的是( )
①HCl能與Fe反應生成H2,HCl也能與Zn反應生成H2
②NaOH溶液能使無色酚酞試液變紅色,Cu(OH)2也能使無色酚酞試液變紅色
③堿溶液呈堿性,能使無色酚酞變紅,則呈堿性的溶液一定是堿溶液
④酸和堿反應生成鹽和水,則生成鹽和水的反應一定是酸和堿的反應A.②③④ B.①② C.①③ D.①②③ 組卷:135引用:3難度:0.7 -
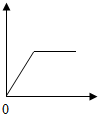 7.從圖象獲取信息是化學學習的重要技能。在分析圖象時,要注意橫坐標與縱坐標表示的含義。結合表格與圖進行分析,能夠正確的反映圖象關系的選項是( )
7.從圖象獲取信息是化學學習的重要技能。在分析圖象時,要注意橫坐標與縱坐標表示的含義。結合表格與圖進行分析,能夠正確的反映圖象關系的選項是( ) 選項 變化過程 橫坐標表示 縱坐標表示 A. 氧化鈣固體敞口放置在空氣中 放置時間 固體質量 B. 向氫氧化鈣溶液中逐滴加入碳酸鈉溶
液至過量碳酸鈉溶液質量 沉淀質量 C. 向20℃的不飽和氯化鈉溶液中逐漸加
入氯化鈉固體加入氯化鈉固體
質量溶劑質量 D. 向氫氧化鈉溶液中逐漸加水 水的質量 溶液pH A.A B.B C.C D.D 組卷:113引用:3難度:0.9 -
8.如圖是硫酸銅溶液與過量鐵粉反應前后溶液中主要離子變化示意圖,下列說法正確的是( )
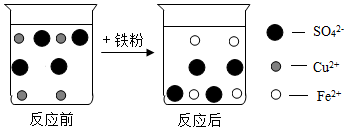
A.該反應的化學方程式為:2Fe+3CuSO4═Fe2(SO4)3+3Cu B.該反應過程中沒有變化的粒子是 SO2-4C.該反應過程中發生改變的粒子只有Cu2+ D.反應現象為有紅色固體析出,溶液由淺綠色變成藍色 組卷:377引用:6難度:0.4 -
9.對實驗現象的觀察和分析,有助于獲得化學知識并學會科學探究的方法.下列對實驗現象的分析合理的是( )
A.向某無色溶液中滴入酚酞試液,呈紅色,證明該溶液是堿溶液 B.向某無色溶液中滴入硝酸銀溶液,產生白色沉淀,證明該溶液是鹽酸 C.某白色固體與熟石灰混合后加熱,產生可使濕潤的紅色石蕊試紙變藍色的氣體,證明該固體是銨鹽 D.把燃著的木條伸入某無色氣體的集氣瓶中,火焰熄滅,證明該氣體是二氧化碳 組卷:214引用:32難度:0.9
四、分析計算題
-
26.為了測定某品牌食用純堿中碳酸鈉的質量分數,小明取10克食用純堿樣品和足量的溶質質量分數為10%的稀硫酸,進行如圖甲實驗,實驗前后,均需往裝置中緩慢通一會兒氮氣.(樣品中其他成分不與稀硫酸反應)
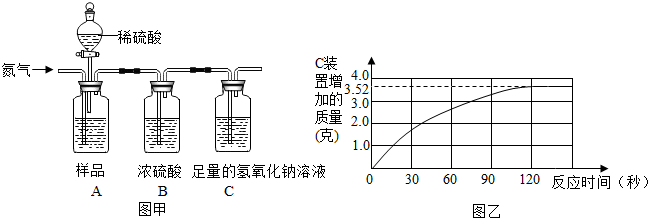
(1)實驗前,先往A裝置通入一會兒氮氣的目的是,B裝置的作用.
(2)若將稀硫酸換為濃鹽酸,實驗中C裝置增加的質量會偏大,請說明理由.
(3)隨著純堿樣品與稀硫酸反應,C裝置增加的質量變化情況如圖乙所示,則該食用純堿中碳酸鈉的質量分數是多少?組卷:31引用:2難度:0.5 -
 27.有一包固體粉末,由CaCO3、Na2SO4、CuSO4、Na2CO3中的一種或幾種組成,某實驗小組對其組成成分進行了以下探究活動。(注:Na2CO3溶液與CuSO4溶液混合能產生藍色沉淀。)
27.有一包固體粉末,由CaCO3、Na2SO4、CuSO4、Na2CO3中的一種或幾種組成,某實驗小組對其組成成分進行了以下探究活動。(注:Na2CO3溶液與CuSO4溶液混合能產生藍色沉淀。)
活動1:取一定量上述固體粉末,加足量水溶解。得到藍色澄清溶液,則原固體粉末中一定沒有(填化學式)。
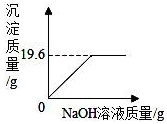
活動2:為進一步確定原固體粉末的組成,該實驗小組同學先用托盤天平稱取43.6g該粉末,溶于水配成219.6g溶液,再往其中加入溶質質量分數為8%的NaOH溶液,產生沉淀的質量與所加NaOH溶液質量的關系如圖所示。
(1)計算產生最大沉淀量時所加NaOH溶液的質量。(寫出過程)
(2)計算恰好完全反應時所得溶液中溶質的質量分數。(寫出過程)組卷:10引用:3難度:0.1


