人教版(2019)選擇性必修1《專題1 化學反應的熱效應(2)》2023年同步練習卷(1)
發布:2024/8/16 11:0:4
一、選擇題
-
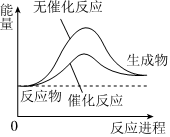
1.過氧化氫分解反應過程中,能量變化如圖所示:下列說法正確的是( )

A.催化劑可以改變過氧化氫分解反應的焓變 B.MnO2或FeCl3可以催化H2O2分解反應 C.催化劑不能改變反應路徑 D.H2O2分解是吸熱反應 組卷:46引用:5難度:0.6 -
 2.下列說法正確的是( )
2.下列說法正確的是( )A.如圖可表示水分解過程中的能量變化 B.若2C(s)+O2(g)═2CO(g)△H=-221.0 kJ/mol,則碳的燃燒熱為110.5 kJ/mol C.需要加熱的反應一定是吸熱反應,常溫下能發生的反應一定是放熱反應 D.已知I:反應H2(g)+Cl2(g)═2HCl(g)△H=-a kJ/mol,Ⅱ: 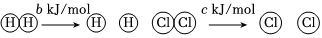
且a、b、c均大于零,則斷開1 mol H-Cl鍵所需的能量為(-a-b-c)kJ/mol組卷:37引用:6難度:0.9 -
3.在下列各說法中,正確的是( )
A.熱化學方程式中的化學計量數只表示物質的量,可以是分數 B.ΔH>0表示放熱反應,ΔH<0表示吸熱反應 C.1molH2SO4與1molBa (OH)2反應生成沉淀BaSO4時放出的熱叫做中和熱 D.1molH2與0.5molO2反應放出的熱就是H2的燃燒熱 組卷:87引用:8難度:0.6 -
4.下列說法正確的是( )
A.放熱的化學反應不需要加熱就能發生 B.物質燃燒不一定是放熱反應 C.化學反應除了生成新的物質外,還伴隨著能量的變化 D.吸熱反應不加熱就不會發生 組卷:3引用:2難度:0.9 -
5.已知化學反應2C(s)+O2(g)
2CO(g),2CO(g)+O2(g)點燃2CO2(g)都是放熱反應。據此判斷,下列說法中不正確的是( )點燃A.12g C所具有的能量一定高于28gCO所具有的能量 B.56gCO和32gO2所具有的總能量大于88gCO2所具有的總能量 C.12gC和32gO2所具有的總能量大于44gCO2所具有的總能量 D.將一定質量的C燃燒,生成CO2比生成CO時放出的熱量多 組卷:111引用:38難度:0.9 -
6.氫氣在氯氣中燃燒產生蒼白色火焰,在反應中破壞1mol氫氣中的化學鍵消耗的能量為akJ,破壞1mol氯氣中的化學鍵消耗的能量為bkJ,形成1mol氯化氫中的化學鍵釋放的能量為ckJ.下列關系式中正確的是( )
A.a+b=c B.a+b>2c C.a+b=2c D.a+b<2c 組卷:16引用:4難度:0.7
三、解答題
-
 18.為了研究化學反應A+B=C+D的能量變化情況,某同學設計了如圖所示裝置。當向盛有A的試管中滴加試劑B時,看到U形管中甲處液面下降乙處液面上升。試回答下列問題:
18.為了研究化學反應A+B=C+D的能量變化情況,某同學設計了如圖所示裝置。當向盛有A的試管中滴加試劑B時,看到U形管中甲處液面下降乙處液面上升。試回答下列問題:
(1)該反應為反應(填“放熱”或“吸熱”)。
(2)A和B的總能量比C和D的總能量(填“高”或“低’’)。
(3)反應物化學鍵斷裂吸收的能量(填“高’’或“低’’)于生成物化學鍵形成放出的能量。
(4)寫出一個符合題中條件的化學方程式:。組卷:20引用:3難度:0.7 -
 19.回答下列問題:
19.回答下列問題:
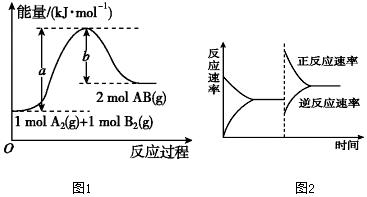
Ⅰ.(1)已知化學反應A2(g)+B2(g)=2AB(g)的能量變化如圖1所示:
①該反應的ΔH0(填“大于”“小于”或“等于”)。
②反應物的總鍵能為。
③寫出該反應的熱化學方程式。
(2)聯氨(又稱肼,N2H4,無色液體)是一種應用廣泛的化工原料,可用作火箭燃料,回答下列問題:
①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ΔH4=-1048.9kJ?mol-1
上述反應熱效應之間的關系式為ΔH4=,聯氨和N2O4可作為火箭推進劑的主要原因為。(至少答兩條)
Ⅱ.合成氨工業在工農業生產、生活中有著重要作用。反應原理為3H2(g)+N2(g)?2NH3(g) ΔH<0。
(3)在T℃時,將一定物質的量的H2和N2置于一容積不變的密閉容器中。
①下列各項能說明該反應已達到平衡狀態的是(填序號)。
a.容器內的壓強不再隨時間變化
b.3v(N2)=v(H2)
c.3v正(H2)=2v逆(NH3)
d.混合氣體的密度保持不變
②上述反應達到平衡后,其他條件不變,升高溫度,v逆(填“增大”“不變”或“減小”),v正和v逆的關系為v正v逆(填“>”“=”或“<”),最后二者相等。
③該條件下達到平衡時,向容器內充入惰性氣體,增大容器內的壓強,NH3的體積分數將(填“變大”“不變”或“變小”)。
(4)在T℃時,將一定物質的量的H2和N2置于一容積可變的密閉容器中。達到平衡后,改變某一條件使反應速率發生了如圖2所示的變化,改變的條件可是。
a.升高溫度,同時加壓
b.降低溫度,同時減壓
c.保持溫度、壓強不變,增大反應物濃度
d.保持溫度、壓強不變,減小生成物濃度組卷:14引用:2難度:0.7


