2021-2022學年上海市宜川中學高一(下)期末化學試卷
發布:2024/4/20 14:35:0
一、選擇題(每小題一個正確答案,每題2分)
-
1.工農業生產中用途最廣、用量最多的金屬是( )
A.銅 B.鐵 C.金 D.鋁 組卷:72引用:2難度:0.8 -
2.同位素常用做環境分析指示物,下列對同位素的說法正確的是( )
A.34S原子核內的中子數為16 B.16O與 18O的核電荷數相等 C.13C和15N原子核內的質子數相差2 D.2H+質量與1H+的質量相同 組卷:124引用:2難度:0.6 -
3.下列物質在常溫下接觸時無明顯現象的是( )
A.鐵和濃鹽酸 B.鐵和稀硫酸 C.鐵和濃硫酸 D.鐵和稀硝酸 組卷:41引用:2難度:0.7 -
4.下列各物質中,不能由組成它的兩種元素的單質直接化合得到的是( )
A.FeS B.FeCl2 C.FeCl3 D.Fe3O4 組卷:77引用:14難度:0.9 -
5.鋁分別與足量的稀鹽酸和氫氧化鈉溶液反應,當兩個反應放出的氣體在相同狀況下體積相等時,反應中消耗的HCl和NaOH的物質的量之比是( )
A.1:1 B.2:1 C.1:3 D.3:1 組卷:107引用:10難度:0.9 -
6.鋁能提煉難熔金屬和制成鋁熱劑,是因為鋁( )
A.密度小,熔點較低 B.具有還原性,且生成氧化鋁時放出大量熱 C.在空氣中燃燒,發出耀眼白光 D.是金屬 組卷:133引用:7難度:0.9 -
7.鎂粉中混進少量鋁粉,將鋁粉除去,可選用的試劑是( )
A.氫氧化鈉溶液 B.硫酸銅溶液 C.鹽酸 D.水 組卷:31引用:2難度:0.5 -
8.下列有關物質性質的比較,錯誤的是( )
A.金屬性:Mg>Al B.穩定性:HF>HCl C.堿性:NaOH>Mg(OH)2 D.酸性:HClO3>H2SO3 組卷:28引用:2難度:0.9 -
9.在密閉容器中發生反應H2(g)+I2(g)?2HI(g),0~5min內H2的濃度減少了0.1mol/L,則在這段時間內用HI表示的平均反應速率[mol/(L?min)]為( )
A.0.01 B.0.04 C.0.2 D.0.5 組卷:102引用:5難度:0.7
二、綜合分析題(共50分)
-
28.煤是重要能源。燃煤會釋放SO2、CO等有毒氣體。消除有毒氣體的研究和實踐從未停止。用CaSO4可消除CO。
反應①:CaSO4(s)+4CO(g)?CaS(s)+4CO2(g) (放熱反應)
反應②:CaSO4(s)+CO(g)?CaO(s)+SO2(g)+CO2(g) (吸熱反應)
(1)其他條件不變,增加CaSO4(的用量(質量),反應①的速率
a.增大
b.減小
c.不變
d.無法判斷
(2)若在容積為1L的密閉裝置中僅發生反應①,20分鐘后,固體的質量減少了3.2g,則CO2的反應速率為,不能說明反應①一定達到平衡狀態的是。
A.壓強不變
B.氣體的密度不變
C.v正(CO)=v逆(CO2)
D.CO、CO2濃度相等
(3)為了提高反應②的CO的吸收率,可行的措施是、(2條)。
(4)補全如圖中反應②的能量變化示意圖(即注明生成物能量的大致位置)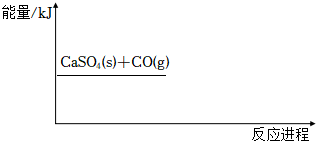
(5)若反應①、②同時發生,一段時間后均到達了平衡,升高溫度,均再次達到平衡,發現CO的吸收率減小,分析可能的原因是。組卷:26引用:2難度:0.5 -
29.高鐵酸鉀(K2FeO4)是優質水處理劑。實驗室制取K2FeO4的裝置如圖。K2FeO4的制備原理為:3Cl2+2Fe(OH)3+10KOH=2K2FeO4+6KCl+8H2O。
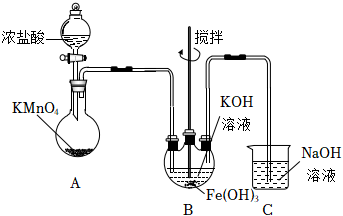
回答下列問題
(1)A裝置的作用是。盛濃鹽酸的儀器名稱為。
(2)裝置C的作用是。B裝置內出現現象時,說明B中反應已停止。
(3)K2FeO4中鐵元素的化合價為,分析K2FeO4是優質水處理劑的原因可能是。
(4)當上述反應消耗標準狀況下672mLCl2時,生成K2FeO4質量為。組卷:13引用:4難度:0.5


