2020-2021學年遼寧省名校聯盟高三(下)開學化學試卷
發布:2024/11/3 15:0:2
一、選擇題:本題共15小題,每小題3分,共45分。每小題只有一個選項符合題目要求。
-
1.化學與生活密切相關,下列說法正確的是( )
A.芯片制造中的“光刻技術”是利用光敏樹脂曝光成像,該過程涉及化學變化 B.推廣使用煤液化技術,可減少二氧化碳等溫室氣體的排放 C.汽車尾氣中含有的氮氧化物,是汽油不完全燃燒造成的 D.古人煮沸海水制取淡水,現代可向海水中加明礬實現淡化 組卷:29引用:3難度:0.7 -
2.已知反應3NH3+3Cl2═NH4Cl+5HCl+N2,其中用化學用語描述的相關微粒正確的是( )
A.中子數為18的氯原子: Cl1817B.NH4Cl屬于離子化合物,不含共價鍵 C.NH4+的結構式: 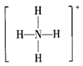
D.N2的電子式: 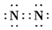 組卷:26引用:4難度:0.8
組卷:26引用:4難度:0.8 -
3.X、Y、Z、W均為短周期主族元素,且原子序數依次遞增。基態X原子核外有電子的能級是3個,且3個能級上的電子數相等,W與X同主族,Y的氫化物與其最高價氧化物對應的水化物可形成一種鹽,Z為所在周期中原子半徑最大的元素。下列說法正確的是( )
A.電負性:Z>W>X>Y B.簡單氫化物的穩定性:W>Y>X C.X的含氧酸與Y的氫化物形成的化合物中都只含離子鍵 D.Z與W形成的含氧酸鹽的溶液顯堿性 組卷:15引用:2難度:0.5 -
4.我國對銅的認識年代久遠,下列關于銅的幾種表述正確的是( )
A.基態Cu原子的電子排布式:[Ar]4s1 B.基態Cu原子的最高能層符號為N C.基態Cu原子的價電子排布圖為 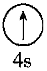
D.基態Cu2+的未成對電子數為2 組卷:23引用:1難度:0.6 -
5.利用下列裝置(夾持裝置略)進行實驗,不能達到實驗目的的是( )
A. 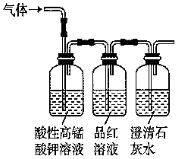
用此裝置檢驗SO2中是否混有CO2B. 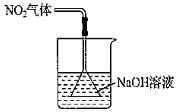
用此裝置防止倒吸C. 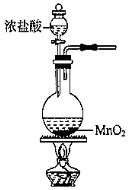
用此裝置制取Cl2D. 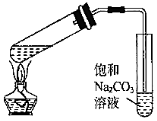
用此裝置制備并收集乙酸乙酯組卷:10引用:1難度:0.7 -
6.維生素B5可以減輕抗生素等藥物引起的毒副作用,其結構為
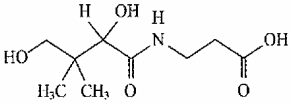 。下列關于維生素B5的說法正確的是( )
。下列關于維生素B5的說法正確的是( )A.該物質可發生消去反應生成碳碳雙鍵 B.分子中含有8個碳原子 C.一定條件下,1mol維生素B5最多可與1mol NaOH發生反應 D.該物質以及所有的水解產物均能發生聚合反應 組卷:9引用:3難度:0.7
二、非選擇題:本題共4題,共55分。
-
18.鋰輝礦是生產鋰離子電池的重要礦物資源。鋰輝礦的主要成分為LiAlSi2O6,主要雜質為Fe2O3。鹽焙燒工藝提取鋰輝礦中鋰的工藝流程如圖所示。
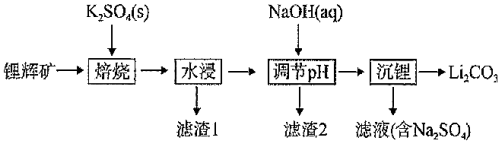
已知:①Al(OH)3的Ksp=1.0×10-33,Fe(OH)3的Ksp=4×10-38,溶液中離子濃度小于10-5mol?L-1時,即認為沉淀完全。
②碳酸鋰在不同溫度下的溶解度如表所示。
回答下列問題:溫度/℃ 0 10 20 50 75 100 Li2CO3的溶解度/g 1.539 1.406 1.329 1.181 0.866 0.728
(1)已知濾渣1的主要成分是K2O?Al2O3?4SiO2,“焙燒”過程發生反應的化學方程式為。
(2)“水浸”過程中,為提高浸出速率,可采取的措施有、(寫出兩條);加入NaOH溶液的目的是去除Al3+和Fe3+,“調節pH”過程需要調節pH的范圍是。
(3)“沉鋰”過程發生反應的化學方程式為。
(4)洗滌產品Li2CO3需要使用(填“冷水”或“熱水”),理由是,檢驗已洗滌干凈的方法是。
(5)某工廠用at鋰輝礦(含LiAlSi2O693%)制得bt Li2CO3,則Li2CO3的產率為。組卷:7引用:1難度:0.5 -
19.化合物G是藥物合成中一種重要的中間體,其合成路線如圖。
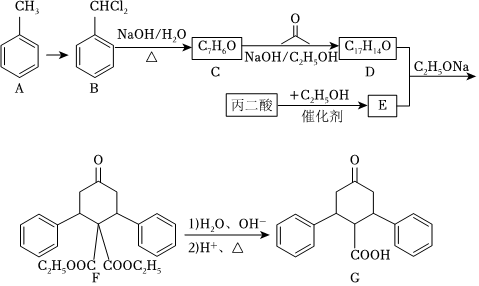
已知:(1)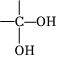 →
→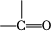 +H2O;
+H2O;
(2)R1CHO+R2CH2CHO一定條件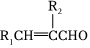 +H2O(R1、R2為烴基或H);
+H2O(R1、R2為烴基或H);
(3)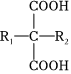 △
△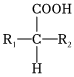 +CO2↑(R1和R2代表烷基)。
+CO2↑(R1和R2代表烷基)。
回答下列問題:
(1)寫出A到B的試劑與反應條件為,C的名稱為。
(2)D的結構簡式為。
(3)丙二酸生成E的反應類型為。
(4)B生成C的化學方程式是。
(5)B的芳香族化合物的同分異構體共有種(不考慮立體異構),其中核磁共振氫譜有3組峰的同分異構體的結構簡式為。(任寫一種)
(6)設計以CH2=CHCH3為原料合成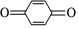 的合成路線:。(無機試劑任選)組卷:24引用:2難度:0.5
的合成路線:。(無機試劑任選)組卷:24引用:2難度:0.5


