2021-2022學年重慶市縉云教育聯盟高一(上)質檢化學試卷(11月份)
發布:2024/11/18 17:30:3
一、選擇題(共25小題,每小題3分,滿分75分)
-
1.化學與生產、生活、社會密切相關,下列有關說法不正確的是。( )
A.德爾塔新冠病毒有可能在空氣中以氣溶膠的形式傳播,氣溶膠屬于膠體 B.“地溝油”經過加工處理可用來制肥皂,實現了廚余垃圾的合理利用 C.光化學煙霧、臭氧空洞、溫室效應的形成都與氮氧化物有關 D.推廣電動汽車和開展植樹造林有利于碳達峰和碳中和 組卷:11引用:2難度:0.7 -
2.分類法是化學學習和研究的重要思想方法。下列有關物質的分類或說法正確的是( )
A.根據樹狀分類法可知,碳酸鈉屬于鈉鹽、碳酸鹽、正鹽 B.淀粉、蛋白質、纖維素、油脂都是高分子化合物,氨水、王水、冰水混合物都是混合物 C.SiO2、Cl2O、Mn2O7,均為酸性氧化物,Na2O、Al2O3、CaO2均為堿性氧化物 D.H3PO4、H2PO4、HAlO2均為含氧酸,CH3COOH、H3BO3(硼酸)、H3PO2(次磷酸)均為一元酸 組卷:10引用:2難度:0.6 -
3.下列有機物屬于電解質的是( )
A.苯 B.酒精 C.己烷 D.甲酸 組卷:30引用:3難度:0.6 -
4.運用元素周期律分析下面的推斷,其中不正確的是( )
A.鈹(Be)的氧化物的水化物具有兩性 B.砹(At)為有色固體,AgAt感光性很強,不溶于水 C.硫酸鍶(SrSO4)是難溶于水的白色固體 D.硒化氫(H2Se)是無色、有毒,比H2S穩定的氣體 組卷:122引用:4難度:0.8 -
5.下列關于離子鍵的說法中,正確的是( )
A.陰、陽離子間的相互吸引即離子鍵 B.非金屬元素所組成的化合物中不可能有離子鍵 C.ⅠA族元素與ⅦA族元素之間形成的化合物一定含離子鍵 D.某化合物在熔融狀態下能導電,該化合物一定含離子鍵 組卷:116引用:5難度:0.7 -
6.由一種陽離子與兩種酸根陰離子組成的鹽稱為混鹽,氯化次氯酸鈣(CaOCl2)是一種常見的混鹽。下列說法不正確的是( )
A.CaOCl2有較強的氧化性 B.該混鹽可能具有漂白性 C.由氯氣和石灰乳為原料,每生成1mol CaOCl2,轉移的電子為2mol D.CaOCl2的溶液中加入足量濃硫酸,可有黃綠色的氣體產生 組卷:19引用:4難度:0.7 -
7.下列反應屬于置換反應的是( )
A.Na2CO3+H2SO4═Na2SO4+CO2↑+H2O B.Br2+2KI═I2+2KBr C.Cl2+H2O?HCl+HClO D.H2O+NaH═NaOH+H2↑ 組卷:3引用:2難度:0.8 -
8.下列操作或操作中使用的試劑正確的是( )
A.用酒精萃取碘水中的碘 B.稱量NaOH固體時,將NaOH固體放在墊有濾紙的托盤上 C.用丁達爾效應可以區分氯化鐵溶液和氫氧化鐵膠體 D.分液時,分液漏斗中下層液體先從下口放出,上層液體再從下口流出 組卷:7引用:2難度:0.7 -
9.下列關于鈉及其化合物的說法中,不正確的是( )
A.火災現場存放有大量金屬鈉時,需要用干燥的沙土來滅火 B.金屬鈉可在呼吸面具或潛水艇中作為氧氣的來源 C.過氧化鈉晶體中陰、陽離子個數比為1:2 D.相同條件下,純堿在水中的溶解度大于小蘇打 組卷:52引用:3難度:0.7 -
10.學生甲在做以下實驗時,在確認刻度線處讀數時由于俯視刻度線,造成實驗誤差(其它操作無誤),學生乙對其實驗結果進行分析評價,以下所得結論正確的是( )
選項 實驗 結論 A 配制溶液定容時確認液面是否達到刻度線 所配溶液的物質的量濃度
偏小B 常溫下用量筒量取10.0mLpH=12的NaOH溶液 所量取的溶液中OH-的物質的量大于10-4mol C 用堿式滴定管量取15.00mL的氫氧化鈉待測液,放液后讀取氫氧化鈉待測液的體積 所量取的氫氧化鈉待測液體積偏小 D 滴定未知濃度的氫氧化鈉待測液,滴定終點時讀取酸式滴定管內標準鹽酸的體積 氫氧化鈉待測液濃度偏小 A.A B.B C.C D.D 組卷:3引用:2難度:0.6
二、解答題(共6小題,滿分0分)
-
30.(1)①寫出“海洋元素”的元素符號
,②寫出鋇餐的化學式:。
(2)鎂失火時不能用二氧化碳滅火,用化學方程式表示其原因。
(3)《新修本草》有云:“青礬( FeSO4?7H2O)本來綠色,新出窟未見風者,正如瑁璃…燒之赤色…。”根據以上信息,寫出“青礬”受熱分解的化學方程式。
(4)雙氧水能使酸性高錳酸鉀溶液褪色,請完成以下相關反應的離子方程式:MnO4-+H2O2+=Mn2++H2O+。組卷:429引用:2難度:0.5 -
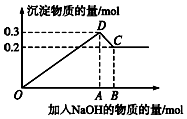 31.在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至過量.經測定,加入的NaOH的物質的量(mol)和所得沉淀的物質的量(mol)的關系如圖所示.
31.在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至過量.經測定,加入的NaOH的物質的量(mol)和所得沉淀的物質的量(mol)的關系如圖所示.
(1)CD段發生反應的離子方程式:.
(2)原溶液中Mg2+、Al3+的物質的量之比為.
(3)圖中D點表示加入mol NaOH.
(4)圖中線段OA:AB=.組卷:21引用:2難度:0.3


