2022-2023學年陜西省西安市藍田縣高二(下)期末化學試卷
發布:2024/6/27 8:0:9
一、本卷共25小題,每小題2分,共50分。在每小題給出的四個選項中,只有一項是符合要求的。
-
1.短周期元素M、W、X、Y、Z在元素周期表中的位置如下所示,其中M、W、X的原子序數之和等于30。下列判斷正確的是( )
M W X Y Z A.M的氫化物與Z的氫化物反應所得產物的水溶液呈中性 B.最高價氧化物的水化物的酸性H3XO4強于HMO3 C.X與Z形成的所有化合物分子中,各原子均滿足8電子穩定結構 D.Y與Z的最高正化合價之和的數值等于13 組卷:25引用:2難度:0.5 -
2.室溫下,0.1mol?L-1 HF溶液與0.1mol?L-1 NaOH溶液等體積混合(忽略混合前后溶液體積的變化),則下列有關混合后的溶液中離子濃度的敘述正確的是( )
A.由水電離產生的c(H+)為1.0×10-7mol?L-1 B.c(F-)+c(HF)=c(Na+) C.升高溫度,c(F-)增大 D.c(F-)>c(Na+)>c(H+)>c(OH-) 組卷:18引用:9難度:0.9 -
3.鐵和氧化鐵的混合物共a mol,加一定量鹽酸后固體全部溶解,得到的溶液中不含Fe3+,同時收集到b mol氫氣,則原混合物中氧化鐵的物質的量為( )
A. (a-b)mol12B. (a+b)mol12C.(a-b)mol D.b mol 組卷:25引用:6難度:0.7 -
4.下列說法正確的是( )
A.相同物質的量濃度的下列溶液中,①NH4Al(SO4)、②NH4Cl、③CH3COONH4、④NH3?H2O;c( )由大到小的順序是:①>②>③>④NH+4B.某物質的溶液中由水電離出的c(H+)=1×10-amol/L,若a>7時,則該溶液的pH一定為14 C.物質的量濃度相等的H2S和NaHS混合溶液中:c (Na+)+c(H+)=c (S2-)+c (HS-)+c (OH-) D.AgCl懸濁液中存在平衡:AgCl(s)?Ag+(aq)+Cl-(aq),往其中加入少量NaCl粉末,平衡會向左移動,Ksp減少 組卷:157引用:2難度:0.5 -
5.某種興奮劑的結構如圖所示,下列說法正確的是( )
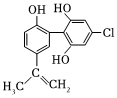
A.該物質遇FeCl3溶液顯紫色,屬于苯酚的同系物 B.1mol該物質分別與濃溴水和NaOH溶液反應時,最多消耗Br2和NaOH均為4mol C.滴入酸性KMnO4溶液振蕩,紫色褪去即證明該物質結構中存在碳碳雙鍵 D.該分子中所有碳原子均可能位于同一平面 組卷:5引用:7難度:0.7 -
6.把300ml有BaCl2和AlCl3的混合溶液分成3等份,取一份加入含a mol硫酸鈉的溶液,恰好使鋇離子完全沉淀;另取一份加入等體積4bmol/L氫氧化鈉溶液,恰好使產生的沉淀溶解.則該混合溶液中氯離子濃度為( )
A.20a+3b B.20a/3+b C.2a+3b D.10a+2b 組卷:27引用:5難度:0.7 -
7.下列表示對應化學反應的離子方程式正確的是( )
A.向含有Fe2O3懸濁液中通入HI:Fe2O3+6H+=2Fe3++3H2O B.NaHSO4溶液中滴入Ba(OH)2溶液至SO42-完全沉淀:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O C.醋酸溶液與水垢中的CaCO3反應:CaCO3+2H+=Ca2++H2O+CO2↑ D.將1 mol/L NaAlO2溶液和1.5 mol/L HCl溶液等體積互相均勻混合:6AlO2-+9H++3H2O=5Al(OH)3↓+Al3+ 組卷:20引用:10難度:0.9 -
8.將11.9g由Mg、Al、Fe組成的合金溶于足量的NaOH溶液中,合金質量減少了2.7g.另取等質量的合金溶于過量稀硝酸中,生成了6.72L NO(標準狀況下),向反應后的溶液中加入過量的NaOH溶液,則最終所得沉淀的質量為( )
A.22.1 g B.27.2 g C.30 g D.19.4 g 組卷:138引用:5難度:0.7 -
9.下列各組中的兩種物質相互反應時,無論哪種過量,都可用同一個離子方程式表示的有( )
①碳酸鈉溶液與鹽酸
②偏鋁酸鈉溶液與鹽酸
③硫酸鋁溶液與氨水
④碳酸氫鈣溶液與澄清石灰水
⑤碘化亞鐵溶液與氯水
⑥鐵與稀硝酸A.1個 B.2個 C.4個 D.5個 組卷:43引用:2難度:0.7 -
10.下列解釋事實的方程式不正確的是( )
A.金屬鈉露置在空氣中,光亮表面顏色變暗:4Na+O2=2Na2O B.鋁條插入燒堿溶液中,開始沒有明顯現象:Al2O3+2OH-=2 +H2OAlO-2C.鐵溶于稀硝酸,溶液變為淺綠色:3Fe+8H++2 =3Fe2++2NO↑+4H2ONO-3D.硫酸銨溶液與氫氧化鋇溶液混合,產生氣體: +OH-=NH3↑+H2ONH+4組卷:84引用:2難度:0.8
第II卷(非選擇題)本卷均為必考題,共5大題50分。請考生將答案寫在答題卡相應位置。
-
29.我國科學家選取了33個土壤樣本,分別測定大量元素(N、Ca、K、Fe、P)、微量元素(Mn、Zn、Cu、Co、Sn)和重金屬(Pb、Cr、Ag、Cd、Hg)的含量,研究表明:15種礦物元素中,5種元素(P、Cu、Zn、Co、
Pb)的含量與地理位置有關。
回答下列問題:
(1)基態錳原子的價層電子排布式為。
(2)基態鈣原子的核外電子云輪廓圖呈球形的能級上填充個電子,基態鉀原子的核外電子云有個伸展方向。
(3)NH3與H2O可與Zn2+形成配合物[Zn(NH3)3(H2O)]2+。與Zn2+形成配位鍵的原子是(填元素符號);寫出一種與NH3互為等電子體的陽離子:(填化學式)。
(4)《中華本草》等中醫典籍中,記載了爐甘石(ZnCO3)入藥,可用于治療皮膚炎癥或表面創傷,在ZnCO3中,陰離子空間構型為。
(5)已知KH2PO4是次磷酸的正鹽,H3PO2的結構式為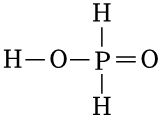 ,其中P采取 雜化方式。
,其中P采取 雜化方式。
(6)某磷青銅晶胞結構如圖所示: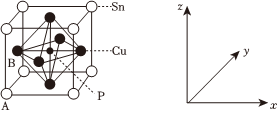
①其中原子坐標參數A為(0,0,0);B為(0,,12)。則P原子的坐標參數為12。
②該晶體中距離Cu原子最近的Sn原子有個。
③若晶體密度為ag?cm3,最近的Cu原子核間距為pm(用含NA和a的代數式表示)。組卷:23引用:3難度:0.7 -
30.化合物G是合成藥物鹽酸沙格雷酯的重要中間體,其合成路線如圖。
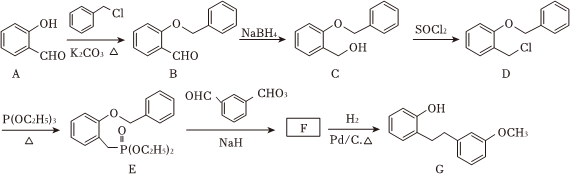
(1)A與對羥基苯甲醛互為同分異構體。A的熔點比對羥基苯甲醛的低,其原因是。
(2)可用于鑒別A與B的常用化學試劑為。
(3)B→C的反應中,“-CHO”被轉化為“-CH2OH”,相應的碳原子軌道雜化類型的變化為。
(4)上述合成路線中,F的分子式為C22H20O2,其結構簡式為。
(5)請設計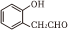 和
和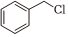 為原料制備
為原料制備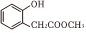 的合成路線 。(無機試劑和兩碳以下的有機試劑任用,合成路線示例見本題題干)組卷:71引用:3難度:0.6
的合成路線 。(無機試劑和兩碳以下的有機試劑任用,合成路線示例見本題題干)組卷:71引用:3難度:0.6


