2020-2021學年浙江省臺州市臨海市尤溪中學九年級(上)期中科學試卷
發布:2024/4/20 14:35:0
一、選擇題(本大題共15小題,每題4分,共計60分)
-
1.2020年春,“新冠病毒”肆虐,全國上下齊心協力、眾志成城,堅決打贏“新冠肺炎”阻擊戰。下列行動中發生了化學變化的是( )
A. 
排查統計B. 
分發口罩C. 
消毒殺菌D. 
測量體溫組卷:1引用:2難度:0.5 -
2.下列用途中,不屬于氫氧化鈣的用途是( )
A.在農業上常用來改良酸性土壤 B.用作建筑材料,用來抹墻 C.常用來檢驗銨鹽的存在 D.廣泛用于制肥皂、造紙等工業 組卷:3引用:1難度:0.5 -
3.下列物質長時間敞口放置在空氣中,質量增加并發生化學反應的是( )
①燒堿②生石灰③濃鹽酸④濃硫酸⑤熟石灰⑥鐵釘A.①②④ B.①②⑤ C.①②⑤⑥ D.①②④⑤⑥ 組卷:3引用:1難度:0.5 -
4.實驗室的藥品是按照物質分類的方式存放的,下列四個藥品柜已存放了下列藥品,現學實驗室新購進一瓶硫酸銅,正確存放它的藥品柜是( )
藥品柜 A甲柜 B乙柜 B丙柜 C丁柜 藥品 氯化鈉 氯化鈣 氫氧化鈉 氫氧化鈣 鹽酸 硫酸 銅 鐵 A.A B.B C.C D.D 組卷:0引用:1難度:0.5 -
5.下列實驗操作中,正確的是( )
A. 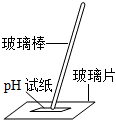
測定溶液的pHB. 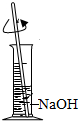
溶解NaOH固體C. 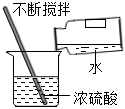
稀釋濃硫酸D. 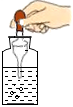
用滴管取液體組卷:0引用:1難度:0.5 -
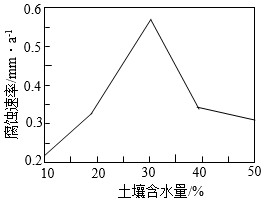 6.長期埋在地下的金屬管線會被腐蝕。常溫下,某金屬管線腐蝕速率與土壤含水量的關系如圖所示,下列說法正確的是( )
6.長期埋在地下的金屬管線會被腐蝕。常溫下,某金屬管線腐蝕速率與土壤含水量的關系如圖所示,下列說法正確的是( )A.土壤含水量越高,金屬腐蝕速率越快 B.埋在地下的金屬管線被腐蝕僅與土壤中水分有關 C.土壤含水量在20%~40%時,金屬腐蝕的速率逐漸加快 D.可以采用刷漆、涂油等方法防止金屬管線被腐蝕 組卷:2引用:1難度:0.5 -
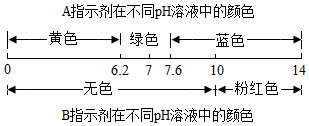 7.有A、B兩種酸堿指示劑,它們顯示的顏色與溶液pH的關系如圖,它們在甲溶液和乙溶液中顯示的顏色如表,下列判斷錯誤的是( )
7.有A、B兩種酸堿指示劑,它們顯示的顏色與溶液pH的關系如圖,它們在甲溶液和乙溶液中顯示的顏色如表,下列判斷錯誤的是( )溶液
指示劑甲 乙 A 黃色 藍色 B 無色 粉紅色 A.甲溶液呈酸性 B.乙溶液的pH可能為11 C.只用A指示劑就可鑒別甲溶液、乙溶液和蒸餾水三種液體 D.在滴有A指示劑的甲溶液中不斷地加入乙溶液,最后溶液一定呈綠色 組卷:72引用:6難度:0.5 -
8.如圖是燃料使用的發展歷程(括號內表示主要成分),下列有關說法錯誤的是( )
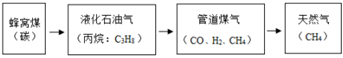
A.主要成分中除C、H2外均為有機物 B.液化石油氣不充分燃燒時會有一氧化碳生成 C.取天然氣進行化學實驗前要先檢驗其純度 D.等質量甲烷比等質量丙烷完全燃燒后CO2排放量低 組卷:13引用:1難度:0.5 -
9.下列有關氫氧化鈉性質探究實驗的敘述中,錯誤的是( )

A.甲向接近沸騰的水中加入一定量NaOH固體,液體迅速沸騰 B.乙將少量頭發加入到熱的濃NaOH溶液中,頭發逐漸溶解消失 C.丙向久置空氣里的氫氧化鈉溶液中滴加無色酚酞試液,檢驗其是否變質 D.丁向盛滿CO2氣體的集氣瓶中加入適量濃燒堿溶液,雞蛋被“吞”入瓶中 組卷:4引用:1難度:0.5 -
10.除去下列物質中含有的少量雜質,所用試劑或方法正確的是( )
選項 混合物(括號內為雜質) 除雜試劑或方法 A NaCl溶液(MgCl2) 過量NaOH溶液 B KNO3溶液(K2SO4) 適量Ba(NO3)2溶液 C Na2SO4溶液(Na2CO3) 適量稀鹽酸 D CO2氣體(CO) 點燃 A.A B.B C.C D.D 組卷:7引用:1難度:0.5 -
11.有關專家提出了“以廢治廢”的治理污染新思路,并且起到了一定的成效如冶煉鋼鐵時,為減少煤中硫燃燒生成的二氧化硫所造成的污染,一般是在煤燃燒時添加生石灰或石灰石進行固硫主要是利用氧化鈣與二氧化硫反應生成亞硫酸鈣根據這一原理,有人將造紙廠回收的堿白泥主要成分:和摻進煤中進行固硫用堿白泥固硫時,下列所寫的化學反應可能發生的是( )
①S+O2SO2點燃
②CaCO3CaO+CO2↑高溫
③CaCO3+2NaOH═Na2CO3+Ca(OH)2
④SO2+CaOCaSO3高溫
⑤SO2+2NaOH═Na2SO3+H2OA.①②③ B.②③④ C.③④⑤ D.①②④⑤ 組卷:3引用:1難度:0.5
四、解答題(本大題共6小題,第28、29題各8分,第30、32題各11分,第31題7分,第33題10分,共計55分)
-
32.墨魚骨能治療胃酸過多等多種疾病,其主要成分為碳酸鈣(雜質可溶于水),為了測定墨魚骨中碳酸鈣的質量分數,某科學興趣小組用如圖裝置進行實驗:
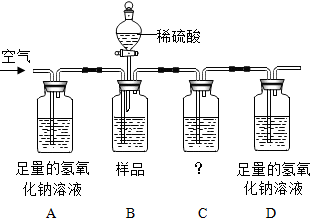
(1)小朱采用如圖所示實驗裝置,通過測定D瓶質量變化來研究。
①裝置C用于干燥氣體,C中所盛的試劑可以是。
②反應結束后未鼓入一定量的空氣,對測量結果有什么影響?并說明理由。
(2)小科也采用如圖所示實驗裝置,通過測定B瓶質量變化來研究。他用相同溶質質量分數的稀鹽酸和該樣品反應(所得溶液均為不飽和溶液),三組實驗數據記錄如下表,請分析計算在第三次實驗中m的值,(寫出計算過程,反應方程式為:CaCO3+2HCl=CaCl2+H2O+CO2↑)實驗組別 一 二 三 稀鹽酸質量/g 100.0 100.0 100.0 樣品質量/g 3.0 6.0 9.0 所得溶液質量/g 101.9 103.8 105.0 剩余固體質量/g 0 0 m 組卷:5引用:1難度:0.5 -
33.人類的生產和生活都離不開鐵及其礦石。科學興趣小組的同學開展了如下學習研究。
(1)如圖中礦石的主要成分屬于氧化物的是(填下列所給選項)。
(2)用如圖裝置來探究煉鐵的化學反應原理,已知由一氧化碳發生裝置得到的CO中混有雜質CO2和H2O,A裝置的作用是。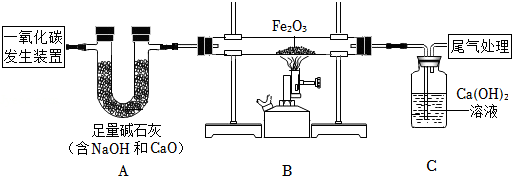
(3)從環保角度考慮,請寫出一種尾氣處理方法:。
(4)稱取10g赤鐵礦粉末(雜質不與酸反應),置于硬質玻璃管中并充分加熱一段時間,熄滅酒精噴燈后繼續通入CO至硬質玻璃管冷卻,把反應后的固體進行酸洗、干燥,稱量剩余固體雜質的質量為1.2g。計算該興趣小組的同學冶煉得到鐵的質量。組卷:1引用:1難度:0.5


