2021年安徽省江南十校高考化學摸底試卷
發布:2024/4/20 14:35:0
一、選擇題:本題共14小題,每小題3分,共12分。在每小題給出的四個選項中,只有一項是符合題目要求的。
-
1.新修訂的《城市生活垃圾管理條例》已經正式實施,垃圾分類并回收利用可以減少污染,節約自然資源。下列垃圾投放有錯誤的是( )
A. 
廢電池B. 
玻璃C. 
菜葉,果皮等D. 
煙頭,盆景的殘枝落葉等組卷:11引用:2難度:0.7 -
2.2019年底突發的新冠病毒肺炎威脅著人們的身體健康。下列有關說法正確的是( )
A.口罩中間的熔噴布具有核心作用,其主要原料為聚丙烯,屬于合成有機高分子材料 B.新型冠狀病毒僅由C、H、O三種元素組成 C.“84”消毒液是以NaClO為主要有效成分的消毒液,為了提升消毒效果,可以與潔廁靈(主要成分為鹽酸)混合使用 D.過氧化氫、乙醇、過氧乙酸等消毒液的消毒原理均是將病毒氧化而達到消毒的目的 組卷:18引用:1難度:0.7 -
3.用NA代表阿伏加德羅常數的值。下列敘述正確的是( )
A.39g鉀與氧氣完全反應,生成K2O轉移NA個電子,生成KO2轉移2NA電子 B.電解精煉銅時,當電路中轉移NA個電子,陽極溶解32g銅 C.常溫常壓下,Na2O2與H2O反應生成1mol O2時,轉移電子數是2NA D.在反應KIO3+6HI═KI+3I2+3H2O中,每生成3mol I2轉移的電子數為6NA 組卷:57引用:2難度:0.9 -
4.下列除雜試劑及方法不合理的是( )
選項 物質(雜質) 所加試劑 操作方法 A CH2═CH2(SO2) 酸性KMnO4溶液 洗氣 B 乙酸乙酯(乙酸) 飽和Na2CO3 分液 C 乙醇(水) 生石灰 蒸餾 D 溴苯(Br2) NaOH溶液 分液 A.A B.B C.C D.D 組卷:39引用:1難度:0.5 -
5.下列離子反應方程式書寫正確的是( )
A.Fe2O3溶于氫碘酸溶液中:Fe2O3+6H+═2Fe3++3H2O B.向FeBr2溶液中通入足量氯氣:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- C.Ca(HCO3)2溶液與過量NaOH溶液反應:HCO3-+Ca2++OH-═CaCO3↓+H2O D.SO2通入酸性KMnO4溶液:5SO2+2H2O+2MnO4-═5SO42-+2Mn2++4H+ 組卷:132引用:2難度:0.6 -
6.“類推”的思維方式在化學學習與研究中經常采用.下列類推思維中正確的是( )
A.NaOH飽和溶液導電能力強,則Ca(OH)2飽和溶液導電能力也強 B.CaC2能水解:CaC2+2H2O→Ca(OH)2+HC≡CH,則Mg2C3也能水解Mg2C3+4H2O→2Mg(OH)2+CH3-C≡CH C.加熱時Cu與O2反應生成CuO,則加熱時Cu與S反應生成CuS D.BaCl2溶液中通入SO2無沉淀產生,則Ba(NO3)2溶液中通入SO2也無沉淀產生 組卷:32引用:4難度:0.7
(二)選考題:共15分。請考生任選一題作答。如果多做,則按所做的第一題計分【選修3:物質結構與性質】(共1小題,滿分15分)
-
18.第四周期的過渡元素Cr、Fe、Cu及其化合物在工業上有著重要的用途。
(1)基態Fe2+的核處電子排布式為[Ar],有個未成對電子。
(2)已知:3K4Fe(CN)612KCN+Fe3C+3C+(CN)2↑+2N2↑。△
K4Fe(CN)6中含有的化學鍵類型有。
A.非極性共價鍵
B.離子鍵
C.配位鍵
D.氫鍵
E.極性共價鍵
KCN中三種元素的電負性由大到小為,(CN)2分子中σ鍵與π鍵的數目比n(σ):n(π)=。
(3)二茂鐵Fe(C5H5)2一種金屬有機配合物,是燃料油的添加劑,用以提高燃燒的效率和去煙。C5H5-是平面結構,其中碳的雜化類型為。
(4)在過氧化氫中加入乙醚后,再加入數滴K2Cr2O7的硫酸溶液,輕輕振蕩后靜置,乙醚層呈藍色,這是由于生成的過氧化鉻(CrO5)溶于乙醚的緣故。已知CrO5中的鉻只表現+6價,氧為-1價或-2價,請預測CrO5的結構。
(5)一種銅的氯化物晶胞結構如圖所示。
該化合物的化學式為,Cu配位數為。已知P、Q、R的原子坐標分別(0,0,0)、(1,1,1)、(,14,14),若Cu原子與最近的Cl原子的核間距為apm,則該晶體的密度計算表達式為14。(用含a、NA的代數式表示,其中NA表示阿伏加德羅常數的值)組卷:12引用:1難度:0.5
【選修5:有機化學基礎】(共1小題,滿分0分)
-
19.A(C3H6)是基本有機化工原料。由A制備聚合物C和
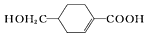 的合成路線(部分反應條件略去)如圖所示。
的合成路線(部分反應條件略去)如圖所示。
已知: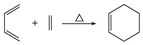 ;R-C≡NR-COOH。i.NaOHii.HCl
;R-C≡NR-COOH。i.NaOHii.HCl
回答下列問題:
(1)A的名稱是,B含有的官能團的名稱是。(寫名稱)
(2)C的結構簡式為,D→E的反應類型為。
(3)E→F的化學方程式為。
(4)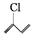 中最多有 個原子共平面。
中最多有 個原子共平面。
(5)B的同分異構體中,與B具有相同的官能團且能發生銀鏡反應的共有種;其中核磁共振氫譜為3組峰,且峰面積之比為6:1:1的是。(寫結構簡式)
(6)我國自主研發對二甲苯的綠色合成路線取得新進展,其合成示意圖如圖。結合題給信息,下列說法正確的是。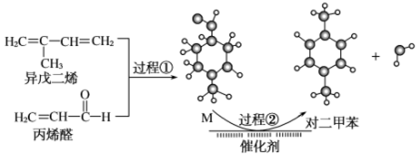
A.過程①發生了取代反應
B.中間產物M的結構簡式為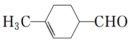
C.利用相同原理以及相同原料,也能合成鄰二甲苯和間二甲苯
D.該合成路線原子利用率為100%,最終得到的產物易分離組卷:26引用:1難度:0.3


