2021-2022學年甘肅省蘭州一中高二(下)期中化學試卷
發布:2024/12/28 13:30:3
一、單選題(每題2分,共50分)
-
1.下列說法錯誤的是( )
A.水汽化和水分解的變化過程中,都需要破壞氫鍵 B.干冰容易升華,是由于干冰中的共價鍵強度較弱 C.NaOH和K2SO4的化學鍵類型和晶體類型相同 D.區分晶體和非晶體最科學的方法是X-射線衍射法 組卷:3引用:1難度:0.8 -
 2.關于如圖敘述錯誤的是( )
2.關于如圖敘述錯誤的是( )A.該種堆積方式為最密堆積 B.該種堆積方式可用符號“???ABCABC???”表示 C.該種堆積方式為簡單立方堆積 D.金屬Cu屬于此種最密堆積模式 組卷:55引用:1難度:0.6 -
3.下列各組物質中,按熔點由高到低的順序排列正確的是( )
A.CH4>SiH4>GeH4 B.CsCl>KCl>NaCl C.Na>Mg>Al D.金剛石>碳化硅>晶體硅 組卷:19引用:4難度:0.7 -
4.下列物質所屬晶體類型分類正確的是( )
A B C D 共價晶體 石墨 生石灰 碳化硅 金剛石 分子晶體 冰 固態氨 氯化銫 干冰 離子晶體 氮化硼 食鹽 明礬 石膏 金屬晶體 銅 汞 鋁 鐵 A.A B.B C.C D.D 組卷:37引用:2難度:0.7 -
5.下列說法錯誤的是( )
A.CH≡CCH(CH3)CH=CHCH3分子中含1個手性碳原子 B.硫單質難溶于水,微溶于酒精,易溶于CS2,說明極性:水>酒精>CS2 C.  的沸點高于
的沸點高于 的沸點
的沸點D.H3PO4酸性強于H3BO3,是因為H3PO4中非羥基氧原子數大于H3BO3中非羥基氧原子數 組卷:18引用:1難度:0.7 -
6.如圖是第三周期11~17號元素某些性質變化趨勢的柱形圖,下列有關說法中正確的是( )
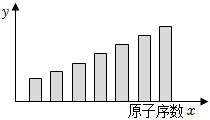
A.y軸表示的可能是第一電離能 B.y軸表示的可能是電負性 C.y軸表示的可能是原子半徑 D.y軸表示的可能是形成基態離子轉移的電子數 組卷:260引用:20難度:0.9 -
7.下列說法正確的是( )
A.在任何情況下,都是σ鍵比π鍵強度大 B.KSCN是檢驗鐵離子的常用指示劑,[Fe(SCN)6]3-離子中σ鍵與π鍵數目之比為 3:2 C.非金屬的電負性一定大于1.8,金屬的電負性一定小于1.8 D.由極性鍵構成的非極性分子往往是高度對稱的分子,如BF3、PCl5、H2O2、CO2 組卷:4引用:1難度:0.7 -
8.幾種單質的沸點如圖所示,下列推斷正確的是( )
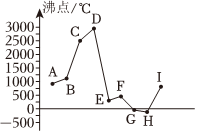
A.D可能為原子晶體,H可能為分子晶體 B.G可能為離子晶體 C.F一定是金屬晶體 D.B一定是離子晶體 組卷:22引用:1難度:0.8 -
9.下列說法正確的有( )項
①晶體中只要有陽離子就一定有陰離子
②晶胞是晶體中最小的平行六面體
③單質分子一定是非極性分子
④離子晶體都是化合物
⑤分子晶體中都存在共價鍵
⑥硫酸氫鉀在熔融狀態下離子鍵、共價鍵均被破壞A.0項 B.1項 C.2項 D.3項 組卷:14引用:1難度:0.6
二、第II卷(非選擇題,共50分)
-
28.錫、鉻、鈷、銅等金屬及其化合物在工業上有重要用途。
(1)錫合金具有優異的抗蝕性能,可以用來生產制作各種精美合金飾品。
①基態Sn原子價層電子排布為。
②Co元素在元素周期表中的位置是。
③Cu元素位于元素周期表的區。
(2)制備CrO2Cl2的反應為K2Cr2O7+3CCl4=2KCl+2CrO2Cl2+3COCl2↑。
①上述方程式中非金屬元素電負性由小到大的順序為(用元素符號表示)。
②COCl2分子中π鍵和σ鍵的個數比為,中心原子的雜化方式為,COCl2屬于分子(填“極性”或“非極性”)。
(3)Cu-Mn-Al合金為磁性形狀記憶合金材料之一,其晶胞結構如圖所示:
①合金的化學式為。
②A原子坐標參數為(0,1,0),則B原子坐標參數為。
③已知該合金晶體密度為ρg?cm-3,則兩個Al原子間的最近距離為nm(阿伏加德羅常數用NA表示,只列計算式)。組卷:5引用:1難度:0.6 -
 29.氮元素可形成很多重要的化合物,如疊氮化鈉(NaN3)和Cu3N。
29.氮元素可形成很多重要的化合物,如疊氮化鈉(NaN3)和Cu3N。
(1)NaNH2與N2O按物質的量2:1反應可生成NaN3、NaOH和一種氣體,請寫出對應的化學反應方程式:。
(2)的等電子體有NH-2(寫兩種分子),比較鍵角大小:NH-2(填“>”或“<”或“=”),請解釋原因N-3。
(3)分解NaN3可制備N2,下列說法正確的是(填符號)
A.常溫下氮氣很穩定,是因為氮的電負性大
B.NaN3的晶格能大于與KN3
C.第一電離能:N>P>S
D.NH3的穩定性強于PH3,是因為NH3分子間有氫鍵
(4)Cu3N的晶胞結構如圖所示,N3-的配位數為,若Cu+和N3-的最近核間距為(a+b)pm,則Cu3N的晶胞密度為g?cm-3(伏加德羅常數用NA表示,只列計算式)。組卷:8引用:1難度:0.6


