魯科版(2019)選擇性必修1《1.1 化學反應的熱效應》2020年同步練習卷(7)
發布:2024/4/20 14:35:0
一、選擇題:本題共10小題,每題2分,共20分.每小題只有一個選項符合題意.
-
1.下列分別是利用不同能源發電的實例圖形,其中不屬于新能源開發利用的是( )
A. 
風力發電B. 
太陽能發電C. 
火力發電D. 
潮汐能發電組卷:126引用:29難度:0.9 -
2.氫氣是人類未來最理想的燃料,以水為原料大量制取氫氣的最理想的途徑是( )
A.利用太陽能直接使水分解產生氫氣 B.以焦炭和水制取水煤氣(含CO和H2)后分離出氫氣 C.用鐵和鹽酸反應放出氫氣 D.由熱電站提供電力電解水產生氫 組卷:49引用:6難度:0.7 -
3.下列說法不正確的是( )
A.應用蓋斯定律,可計算某些難以測定的反應焓變 B.一個化學反應的焓變與反應途徑無關 C.在特定條件下反應熱可以等于焓變 D.一個反應一步完成或分幾步完成,兩者相比,經過的步驟越多,放出的熱量越多 組卷:7引用:1難度:0.8 -
4.灰錫(以粉末狀存在)和白錫是錫的兩種同素異形體.已知:
①Sn(s,白)+2HCl(aq)═SnCl2(aq)+H2(g)△H1
②Sn(s,灰)+2HCl(aq)═SnCl2(aq)+H2(g)△H2
③Sn(s,灰)Sn(s,白)△H3=+2.1kJ?mol-1,>13.2℃<13.2℃
下列說法正確的是( )A.△H1>△H2 B.錫在常溫下以灰錫狀態存在 C.灰錫轉為白錫的反應是放熱反應 D.錫制器皿長期處在低于13.2℃的環境中,會自行毀壞 組卷:226引用:55難度:0.7 -
5.已知反應:H2(g)+
O2(g)=H2O(g)△H112N2(g)+O2(g)=NO2(g)△H212N2(g)+12H2(g)=NH3(g)△H332
則反應2NH3(g)+O2(g)=2NO2(g)+3H2O(g)的△H為( )72A.2△H1+2△H2-2△H3 B.△H1+△H2-△H3 C.3△H1+2△H2+2△H3 D.3△H1+2△H2-2△H3 組卷:1164引用:27難度:0.9 -
6.已知熱化學方程式:
①C2H2(g)+O2(g)═2CO2(g)+H2O(1)△H1=-1301.0kJ?mol-152
②C(s)+O2(g)═CO2(g)△H2=-393.5kJ?mol-1
③H2(g)+O2(g)═H2O(1)△H3=-285.8kJ?mol-112
則反應④2C(s)+H2(g)═C2H2(g)的△H為( )A.+228.2 kJ?mol-1 B.-228.2 kJ?mol-1 C.+1301.0 kJ?mol-1 D.+621.7 kJ?mol-1 組卷:153引用:10難度:0.6
三、非選擇題:本題共5小題,共60分
-
19.城市使用的燃料,現大多為煤氣、液化石油氣.煤氣的主要成分是一氧化碳和氫氣的混合氣,它由煤炭與水(蒸氣)反應制得,故又稱水煤氣.
(1)試寫出制取水煤氣的主要化學反應方程式.
(2)液化石油氣的主要成分是丙烷,丙烷燃燒的熱化學方程式為:C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=-2220.0kJ?mol-1已知CO氣體燃燒的熱化學方程式為CO(g)+O2(g)═CO2(g)△H=-282.57kJ?mol-1試比較同物質的量的C3H8和CO燃燒,產生的熱量比值約為12.
(3)已知氫氣燃燒的熱化學方程式為2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ?mol-1試比較同物質的量的氫氣和丙烷燃燒,產生的熱量比值約為.
(4)氫氣是未來的能源,除產生的熱量多之外,還具有的優點是.組卷:77引用:7難度:0.5 -
 20.斷開1mol AB(g)分子中的化學鍵使其分別生成氣態A原子和氣態B原子所吸收的能量稱為A-B鍵的鍵能.下表列出了一些化學鍵的鍵能E:
20.斷開1mol AB(g)分子中的化學鍵使其分別生成氣態A原子和氣態B原子所吸收的能量稱為A-B鍵的鍵能.下表列出了一些化學鍵的鍵能E:
請回答下列問題:化學鍵 H-H Cl-Cl O═O C-Cl C-H O-H H-Cl E/kJ?mol-1 436 247 x 330 413 463 431
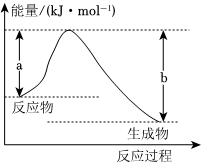
(1)如圖表示某反應的能量變化關系,則此反應為(填“吸熱”或“放熱”)反應,其中△H=(用含有a、b的關系式表示).
(2)若圖示中表示反應H2(g)+O2(g)═H2O(g)△H=-241.8kJ?mol-1,則b=12kJ?mol-1,
x=.
(3)歷史上曾用“地康法”制氯氣,這一方法是用CuCl2作催化劑,在450℃利用空氣中的氧氣跟氯化氫反應制氯氣.反應的化學方程式為.
若忽略溫度和壓強對反應熱的影響,根據上題中的有關數據,計算當反應中有1mol電子轉移時,反應的能量變化為.組卷:281引用:11難度:0.1


