2022-2023學年天津市咸水沽一中高三(上)模擬化學試卷(一)
發布:2024/12/10 7:0:1
一、選擇題(共12小題,每小題3分,滿分36分)
-
1.第24屆冬奧會中所使用的材料屬于有機高分子材料的是( )
A. 
為場館提供電能的晶體硅太陽能電池B. 
輕合金材料制成的冰刀C. 
大理石冰壺D. 
聚氨酯速滑服組卷:67引用:2難度:0.9 -
2.反應NH4Cl+NaNO2═NaCl+N2↑+2H2O放熱且產生氣體,可用于冬天石油開采。下列表示反應中相關微粒的化學用語正確的是( )
A.中子數為18的氯原子: Cl1817B.N2的結構式:N═N C.Na+的結構示意圖: 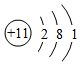
D.H2O的電子式: 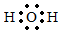 組卷:742引用:39難度:0.7
組卷:742引用:39難度:0.7 -
3.宏觀辨識與微觀探析是化學學科核心素養之一。下列物質性質實驗對應的反應方程式書寫正確的是( )
A.Na2O2放入水中:Na2O2+H2O═2NaOH+O2↑ B.H2O(g)通過灼熱鐵粉:3H2O+2Fe═Fe2O3+3H2 C.銅絲插入熱的濃硫酸中:Cu+H2SO4═CuSO4+H2↑ D.SO2通入酸性KMnO4溶液中:5SO2+2H2O+2MnO4-═5SO42-+4H++2Mn2+ 組卷:613引用:10難度:0.6 -
4.研究表明,氮氧化物和二氧化硫在形成霧霾時與大氣中的氨有關(如圖所示)。下列敘述錯誤的是( )
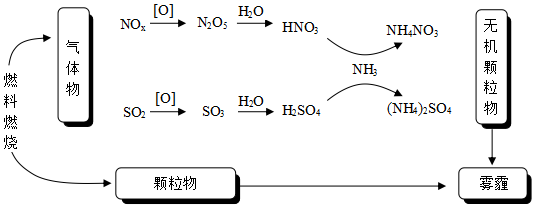
A.霧和霾的分散劑相同 B.霧霾中含有硝酸銨和硫酸銨 C.NH3是形成無機顆粒物的催化劑 D.霧霾的形成與過度施用氮肥有關 組卷:1946引用:49難度:0.9 -
5.設NA為阿伏加德羅常數值。下列有關敘述正確的是( )
A.14g乙烯和丙烯混合氣體中的氫原子數為2NA B.1molN2與4molH2反應生成的NH3分子數為2NA C.1molFe溶于過量硝酸,電子轉移數為2NA D.標準狀況下,2.24LCCl4含有的共價鍵數為0.4NA 組卷:49引用:2難度:0.8
二、解答題(共4小題,滿分64分)
-
15.化合物N具有鎮痛、消炎等藥理作用,其合成路線如圖:
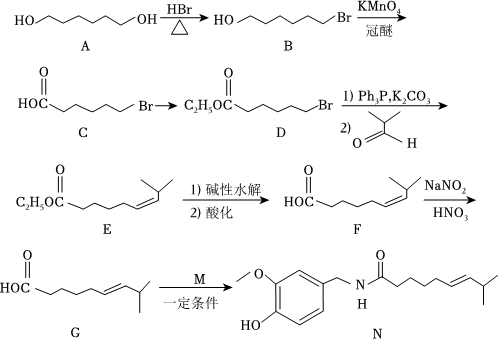
(1)A的系統命名為,E中官能團的名稱為。
(2)A→B的反應類型為,從反應所得液態有機混合物中提純B的常用方法為。
(3)C→D的化學方程式為。
(4)C的同分異構體W(不考慮手性異構)可發生銀鏡反應:且1mol W最多與2mol NaOH發生反應,產物之一可被氧化成二元醛。滿足上述條件的W有種,若W的核磁共振氫譜具有四組峰,則其結構簡式為。
(5)F與G的關系為(填序號)。
a.碳鏈異構 b.官能團異構 c.順反異構 d.位置異構
(6)M的結構簡式為。
(7)參照上述合成路線,以 為原料,采用如下方法制備醫藥中間體
為原料,采用如下方法制備醫藥中間體 。
。
該路線中試劑與條件1為,X的結構簡式為;
試劑與條件2為,Y的結構簡式為。組卷:1219引用:9難度:0.5 -
16.某興趣小組用鉻鐵礦[Fe(CrO2)2]制備K2Cr2O7晶體,流程如圖。
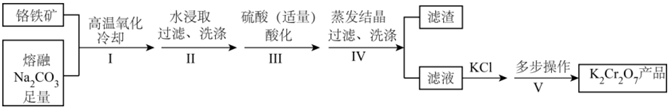
已知:4Fe (CrO2)2+10Na2CO3+7O28Na2CrO4+4NaFeO2+10CO2高溫
2H++2CrO42-?Cr2O72-+H2O
相關物質的溶解度隨溫度變化如圖。請回答: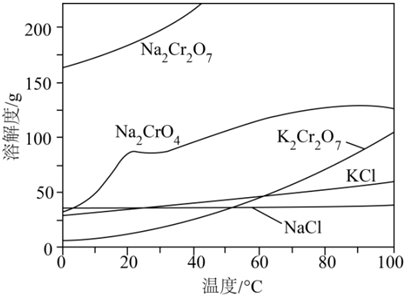
(1)步驟Ⅰ,將鉻鐵礦粉碎有利于加快高溫氧化的速率,其理由是。
(2)下列說法正確的是。
A.步驟Ⅱ,低溫可提高浸取率
B.步驟Ⅱ,過濾可除去NaFeO2水解產生的Fe(OH)3
C.步驟Ⅲ,酸化的目的主要是使Na2CrO4轉變為Na2Cr2O7
D.步驟Ⅳ,所得濾渣的主要成分是Na2SO4和Na2CO3
(3)步驟Ⅴ,重結晶前,為了得到雜質較少的K2Cr2O7粗產品,從下列選項中選出合理的操作(操作不能重復使用)并排序:溶解KCl→→→→→重結晶。
a.50℃蒸發溶劑;
b.100℃蒸發溶劑;
c.抽濾;
d.冷卻至室溫;
e.蒸發至溶液出現晶膜,停止加熱;
f.蒸發至溶液中出現大量晶體,停止加熱。
(4)為了測定K2Cr2O7產品的純度,可采用氧化還原滴定法。
①下列關于滴定分析的操作,不正確的是。
A.用量筒量取25.00mL待測液轉移至錐形瓶
B.滴定時要適當控制滴定速度
C.滴定時應一直觀察滴定管中溶液體積的變化
D.讀數時應將滴定管從架上取下,捏住管上端無刻度處,使滴定管保持垂直
E.平行滴定時,須重新裝液并調節液面至“0”刻度或“0”刻度以下
②在接近終點時,使用“半滴操作”可提高測量的準確度。其方法是:將旋塞稍稍轉動,使半滴溶液懸于管口,用錐形瓶內壁將半滴溶液沾落,繼續搖動錐形瓶,觀察顏色變化。(請在橫線上補全操作)
(5)該小組用滴定法準確測得產品中K2Cr2O7的質量分數為98.50%。某同學還用分光光度法測定產品純度(K2Cr2O7溶液的吸光度與其濃度成正比例),但測得的質量分數明顯偏低。分析其原因,發現配制K2Cr2O7待測水溶液時少加了一種試劑。該試劑是,添加該試劑的理由是。組卷:475引用:4難度:0.5


