浙教版九年級上冊《1.5 酸和堿之間發生的反應》2019年同步練習卷(浙江省金華市)
發布:2024/12/20 7:30:2
一、選擇題。
-
 1.向氫氧化鈉溶液中滴加稀鹽酸至恰好完全反應,反應前后溶液中存在的離子種類如圖所示(其中“〇”“
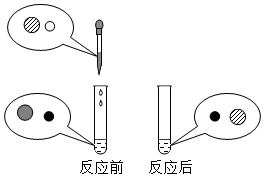
1.向氫氧化鈉溶液中滴加稀鹽酸至恰好完全反應,反應前后溶液中存在的離子種類如圖所示(其中“〇”“ ”表示不同離子)。則下列說法正確的是( )
”表示不同離子)。則下列說法正確的是( )A.〇表示氯離子 B.  表示鈉離子
表示鈉離子C.  可用適量硝酸銀溶液和足量稀硝酸進行檢測
可用適量硝酸銀溶液和足量稀硝酸進行檢測D.此反應的實質是  和〇結合生成水分子組卷:884引用:19難度:0.7
和〇結合生成水分子組卷:884引用:19難度:0.7 -
2.在氫氧化鈉溶液中加入一定量的稀鹽酸后,下列實驗能證明兩者恰好完全中和的是( )
A.滴入適量CuCl2溶液,溶液變藍,但無沉淀生成 B.滴入幾滴酚酞試液不變色 C.測得反應后溶液中Na+與Cl-的個數比為1:1 D.滴入適量硝酸銀溶液和稀硝酸,觀察到有白色沉淀 組卷:888引用:7難度:0.5 -
3.氫氧化鈉溶液與稀鹽酸發生中和反應時常觀察不到明顯現象,如圖①所示。為證明氫氧化鈉與稀鹽酸會發生反應,步驟②中加入的試劑不能是( )
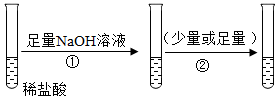
A.Zn粒 B.Na2CO3溶液 C.石蕊試液 D.AgNO3溶液 組卷:223引用:3難度:0.5
三、選擇題。
-
8.氯氣(Cl2)能與水發生如下反應:Cl2+H2O═HCl+HClO,其中HClO是一種酸。將Cl2通入氫氧化鈉溶液中,反應的生成物有( )
A.NaCl H2O B.NaClO H2O C.NaCl NaClO D.NaCl NaClO H2O 組卷:99引用:8難度:0.9
四、解答題.
-
9.海洋是一個巨大的寶庫,從海水中得到的食鹽不僅可作調料,還可作化工原料。氯堿工業就是以電解食鹽水為基礎的,化學方程式為:2NaCl+2H2O
Cl2↑+H2↑+2NaOH.某科學興趣小組模擬氯堿工業,將一定濃度的氯化鈉溶液通電一段時間(只發生上述反應),收集到0.02克H2.停止通電,向所得溶液中加入10克鹽酸后,溶液恰好為中性。求:通電
(1)電解過程中消耗氯化鈉的質量。
(2)所加鹽酸中溶質的質量分數(用化學方程式計算)。組卷:346引用:6難度:0.5


