2016-2017學(xué)年河北省保定市定州中學(xué)高二(上)開(kāi)學(xué)化學(xué)試卷
發(fā)布:2024/4/20 14:35:0
一、單選題:共16題每題3分共48分
-
1.將一定量的SO2和O2充入一個(gè)容積固定的密閉容器中,在一定條件下發(fā)生反應(yīng):2SO2+O2?2SO3,下列哪個(gè)量不再變化時(shí),并不能說(shuō)明化學(xué)反應(yīng)已達(dá)到平衡狀態(tài)( )
A.混合氣體的密度 B.混合氣體的壓強(qiáng) C.混合氣體的平均摩爾質(zhì)量 D.SO2的轉(zhuǎn)化率 組卷:32引用:4難度:0.7 -
2.下列反應(yīng)是吸熱反應(yīng)的是( )
A.C+CO2 2CO高溫B.Fe+H2SO4═FeSO4+H2↑ C.2Al+Fe2O3 2Fe+Al2O3高溫D.2Na2O2+2H2O═4NaOH+O2↑ 組卷:38引用:4難度:0.9 -
3.已知某主族元素X的原子獲得一個(gè)電子成為X-離子,則該元素在周期表中所在的族為( )
①ⅦA族 ②ⅥA族 ③IA族.A.只可能是① B.只可能是③ C.可能是①或③ D.可能是①或②或③ 組卷:43引用:2難度:0.7 -
4.X、Y、Z三種元素原子的核電荷數(shù)在11-17之間.它們的最高價(jià)氧化物對(duì)應(yīng)的水化物是HXO4、H2YO4、H3ZO4.則下列判斷不正確的是( )
A.最高正價(jià):X>Y>Z B.酸性:H3ZO4>H2YO4>HXO4 C.穩(wěn)定性:HX>H2Y>ZH3 D.非金屬性:X>Y>Z 組卷:17引用:7難度:0.7 -
5.用鐵片與稀硫酸反應(yīng)制取氫氣時(shí),下列措施不能使氫氣生成速率加快的是( )
A.滴加少量CuSO4溶液 B.不用稀硫酸,改用98%的濃硫酸 C.對(duì)該反應(yīng)體系加熱 D.不用鐵片,改用鐵粉 組卷:77引用:16難度:0.9 -
6.下列各組金屬的冶煉最適合用H2或CO把它從化合物中還原出來(lái)的是( )
A.Ca、Mg B.Al、Fe C.Hg、Ag D.Fe、Cu 組卷:34引用:7難度:0.9 -
7.如圖為某有機(jī)物的結(jié)構(gòu)簡(jiǎn)式,該有機(jī)物不具有的性質(zhì)是( )
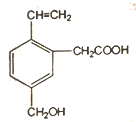
A.能使酸性KMnO4溶液褪色 B.能發(fā)生酯化反應(yīng) C.能與NaOH溶液反應(yīng) D.能發(fā)生水解反應(yīng) 組卷:30引用:4難度:0.7
二、計(jì)算題:共6題共52分
-
21.把1mol X和1mol Y混合于2L的密閉容器中,發(fā)生如下反應(yīng) 2X(g)+Y(g)=nZ(g)+2W(g),2min末X的物質(zhì)的量為0.2mol,以Z的濃度表示的反應(yīng)速率為0.1mol/(L?min)
請(qǐng)回答:
(1)前2min以X的濃度表示的平均反應(yīng)速率
(2)n值.組卷:496引用:4難度:0.5 -
22.已知:①2H2( g )+O2( g )=2H2O ( l );△H=-572kJ/mol
②2H2( g )+O2( g )=2H2O ( g );△H=-484kJ/mol
③CH4 ( g )+2O2( g )=2H2O ( l )+CO2( g );△H=-890kJ/mol
(1)已知H-H的鍵能436kJ/mol O=O的鍵能496kJ/mol H-O的鍵能463kJ/mol,根據(jù)上述數(shù)據(jù)計(jì)算①②哪一個(gè)反應(yīng)可以通過(guò)鍵能直接計(jì)算得出.并計(jì)算寫(xiě)出反應(yīng) H2O ( l )=H2O ( g )的焓變△H=.
(2)請(qǐng)根據(jù)題干計(jì)算CO2(g)+4H2( g )=CH4( g )+2H2O( g )的焓變△H=.
(3)在①②③三個(gè)方程式中哪一個(gè)是燃燒熱的熱化學(xué)方程式.(填反應(yīng)方程式的序號(hào))
標(biāo)準(zhǔn)狀況下,取甲烷和氫氣的混合氣體11.2L完全燃燒后恢復(fù)到常溫,則放出的熱量為26、3.8kJ,試求混合氣體中甲烷和氫氣體積比.組卷:81引用:4難度:0.3


