2023年湖南省長沙一中高考化學模擬試卷(八)
發布:2024/4/20 14:35:0
一、選擇題(本題共14個小題,每小題3分,共42分。每小題只有一項符合題目要求)
-
1.化學與生產、生活密切相關,下列說法不正確的是( )
A.可施加適量石膏(CaSO4?2H2O)降低鹽堿地(含較多NaCl、Na2CO3)土壤的堿性 B.二氧化氯(ClO2)、臭氧可以用于自來水消毒 C.“雷蟠電掣云滔滔,夜半載雨輸亭皋”,雷雨天可實現氮的固定 D.市售食用油中加入微量叔丁基對苯二酚作氧化劑,以確保食品安全 組卷:52引用:2難度:0.6 -
2.下列化學用語不正確的是( )
A.雙線橋表示H2S和濃H2SO4反應電子轉移的方向和數目: 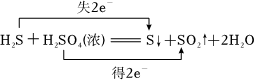
B.芒硝化學式:Na2SO4?10H2O C.用電子式表示H2O的形成過程: 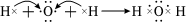
D.PH3的VSEPR模型: 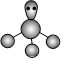 組卷:39引用:1難度:0.7
組卷:39引用:1難度:0.7 -
3.化學是實驗的科學,下列有關實驗設計能達到目的的是( )
A B C D 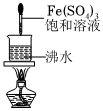
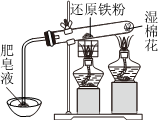
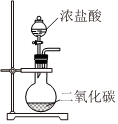
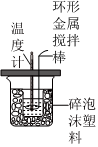
制備Fe(OH)3膠體 探究鐵與水蒸氣的反應,點燃肥皂泡檢驗氫氣 實驗室快速制取氯氣 測定中和熱 A.A B.B C.C D.D 組卷:29引用:1難度:0.7 -
4.中科院通過調控N-carbon的孔道結構和表面活性位構型,成功實現了電催化二氧化碳生成乙醇和CO,合成過程如圖所示。用NA表示阿伏加德羅常數的值,下列說法正確的是( )
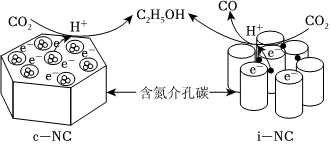
A.標準狀況下,5.6LCO2中所含π鍵的數目為0.25NA B.100g46%C2H5OH的水溶液中采取sp3雜化的原子數目為6NA C.0.1mol乙醇和0.2mol乙酸發生酯化反應,最多可生成乙酸乙酯分子數為0.1NA D.電催化過程中,若i-NC端生成1molCO,轉移電子的數目為NA 組卷:42引用:2難度:0.7 -
5.利用超分子可分離C60和C70,將C60、C70混合物加入一種空腔大小適配C60的“杯酚”中進行分離的流程如圖。下列說法正確的是( )
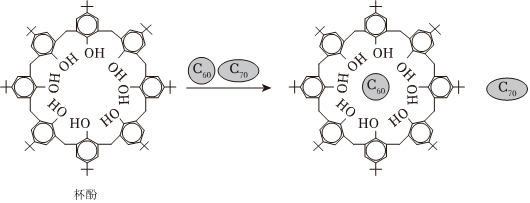
A.一個C60分子中含有90個σ鍵 B.“杯酚”與C60形成氫鍵 C.一個C60晶胞中含有8個C60分子 D.該分離過程利用的是超分子的自組裝特征 組卷:98引用:1難度:0.7 -
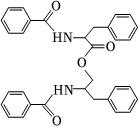 6.某種天然生物活性物質結構如圖所示,下列說法錯誤的是( )
6.某種天然生物活性物質結構如圖所示,下列說法錯誤的是( )A.分子中有兩種含氧官能團 B.苯環上的一氯代物共有6種 C.分子中有兩個手性碳原子 D.完全水解可得3種有機產物 組卷:42引用:1難度:0.7
二、非選擇題(共4個大題,58分)
-
17.化合物G是一種藥物合成中間體,其合成路線如圖所示(部分反應條件已省略):
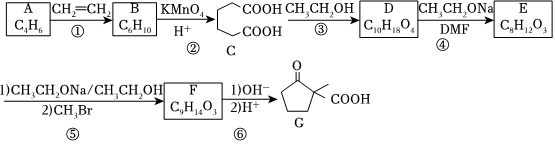
已知:①R1CH=CHR2R1COOH+R2COOH;KMnO4H+
②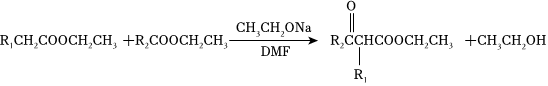
回答下列問題:
(1)A是一種烯烴,其系統命名為。
(2)B分子中共平面碳原子最多有個;第⑤步反應的反應類型為。
(3)由C生成D的化學方程式為。
(4)E的結構簡式為。
(5)同時滿足下列條件的C的同分異構體有種(不含立體異構),其中核磁共振氫譜顯示有3組峰,且峰面積之比為2:2:1的結構簡式為。
①1mol該物質能與2molNaOH反應;
②1mol該物質與銀氨溶液反應生成4molAg。
(6)參考G的合成路線,設計以乙酸乙酯和溴乙烷為原料(其他試劑任選),制備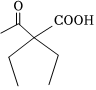 的合成路線 。組卷:36引用:1難度:0.3
的合成路線 。組卷:36引用:1難度:0.3 -
18.利用1-甲基萘(1-MN)制備四氫萘類物質(MTLs,包括1-MTL和5-MTL)。反應過程中伴有生成十氫萘(1-MD)的副反應,涉及反應如圖:
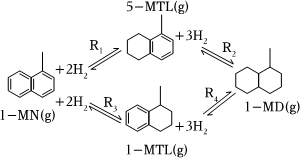
回答下列問題:
(1)1-甲基萘(1-MN)的組成元素電負性由小到大的順序為。
(2)已知一定條件下反應R1、R2、R3的焓變分別為ΔH1、ΔH2、ΔH3,則反應R4的焓變為(用含ΔH1、ΔH2、ΔH3的代數式表示)。
(3)四個平衡體系的平衡常數與溫度的關系如圖甲所示。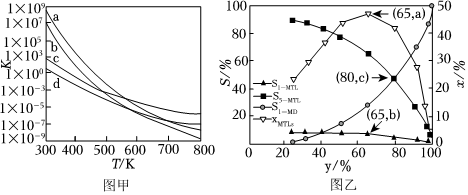
①c、d分別為反應R1和R3的平衡常數隨溫度變化的曲線,則表示反應R4的平衡常數隨溫度變化曲線為。
②已知反應R1的速率方程v正=k正?c(1-MN)?c2(H2),v逆=k逆?c(5-MTL)(k正、k逆分別為正、逆反應速率常數,只與溫度、催化劑有關)。溫度T1下反應達到平衡時k正=1.5k逆,溫度T2下反應達到平衡時k正=3k逆。由此推知,T1T2(填“>”“<”或“=”)。
③下列說法不正確的是(填標號)。
A.四個反應均為放熱反應
B.反應體系中1-MD最穩定
C.壓強越大,溫度越低越有利于生成四氫萘類物質
D.由上述信息可知,400K時反應R4速率最快
(4)1-MN在6.0×103kPa的高壓H2氛圍下反應(H2壓強近似等于總壓)。不同溫度下達平衡時各產物的選擇性Si(某生成物i的物質的量與消耗1-MN的物質的量之比)和物質的量分數xi(xi表示物種i與除H2外其他各物種總物質的量之比)隨1-MN平衡轉化率y的變化關系如圖乙所示,1-MN平衡轉化率y為80%時,1-MTL的產率=;y為65%時反應R1的平衡常數Kp=kPa-2(列出計算式)。組卷:39引用:1難度:0.4


