2006年第十六屆“天原杯”全國初中學生化學素質和實驗能力競賽(河南賽區)初賽試卷
發布:2024/11/3 6:0:1
一、選擇題(本題包括20個題,每題1分,共20分)
-
1.下列對各種材料的開發利用過程中,主要過程屬于化學變化的是( )
A.用棉、麻等植物纖維紡紗織布 B.用鈦和鈦合金制成飛機、火箭的外殼 C.用砂子、石灰石和純堿等為原料生產各種玻璃 D.用鋁箔制成各種形狀的制品 組卷:126引用:21難度:0.9 -
2.下列敘述中不正確的是( )
A.陽離子獲得電子后一定變成原子 B.僅含一種元素的物質不可能是化合物 C.由同種分子構成的物質一定是純凈物 D.空氣中既含游離態氧元素又含化合態氧元素 組卷:16引用:2難度:0.9 -
3.下列說法或做法中,你不贊成的是( )
A.某飲料純天然,絕對不含任何化學物質 B.為保護環境,充分利用資源,要將垃圾分類回收 C.為使養分還田,要鼓勵農民將植物秸稈就地粉碎還田 D.將工廠煙囪建高些,只能轉移煤煙產生的環境污染 組卷:35引用:3難度:0.9 -
4.由ag溶質的質量分數為15%的某溶液,欲使其質量分數變為30%,采用下列方法正確的是( )
A.蒸發掉溶劑的 12B.取出 的溶質12C.加入 g的溶質3a14D.加入 g的溶質3a20組卷:30引用:2難度:0.9 -
5.下列各組物質分別放入足量的水中,能夠大量共存且形成無色溶液的一組是( )
A.CuSO4 NaCl H2SO4 B.Na2CO3 KOH NaNO3 C.CaCl2 Na2CO3 AgNO3 D.BaCl2 HNO3 Na2SO4 組卷:27引用:4難度:0.7 -
6.現有Fe、NaOH溶液、MgO、CuSO4溶液、稀H2SO4五種物質,兩兩混合后,能發生的反應共有( )
A.3個 B.4個 C.5個 D.6個 組卷:18引用:2難度:0.9 -
7.野外旅行時,根據季節可以帶上“即熱飯盒”或“化學冰箱”.“化學冰箱”即把一種化學試劑放入容器中,加一定量的水,就可以形成低溫小環境,這種試劑可以是下列物質中的( )
A.濃硫酸 B.硝酸銨 C.固體氫氧化鈉 D.食鹽 組卷:56引用:5難度:0.9 -
8.高中化學把化學反應分為兩類,一類是有元素的化合價升降的化學反應是氧化還原反應;另一類是反應前后元素化合價都沒有改變的是非氧化還原反應.下列化學反應屬于非氧化還原反應的是( )
A.2KMnO4 K2MnO4+MnO2+O2↑△B.2Na+Cl2═2NaCl C.Zn+H2SO4═ZnSO4+H2↑ D.CaCO3+2HCl═CaCl2+CO2↑+H2O 組卷:40引用:2難度:0.9 -
9.氨(NH3)是一種無色、極易溶于水的氣體.在實驗室加熱氯化銨和熟石灰兩種固體的混合物可制取氨氣,則該實驗可選用的制取裝置和集氣方法正確的是( )
A.用啟普發生器制取,用排水法收集 B.用啟普發生器制取,用向下排空氣法收集 C.與加熱分解KClO3制氧氣的裝置相同,用向下排空氣法收集 D.與加熱分解KClO3制氧氣的裝置相同,用向上排空氣法收集 組卷:96引用:1難度:0.7 -
10.某有機物在氧氣中完全燃燒后生成水和二氧化碳的質量比為9:22,則該有機物可能是( )
A.C2H2 B.C2H5OH C.C6H12O6 D.CH4 組卷:20引用:3難度:0.9 -
11.錳和鎳(Ni)都是金屬元素,將鎳絲插入MnSO4溶液中無變化,插入CuSO4溶液中,鎳絲上有紅色固體析出.Mn、Ni、Cu三種金屬的活動性由強到弱的順序是( )
A.Cu、Mn、Ni B.Mn、Ni、Cu C.Ni、Cu、Mn D.Mn、Cu、Ni 組卷:31引用:15難度:0.9 -
12.長期使用的鍋爐底部會形成一層鍋垢,它是由一種難溶性的鹽和一種難溶性的堿組成的,下列可能屬于鍋垢成分的一組是
( )A.Ca(OH)2和MgCO3 B.CaSO4和Mg(OH)2 C.CaCO3和Mg(OH)2 D.CaCl2和MgCO3 組卷:57引用:5難度:0.9
四、綜合應用題(本題包括3個題,共20分)
-
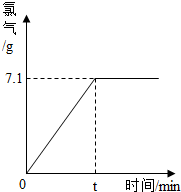 37.在化工生產中,原料往往不能全部轉化成產品.某校學生對買來的工業固體燒堿的雜質成分進行研究,他們查閱資料得知:在工業上用食鹽和水配成飽和食鹽水,通過電解(通電)制得燒堿溶液,再將溶液濃縮即可得到固體燒堿,通電過程中還可得到氫氣和氯氣(Cl2).他們推測該工業固體燒堿中可能含有碳酸鈉、氯化鈉,并設計了實驗來驗證假設.
37.在化工生產中,原料往往不能全部轉化成產品.某校學生對買來的工業固體燒堿的雜質成分進行研究,他們查閱資料得知:在工業上用食鹽和水配成飽和食鹽水,通過電解(通電)制得燒堿溶液,再將溶液濃縮即可得到固體燒堿,通電過程中還可得到氫氣和氯氣(Cl2).他們推測該工業固體燒堿中可能含有碳酸鈉、氯化鈉,并設計了實驗來驗證假設.
(1)請你幫助他們完成實驗報告:
(2)請寫出工業上用電解飽和食鹽水制燒堿的化學方程式實驗步驟 實驗現象 結 論 ①取樣,加足量的水 固體完全溶解 -- ②用試管取上述試液,加入過量稀硝酸,塞上帶導管的單孔塞;將導管的另一端插入 中有 生成
有生成證明原固體燒堿中含有碳酸鈉 ③向試管中再加入硝酸銀 有白色沉淀生成 證明原固體燒堿中含有 .
( 3 )現取100g室溫下的飽和食鹽水(此時質量分數約為26.5%)進行電解,當反應停止后,生成氯氣的質量與時間的關系如圖所示.請計算:參加反應的氯化鈉的質量是多少?反應后所得燒堿溶液的質量分數是多少?(計算結果精確到0.001)組卷:27引用:1難度:0.1 -
38.已知草酸(H2C2O4)在加熱條件下的反應為H2C2O4
CO2↑+CO↑+H2O.現用下圖甲、乙裝置(圖中a、b為活塞的開關)對生成的CO和CO2進行分離并干燥.可供選用的試劑有稀硫酸、濃硫酸和氫氧化鈉溶液.△
(1)打開活塞a,關閉活塞b,讓混合氣體通過甲、乙裝置.甲中盛放的試劑為,有關反應的化學方程式為,乙裝置所起的作用是.
(2)要分離出另一種氣體,則丙中應盛裝的試劑是,正確的操作方法是,此時甲裝置中發生反應的化學方程式為.
(3)若要測定分離出來的CO氣體的體積,請從上圖A、B、C三個裝置中選擇一個合理的量氣裝置.
(4)若本實驗所得到CO氣體的體積為1232mL(該實驗條件下CO的密度為1.25g/L),全部用來還原CuO,理論上可生成Cu的質量是多少克?組卷:20引用:1難度:0.5


