2021-2022學年遼寧省葫蘆島市普通高中高一(上)期末化學試卷
發布:2024/12/15 16:30:6
一、選擇題(本題包括15小題,每小題3分,共45分,每小題只有一個選項符合題意)
-
1.Se是人體必需微量元素,含Se食品越來越多,下列有關
Se和7834Se說法正確的是( )8034A. Se和7834Se是同一種核素8034B. Se和7834Se互為同位素8034C. Se和7834Se分別含有48和46個質子8034D. Se和7834Se都含有34個中子8034組卷:39引用:1難度:0.8 -
2.下列關于物質用途的說法不正確的是( )
A.CaO用作食品脫氧劑 B.Na2O2用作呼吸面具供氧劑 C.Ca(ClO)2用作游泳池消毒劑 D.Fe2O3用作油漆紅色顏料 組卷:49引用:4難度:0.7 -
3.下列化學用語表述不正確的是( )
A.CH4分子呈正四面體形 B.KNO3的電離方程式:KNO3═K++ NO-3C.CO2分子結構模型為: 
D.H2還原CuO反應中電子的轉移: 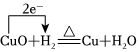 組卷:23引用:1難度:0.8
組卷:23引用:1難度:0.8 -
4.NA代表阿伏加德羅常數的值,下列說法正確的是( )
A.18gD2O中含有的中子數是9NA B.7.8gNa2O2中含有的陰離子數為0.2NA C.在Al3+濃度為0.6mol/L的硫酸鋁溶液中,SO42-的濃度為0.4mol/L D.4.6gNa與1L0.1mol/L的稀鹽酸充分反應,轉移電子數目為0.1NA 組卷:11引用:1難度:0.8 -
5.分類思想是研究化學的常用方法。下列說法正確的是( )
A.根據是否具有丁達爾效應,將分散系分為溶液、膠體和濁液 B.根據化合物的水溶液能否導電,將化合物分為電解質和非電解質 C.有單質參加或有單質生成的反應一定是氧化還原反應 D.堿性氧化物一定是金屬氧化物 組卷:204引用:7難度:0.7 -
6.下列解釋事實的方程式不正確的是( )
A.用FeCl3溶液腐蝕覆銅板:2Fe3++Cu═2Fe2++Cu2+ B.打磨過的鋁片遇NaOH溶液產生氣泡:2Al+2OH-+2H2O═2AlO2-+3H2↑ C.常溫下,新切開的鈉表面很快變暗:2Na+O2═Na2O2 D.熾熱的鐵水不能注入未經干燥的模具,是為防止:3Fe+4H2O(g) Fe3O4+4H2高溫組卷:58引用:3難度:0.7
二、非選擇題(本題包括5小題,共55分)
-
19.小組同學探究Na2CO3的性質及工業制法。
(1)用Na2CO3固體配制100mL 0.200mol?L-1Na2CO3溶液。
①用到的儀器有:天平、藥匙、量筒、燒杯、玻璃棒、膠頭滴管和。
②計算需要Na2CO3固體的質量是g。
③下列情況中,會使所配溶液濃度偏高的是。(填字母)
a.轉移時,沒有洗滌燒杯和玻璃棒
b.定容時,眼睛俯視刻度線
c.搖勻后,發現液面低于刻度線,繼續加水至液面與刻度線相切
(2)探究Na2CO3與鹽酸的反應。向0.200mol?L-1Na2CO3溶液中滴加稀鹽酸,開始無氣泡,繼續滴加,產生氣泡,反應的離子方程式為:+H+═CO2-3、HCO-3。
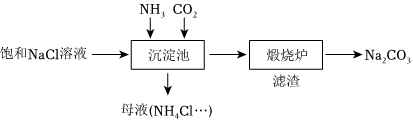
(3)我國化學家侯德榜發明的“聯合制堿法”為世界制堿工業做出了巨大貢獻。如圖為聯合制堿法的主要過程(部分物質已略去)。
已知:
ⅰ.NH3溶于水生成堿,與酸反應生成鹽,如NH3+HNO3═NH4NO3。
ⅱ.有關物質的溶解度(20℃)
①煅燒爐中發生的是分解反應,反應的化學方程式為物質 NaCl NH4HCO3 NaHCO3 NH4Cl 溶解度/g 36.0 21.7 9.6 37.2 。
②沉淀池中發生的是復分解反應,反應的離子方程式為。組卷:95引用:4難度:0.7 -
20.物質類別和核心元素的價態是學習元素及其化合物性質的兩個重要認識視角,CaO2與Na2O2都屬于過氧化物。過氧化鈣(CaO2)是一種難溶于水、可與水緩慢反應、能溶于酸的白色固體,廣泛用于果蔬保鮮、空氣凈化、污水處理等方面。以下是一種制備過氧化鈣的實驗方法。
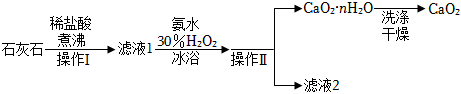
已知:CaCl2+H2O2+2NH3+nH2O═CaO2?H2O↓+2NH4Cl
回答下列問題:
(1)CaO2中氧元素化合價為。
(2)操作Ⅰ、Ⅱ為。
(3)過氧化鈣可用于長途運輸魚苗,與此用途無關的性質是。
A.能緩慢供氧
B.能潮解
C.能抑菌
(4)檢驗“洗滌”是否合格的方法是:取最后一次洗滌液少許于試管中,先滴加稀硝酸酸化,然后滴入溶液,看是否產生白色沉淀。
(5)工業的無水過氧化鈣通常含有部分CaO,實驗室常采用以酸為介質,用高錳酸鉀測定過氧化鈣的含量。稱取1.0g樣品用稀硫酸溶解,滴加0.1mol/L的酸性KMnO4溶液,恰好完全反應時,消耗酸性KMnO4溶液的體積為40.00mL,則CaO2的質量分數為。(已知5CaO2+8H2SO4+2KMnO4═5CaSO4+2MnSO4+K2SO4+5O2↑+8H2O)組卷:78引用:2難度:0.4


