人教版必修2《第3章 有機化合物》2008年單元測試卷(湖南省長沙市長郡中學)
發(fā)布:2024/4/20 14:35:0
一.選擇題(單選,每小題4分,共60分)
-
1.通常用于衡量一個國家石油化工發(fā)展水平的標志是( )
A.石油的產量 B.乙烯的產量 C.天然氣的產量 D.汽油的產量 組卷:882引用:55難度:0.9 -
2.已知乙烯能被酸性高錳酸鉀溶液氧化成CO2.既可以用來鑒別乙烷和乙烯,又可以用來除去乙烷中混有的乙烯的方法是( )
A.在空氣中燃燒 B.通入足量溴水中 C.通入酸性高錳酸鉀溶液中 D.通入水中 組卷:74引用:15難度:0.7 -
3.下列混合物能用分液法分離的是( )
A.乙醇與乙酸 B.苯和溴苯 C.乙酸乙酯和Na2CO3溶液 D.葡萄糖與果糖混合液 組卷:59引用:16難度:0.5 -
4.下列實驗能獲得成功的是( )
A.苯和濃溴水用鐵做催化劑制溴苯 B.將苯與濃硝酸混合共熱制硝基苯 C.甲烷與氯氣光照制得純凈的一氯甲烷 D.乙烯通入溴的四氯化碳溶液得到1,2-二溴乙烷 組卷:54引用:9難度:0.9 -
5.丙烯酸(CH2=CH-COOH)的性質可能有( )
①加成反應 ②取代反應 ③酯化反應 ④中和反應 ⑤氧化反應.A.只有①③ B.只有①③④ C.只有①③④⑤ D.①②③④⑤ 組卷:88引用:33難度:0.7 -
6.1mol乙烯與氯氣完全加成后再與氯氣取代,整個過程最多需氯氣( )
A.1mol B.4mol C.5mol D.6mol 組卷:890引用:22難度:0.9
二.填空
-
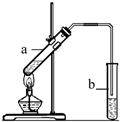 17.“酒是陳的香”,就是因為酒在儲存過程中生成了有香味的乙酸乙酯,在實驗室我們也可以用如右圖所示的裝置制取乙酸乙酯.回答下列問題:
17.“酒是陳的香”,就是因為酒在儲存過程中生成了有香味的乙酸乙酯,在實驗室我們也可以用如右圖所示的裝置制取乙酸乙酯.回答下列問題:
(1)寫出制取乙酸乙酯的化學反應方程式.
(2)濃硫酸的作用是:①;②.
(3)飽和碳酸鈉溶液的主要作用是.
(4)裝置中通蒸氣的導管要插在飽和碳酸鈉溶液的液面上,不能插入溶液中,目的是防止.
(5)若要把制得的乙酸乙酯分離出來,應采用的實驗操作是.
(6)生成乙酸乙酯的反應是可逆反應,反應物不能完全變成生成物,反應一段時間后,就達到了該反應的限度,也即達到化學平衡狀態(tài).下列描述能說明乙醇與乙酸的酯化反應已達到化學平衡狀態(tài)的有(填序號).
①單位時間里,生成1mol乙酸乙酯,同時生成1mol水
②單位時間里,生成1mol乙酸乙酯,同時生成1mol乙酸
③單位時間里,消耗1mol乙醇,同時消耗1mol乙酸
④正反應的速率與逆反應的速率相等
⑤混合物中各物質的濃度不再變化.組卷:106引用:20難度:0.3
三.計算題(10分)
-
18.為測定一種氣態(tài)烴A的化學式,取標準狀況下一定體積的A置于密閉容器中,再通入一定體積的O2,用電火花引燃,定性實驗表明產物是CO2、CO、水蒸氣.相關方案及有關數據如下(圖中的箭頭表示氣體的流向,試驗前系統(tǒng)內的空氣已排除),試回答:
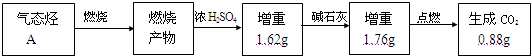
(1)通過計算求出A的實驗式(最簡式).
(2)根據所學知識,你認為氣態(tài)烴A只能是哪種物質?你的根據是什么?
(3)要確定A的化學式,除了上述理論依據,只需要再測定一個數據,即可進一步求出A的化學式,該數據可以是,若該數據用字母a表示,則該烴的分子式可表示為(用含a的式子表示).組卷:27引用:2難度:0.1


