2023-2024學年吉林省長春市農安縣高一(上)期中化學試卷
發布:2024/10/23 9:0:1
一、單選題(每小題3分,合計45分)
-
1.膠體的本質特征是( )
A.丁達爾現象 B.微粒帶電 C.吸附性 D.粒子直徑為1~100nm 組卷:119引用:3難度:0.9 -
2.下列有關焰色試驗的敘述正確的是( )
A.焰色試驗是元素的化學性質 B.可以用稀硫酸清洗用過的鉑絲 C.節日燃放的五彩繽紛的煙花,是某些金屬化合物所呈現的各種艷麗色彩 D.鈉元素的焰色必須通過藍色的鈷玻璃觀察 組卷:14引用:4難度:0.7 -
3.在酸性的無色溶液中,下列離子能大量共存的是( )
A.Cl-、Na+、Ba2+、 SO2-4B.OH-、 、Mg2+、Na+NO-3C.Al3+、Mg2+、 、Cl-SO2-4D. 、MnO-4、K+、Na+SO2-4組卷:16引用:2難度:0.5 -
4.下列實驗操作正確的是( )
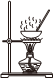
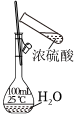
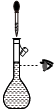
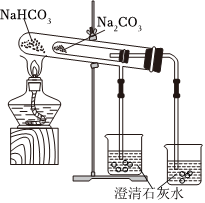
A.制備無水氯化鐵 B.配制一定物質的量濃度的硫酸溶液 C.配制一定物質的量濃度的溶液 D.比較NaHCO3和Na2CO3的熱穩定性大小 A.A B.B C.C D.D 組卷:5引用:1難度:0.7 -
5.下列儀器中,常用于過濾操作的是( )
A. 
B. 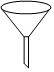
C. 
D. 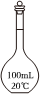 組卷:6引用:1難度:0.8
組卷:6引用:1難度:0.8 -
6.實驗室為了延長試劑的保質期,對不同試劑會采用不同的保存方式。下列試劑的保存方法錯誤的是( )
A.新制氯水應避光保存在棕色細口瓶中 B.少量鈉應保存在盛有煤油的廣口瓶中 C.氫氧化鈉固體應密封保存在細口瓶中 D.少量濃鹽酸應密封保存在細口瓶中 組卷:9引用:3難度:0.5
二、填空題(每空2分,合計44分)
-
18.(1)已知下列反應:Fe+S═FeS 2Fe+3Cl2═2FeCl3 3Fe+2O2═Fe3O4 則 S,Cl2,O2 的氧化性:
>>
(2)用雙線橋標出下列反應中電子轉移的方向和數目:
MnO2+4HCl(濃)MnCl2+Cl2↑+2H2O△
該反應中的氧化劑是,HCl體現的兩個性質是,若有4molHCL參加反應,則被氧化的HCl的物質的量是mol,如反應中轉移了0.4mol電子,則產生的Cl2在標準狀況下體積為L.組卷:60引用:3難度:0.5
三、實驗題(11分,第一空2分,其余每空3分)
-
19.用98%的濃硫酸(其密度為1.84g/cm3)配制100mL 1.0mol?L-1稀硫酸,若實驗儀器有:
A 100mL量筒 B 托盤天平 C 玻璃棒 D 50mL容量瓶E.10mL量筒 F.50mL燒杯 G.100mL容量瓶
(1)完成該實驗還缺少的儀器是。
(2)本實驗需量取濃硫酸的體積為mL。
(3)在容量瓶使用方法中,下列操作不正確的是(填字母)。
A.使用容量瓶前檢查它是否漏水
B.將氫氧化鈉固體放在天平托盤的濾紙上,準確稱量并放入燒杯中溶解后,立即注入容量瓶中
C.將準確量取的18.4mol?L-1的硫酸,注入已盛有30mL水的100mL的容量瓶中,加水至刻度線
D.定容后塞好瓶塞,用食指頂住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒轉搖勻
(4)下列情況使所配制的稀硫酸濃度偏大是(填序號)
①所用的濃硫酸長時間放置在密封不好的容器中
②容量瓶用蒸餾水洗滌后殘留有少量的水
③定容時俯視溶液的凹液面。組卷:5引用:2難度:0.6


