人教版(2019)選擇性必修2《第2章 分子結構與性質》2021年單元測試卷(1)
發布:2024/4/20 14:35:0
一、單選題(共15小題,每小題3分,滿分45分)
-
1.下列說法中正確的是( )
A.氯化氫溶于水能電離出H+、Cl-,所以氯化氫是離子化合物 B.碘晶體受熱轉變成碘蒸氣,吸收的熱量用于克服碘原子間的作用力 C.H2O分子比H2S分子穩定,是因為H2O分子間有氫鍵 D.質子數和電子數均相等的微粒,可以是不同的分子或不同的原子或不同的離子 組卷:27引用:1難度:0.5 -
2.下列關于化學鍵的說法中不正確的是( )
A.化學鍵是一種作用力 B.化學鍵可以使離子相結合,也可以使原子相結合 C.化學反應過程中,反應物分子內的化學鍵斷裂,產物分子中的化學鍵形成 D.氫鍵也是一種化學鍵 組卷:24引用:1難度:0.6 -
3.CFCl3破壞臭氧層的過程如圖所示,下列說法錯誤的是( )
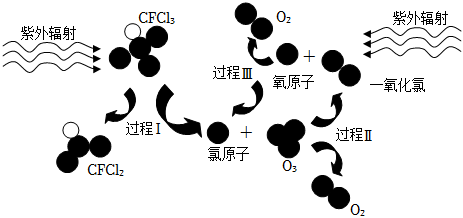
A.過程Ⅰ:斷裂C-Cl鍵 B.過程Ⅱ:O3+Cl═ClO+O2 C.過程Ⅲ:發生了O2═O+O反應 D.整個過程中氯原子是破壞臭氧層的催化劑 組卷:200引用:3難度:0.7 -
4.下列說法不正確的是( )
A.全部由非金屬元素組成的化合物中可能含有離子鍵 B.SiO2屬于原子晶體,熔化破壞共價鍵 C.HF、HCl、HBr、HI的分子間作用力依次增大 D.H2O的穩定性強于H2S,說明H-O鍵穩定性強于H-S鍵 組卷:25引用:1難度:0.5 -
5.HF分子晶體、NH3分子晶體與冰的結構極為相似,在HF分子晶體中,與F原子距離最近的HF分子個數為( )
A.3 B.4 C.5 D.12 組卷:93引用:5難度:0.7 -
6.以下說法哪些是正確的( )
A.氫鍵是化學鍵 B.甲烷可與水形成氫鍵 C.乙醇分子跟水分子之間存在范德華力和氫鍵 D.碘化氫的沸點比氯化氫的沸點高是由于碘化氫分子之間存在氫鍵 組卷:72引用:5難度:0.9 -
7.下列說法錯誤的是(設NA為阿伏加德羅常數的值)( )
A.CH4分子呈正四面體形 B.78g Na2O2晶體中陰陽離子總數為3NA C.3.4g氨氣中含有N-H鍵的數目為0.3NA D.1mol Cl2與足量的鐵粉完全反應,轉移的電子數為2NA 組卷:76引用:3難度:0.8
三、實驗題(共2小題,滿分20分)
-
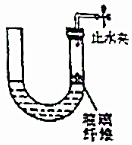 21.某課外活動小組學生模擬呼吸面具中的原理(過氧化鈉與潮濕二氧化碳反應),化學反應方程式如下:
21.某課外活動小組學生模擬呼吸面具中的原理(過氧化鈉與潮濕二氧化碳反應),化學反應方程式如下:
①2Na2O2+2CO2═2Na2CO3+O2
②2Na2O2+2H2O═4NaOH+O2↑
(1)反應①中含極性鍵的非極性分子的電子式為。反應②中含極性鍵的離子化合物的電子式為。
(2)常溫下,CO2為氣體但CS2卻為液體,請用物質結構知識說明原因。
(3)實驗中,用大理石、稀鹽酸制取所需CO2,裝置如圖。簡述檢驗氣密性的操作方法,將氣體通過Na2O2前必須除去的雜質是,該除雜劑是。
(4)確認實驗中生成O2的操作方法是。組卷:85引用:3難度:0.6 -
22.堿金屬元素和鹵族元素廣泛存在,用化學用語回答下列問題。
(1)氫氟酸可以用來雕刻玻璃。用電子式表示氟化氫的形成過程。
(2)過氧化鈉可以用于潛水艇中氧氣的來源,其與二氧化碳反應的化學方程式是。
(3)次氯酸鈉溶液(pH>7)和溴化鈉溶液混合,可以作為角膜塑形鏡的除蛋白液。二者混合后,溶液變成淡黃色,該反應的離子方程式是。
(4)Li—SOCl2電池可用于心臟起搏器。該電池的電極材料分別為鋰和碳,電解液是LiAlCl4—SOCl2.電池的總反應可表示為:4Li+2SOCl2═4LiCl+S+SO2.組裝該電池必須在無水條件下進行,原因是(用化學方程式表示)。
(5)關于堿金屬和鹵族元素,下列說法一定正確的是。
A.從上到下,單質密度依次增大
B.從上到下,單質熔沸點依次升高
C.從上到下,原子半徑依次增大
D.單質都可以與水反應
(6)常溫下,KMnO4固體和濃鹽酸反應產生氯氣。為驗證鹵素單質氧化性的相對強弱,某小組用如圖所示裝置進行實驗(夾持儀器已略去,氣密性已檢驗)。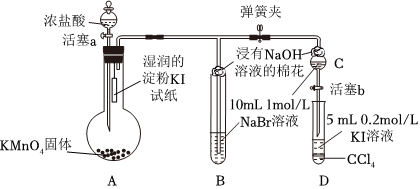
實驗過程:
Ⅰ.打開彈簧夾,打開活塞a,滴加濃鹽酸。
Ⅱ.當B和C中的溶液都變為黃色時,夾緊彈簧夾。
Ⅲ.當B中溶液由黃色變為紅棕色時,關閉活塞a。
Ⅳ.……
(1)驗證氯氣的氧化性強于碘的實驗現象是。
(2)B中溶液發生反應的離子方程式是。
(3)為驗證溴的氧化性強于碘,過程Ⅳ的操作和現象是。組卷:87引用:3難度:0.7


