2023-2024學年山東省濟南市鋼城區九年級(上)期中化學試卷
發布:2024/10/7 10:0:2
一、單項選擇題(本大題共10小題,每小題2分,共20分。每小題給出的四個選項中,只有一個選項最符合題目的要求)
-
1.下列從海洋中獲得資源的方法中,主要利用化學變化的是( )
A.海水淡化 B.海水“曬鹽” C.海帶收割 D.海水“制堿” 組卷:7引用:1難度:0.5 -
2.正確的化學實驗操作是進行探究活動的基礎和保證。下列實驗操作中合理的是( )
A.用紫色石蕊試液鑒別溶液的酸堿性時,要將試液的膠頭滴管伸入待測溶液中 B.稀釋濃硫酸時,將濃硫酸沿容器壁注入盛有水的燒杯中,并不斷攪拌 C.蒸發食鹽水時,將食鹽水全部蒸干后再停止加熱 D.聞濃鹽酸的氣味時,將鼻子盡量湊近試劑瓶口去聞 組卷:1引用:1難度:0.7 -
3.生活中一些常見食物的pH如下:
上述食物中,胃酸過多的人最不宜食用的是( )食物 檸檬汁 雞蛋清 牛奶 紅豆汁 pH 2.0-2.5 7.4-7.6 6.3-8.5 10.2-11.4 A.檸檬汁 B.雞蛋清 C.牛奶 D.紅豆汁 組卷:49引用:1難度:0.6 -
4.為了方便記憶,人們經常會給一些物質起個“俗名”。下列有關物質的化學式、名稱、俗名不完全對應的是( )
A.NaOH 氫氧化鈉 火堿 B.Ca(OH)2 氫氧化鈣 石灰水 C.CaO 氧化鈣 生石灰 D.NaCl 氯化鈉 食鹽 組卷:15引用:2難度:0.5 -
5.純堿在生產生活中有著重要的用途。根據氨堿法用氯化鈉制取純堿的反應原理如下:
(1)NaCl+NH3+CO2+H2O═NaHCO3+NH4Cl
(2)2NaHCO3═Na2CO3+CO2↑+H2O
下列對上述信息的有關理解中,不正確的是( )A.用氯化鈉制取碳酸鈉需要含碳、氧元素的物質 B.在加壓條件下向飽和氨鹽水中通入二氧化碳,能加速NaHCO3的生成 C.因為該過程生成氣體,該方法中的化學反應不遵循質量守恒定律 D.析出NaHCO3晶體后的溶液是NaHCO3的飽和溶液 組卷:49引用:1難度:0.5 -
6.形成化學觀念是化學核心素養的要求之一。下列對化學觀念的認識,不正確的是( )
A.變化觀:燒堿和純堿在一定條件下可相互轉化 B.微粒觀:氫氧化鈉溶液中含有鈉離子、氫氧根離子和水分子 C.元素觀:硫酸是由H、S、O元素組成的,在化學反應前后元素的種類不變 D.守恒觀:12g鎂和12g氧氣充分反應,生成24g氧化鎂 組卷:80引用:2難度:0.5
三、非選擇題(本大題共5小題,共60分)
-
19.某化學實驗小組欲探究稀鹽酸、澄清石灰水的化學性質,取8支試管分別用A~1H編號后,做如下實驗。
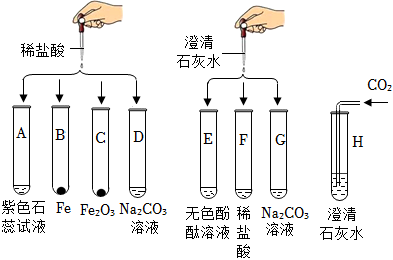
(1)實驗中觀察到有氣泡生成的試管有(填試管序號),E試管中產生的實驗現象為。
(2)某試管中發生了化學反應,但無明顯現象,該化學反應的實質為。
(3)實驗后某試管中變為紅色溶液,當向其中加入過量的NaOH溶液后,溶液變為藍色,由此推斷,該試管為(填試管序號)。
(4)實驗后某試管中為棕黃色溶液,該反應生成鹽的化學式為。
(5)實驗后某試管的底部有白色沉淀,過濾后向濾液中滴加足量鹽酸,反應一段時間后才有氣泡冒出,則該濾液中的溶質是(填化學式)。組卷:61引用:1難度:0.5 -
20.鎂元素廣泛應用于火箭、導彈和飛機制造業,被稱為“國防元素”。如圖為制取單質鎂的轉化過程,試回答下列問題:

(1)海水或鹵水中本來就含有氯化鎂,還需要過程①②的原因是(選填下列選項序號之一)。
A.生成更多氯化鎂
B.將氯化鎂富集提純
C.使石灰乳和稀鹽酸反應
(2)下列有關過程③中能量轉化的說法,正確的是(選填下列選項序號之一)。
A.電能轉化為化學能
B.化學能轉化為電能
C.潮汐能轉化為化學能
(3)在過程②中,發生反應的化學方程式為。
(4)某化學興趣小組欲測定某氯化鎂樣品中MgCl2的含量(雜質為NaCl),稱取12g該樣品置于干凈的燒杯中,加入適量水,使固體樣品完全溶解。向所得溶液中逐滴加入溶質質量分數為10%的NaOH溶液,生成沉淀的質量與滴入NaOH溶液的質量關系如圖所示。試回答下列問題:
①當滴入NaOH溶液120g時(即圖中B點),燒杯中溶液里含有的溶質離子為(填離子符號)。
②當滴入10%的NaOH溶液80g時(即圖中A點),恰好完全反應,試通過計算,求:a.12g氯化鎂樣品中MgCl2的質量分數。(寫出計算過程,計算結果精確至0.1%,下同)b.反應后所得不飽和溶液中溶質的質量。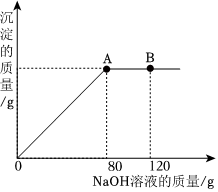 組卷:23引用:1難度:0.5
組卷:23引用:1難度:0.5


