2023-2024學年北京五中高三(上)期中化學試卷(第三次段考)
發布:2024/10/25 2:0:2
一、選擇題,共42分
-
1.我國科研人員首次以CO2為原料合成了葡萄糖和長鏈脂肪酸,這項突破為人工和半人工合成“糧食”提供了新技術。合成路線如下:
CO2CO電解①CH3COOH電解②葡萄糖、脂肪酸釀酒酵母
下列說法不正確的是( )A.過程①、②中電能轉化為化學能 B.葡萄糖分子中含有醛基、羥基 C.CH3COOH和C7H13COOH互為同系物 D.葡萄糖不能發生水解反應 組卷:222引用:7難度:0.7 -
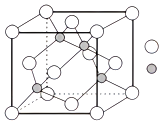 2.碳化硅晶體具有多種結構,其中一種晶體的晶胞(如圖所示)與金剛石的類似。下列判斷不正確的是( )
2.碳化硅晶體具有多種結構,其中一種晶體的晶胞(如圖所示)與金剛石的類似。下列判斷不正確的是( )A.該晶體屬于分子晶體 B.該晶體中只存在極性鍵 C.該晶體中Si的化合價為+4 D.該晶體中C的雜化類型為sp3 組卷:221引用:7難度:0.7 -
3.設NA為阿伏加德羅常數的值,下列說法正確的是( )
A.2L 0.5mol/L CH3COOH溶液中含有H+的數目為NA B.23g Na與足量H2O反應完全后生成H2的體積為11.2L C.密閉容器中2mol SO2與1mol O2充分反應,產物的分子數為2NA D.物質的量相同的 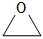 和CH3CHO所含共價鍵數目相同組卷:87引用:3難度:0.6
和CH3CHO所含共價鍵數目相同組卷:87引用:3難度:0.6 -
4.下列顏色變化與氧化還原反應無關的是( )
A.用小刀切開金屬鈉,表面逐漸變暗 B.推進裝有NO2的密閉針筒的活塞,氣體顏色變深 C.將酸性KMnO4溶液滴入H2C2O4溶液中,溶液紫色褪去 D.維生素C常與補鐵劑(有效成分中鐵元素為+2價)同服 組卷:6引用:2難度:0.8 -
5.Fe、HCN與K2CO3在一定條件下發生如下反應:Fe+6HCN+2K2CO3═K4Fe(CN)6+H2↑+2CO2↑+2H2O,下列說法正確的是( )
A.此化學方程式中涉及的第二周期元素的電負性大小的順序為O<N<C B.配合物K4Fe(CN)6的中心離子的價電子排布圖為 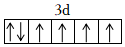 ,該中心離子的配位數是10
,該中心離子的配位數是10C.1molHCN分子中含有σ鍵的數目為1.204×1024 D.K2CO3中陰離子的空間構型為三角錐形,其中碳原子的價層電子對數為4 組卷:62引用:4難度:0.7 -
6.下列關于銅腐蝕的說法及方程式書寫正確的是( )
A.銅在潮濕空氣中被腐蝕:2Cu+O2+H2O+CO2═Cu2(OH)2CO3 B.銅在NH3環境中被腐蝕:2Cu+O2+2NH3?H2O═2Cu2++2NH3+4OH- C.HNO3濃度越大,腐蝕反應3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O速率越大 D.利用FeCl3對銅的腐蝕制作印刷線路板:3Cu+2Fe3+═2Fe+3Cu2+ 組卷:117引用:2難度:0.5
二、非選擇題、共58分
-
18.高鐵酸鉀(K2FeO4)是一種新型的污水處理劑。
(1)K2FeO4的制備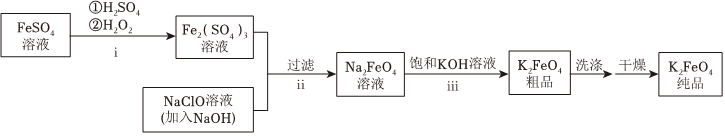
①i中反應的離子方程式是。
②將ii中反應的離子方程式補充完整:Fe3+ +OH-+ClO-═+FeO2-4+
③iii中反應說明溶解度:Na2FeO4K2FeO4(填“>”或“<”)。
(2)K2FeO4的性質
i.將K2FeO4固體溶于蒸餾水中,有少量無色氣泡產生,經檢驗為O2,液體有丁達爾效應。
ii.將K2FeO4固體溶于濃KOH溶液中,放置2小時無明顯變化。
iii.將K2FeO4固體溶于硫酸中,產生無色氣泡的速率明顯比i快。
①K2FeO4溶于蒸餾水的化學反應方程式是。
②K2FeO4的氧化性與溶液pH的關系是。
(3)K2FeO4的應用
K2FeO4可用于生活垃圾滲透液的脫氮(將含氮物質轉化為N2)處理。K2FeO4對生活垃圾滲透液的脫氮效果隨水體pH的變化結果如下: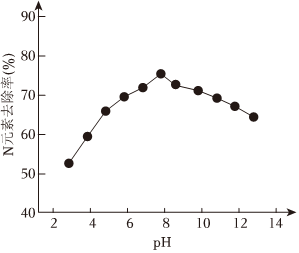
①K2FeO4脫氮的最佳pH是。
②根據圖推測,pH=4時生活垃圾滲透液中含氮物質主要以形式存在。
③pH大于8時,脫氮效果隨pH的升高而減弱,分析可能的原因:。組卷:184引用:7難度:0.5 -
19.某小組探究Fe2S3的制備。配制0.1mol?L-1的FeCl3溶液和0.1mol?L-1的Na2S溶液備用。
【查閱資料】
ⅰ.FeS、Fe2S3均為黑色固體,難溶于水。
ⅱ.Fe3++6F-?[FeF6]3-,[FeF6]3-為無色離子。
ⅲ.硫單質微溶于乙醇,難溶于水。
【設計并實施實驗】
(1)實驗一中,根據復分解反應規律推測,生成黑色沉淀a的離子方程式為編號 實驗一 實驗二 操作 

現象 迅速產生黑色沉淀a,振蕩后黑色沉淀溶解,并產生有臭雞蛋氣味的氣體,最終得到棕黃色濁液X 產生棕黑色沉淀 。
(2)進一步檢驗濁液X的組成,過程如圖。
①通過對濁液X組成的檢驗,推測實驗一的黑色沉淀a溶解過程中有氧化還原反應發生,實驗證據是。
②經檢測,黑色固體b中含有FeS。甲同學認為,FeS是由紅褐色清液中的Fe2+,與加入的S2-反應產生的。乙同學認為該推測不嚴謹,理由是。
(3)實驗二制得了Fe2S3,但其中含少量Fe(OH)3。
①生成Fe(OH)3的離子方程式為。
②從化學反應速率角度推測實驗二的棕黑色沉淀中不含S的原因:。
實驗三 小組同學進行如圖所示的改進實驗。經檢驗,黑色沉淀c為純凈的Fe2S3。
(4)實驗三中,由無色清液生成Fe2S3的離子方程式為。
【反思與評價】
(5)對比三個實驗,實驗三能成功制備Fe2S3的原因是。組卷:17引用:6難度:0.5


