2021-2022學年廣東省惠州市高一(上)期末化學試卷
發布:2024/4/20 14:35:0
一、選擇題(本題共15小題,每題1分,共15分。每題只有一個選項符合題意)
-
1.在我們的日常生活中常有“加碘食鹽”“增鐵醬油”“高鈣牛奶”“富硒茶葉”“含氟牙膏”等商品。其中碘、鐵、鈣、硒、氟指的是( )
A.元素 B.單質 C.分子 D.離子 組卷:117引用:6難度:0.8 -
2.一定條件下,當光束通過下列分散系時,能觀察到丁達爾效應的是( )
A.鹽酸 B.蔗糖溶液 C.NaCl溶液 D.Fe(OH)3膠體 組卷:6引用:2難度:0.8 -
3.下列物質所屬類別不正確的是( )
A.液態氧——純凈物 B.食鹽水——混合物 C.Na2O——氧化物 D.NaHSO4——含氧酸 組卷:18引用:1難度:0.7 -
4.下列物質中,屬于電解質的是( )
A.金屬鋁 B.乙醇 C.NaCl D.NaOH溶液 組卷:4引用:1難度:0.7 -
5.提出元素周期律并根據周期律編制第一個元素周期表的科學家是( )
A.道爾頓 B.牛頓 C.門捷列夫 D.阿伏加德羅 組卷:139引用:6難度:0.9 -
6.下列我國古代技術應用中,主反應不涉及氧化還原反應的是( )
A.古法煉鐵 B.糧食釀醋 C.煅燒石灰石 D.火藥爆炸 組卷:36引用:3難度:0.8 -
7.下列物質或原子中互稱為同位素的是( )
A.O2和O3 B.金剛石和石墨 C. H、11H和21H31D.H2O和H2O2 組卷:5引用:1難度:0.8 -
8.下列元素中,屬于惰性氣體元素的是( )
A.鈉 B.氖 C.鋁 D.硅 組卷:26引用:4難度:0.9 -
9.反應MnO2+4HCl(濃)
MnCl2+Cl2↑+2H2O中,氧化產物是( )△A.MnO2 B.HCl C.MnCl2 D.Cl2 組卷:348引用:16難度:0.8 -
10.為配制一定體積、一定物質的量濃度的氯化鈉溶液,必須用到的儀器是( )
A. 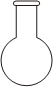
B. 
C. 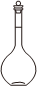
D.  組卷:83引用:2難度:0.8
組卷:83引用:2難度:0.8 -
11.下列元素中,屬于第二周期VA族的是( )
A.氮 B.氧 C.氟 D.氖 組卷:19引用:1難度:0.9 -
12.下列物質中屬于兩性氧化物的是( )
A.CO2 B.Na2O C.Na2O2 D.Al2O3 組卷:20引用:1難度:0.7 -
13.下列物質,不屬于合金的是( )
A.鋁鎂合金窗 B.青銅 C.水銀 D.合金鋼 組卷:6引用:1難度:0.6
三、非選擇題(本題共4小題,合計45分)
-
38.在一定條件下用普通鐵粉和水蒸氣反應,可以得到鐵的氧化物,該氧化物又被H2還原,生成顆粒很細的鐵粉,這種鐵粉具有很高的反應活性,在空氣中受撞擊或受熱時會燃燒,所以俗稱“引火鐵”。
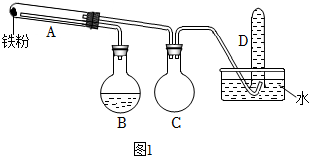
Ⅰ.利用圖1所示裝置(加熱裝置省略)制取鐵的氧化物
(1)試管A中發生反應的化學方程式是
。
(2)裝置C的作用是
。
(3)請設計實驗檢驗裝置A的產物中是否存在+3價的鐵
。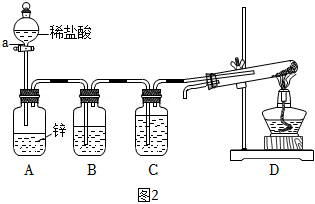
Ⅱ.利用圖2所示裝置制取“引火鐵”
(1)儀器a的名稱是
。
(2)裝置B中飽和氯化鈉溶液的作用為
;裝置C中盛放的試劑是
。
(3)為了安全,在試管中的反應發生前,在導管出口處必須
。組卷:36引用:2難度:0.6 -
39.我國化學家侯德榜發明的“聯合制堿法”為世界制堿工業做出了巨大貢獻。如圖為聯合制堿法的主要過程(部分物質已略去)。
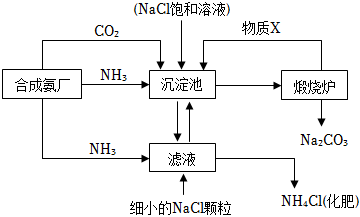
資料:ⅰ.沉淀池中的反應為NaCl+CO2+NH3+H2O═NaHCO3↓+NH4Cl
ⅱ.溶解度
(1)煅燒爐中反應的化學方程式是物質 NaCl NH4HCO3 NaHCO3 NH4Cl 20℃溶解度/g 36.0 21.7 9.6 37.2 ,物質X是(填化學式)。
(2)下列說法正確的是(填字母)。
A.沉淀池中有NaHCO3析出,因為一定條件下NaHCO3的溶解度最小
B.濾液中主要含有NaCl、Na2CO3和NH4Cl
C.設計循環的目的是提高原料的利用率
(3)工業可用純堿代替燒堿生產某些化工產品,如用飽和純堿溶液與Cl2反應可制得一種在生產生活中常用于漂白、消毒的物質,同時有NaHCO3生成,該反應的化學方程式是。
(4)某純堿樣品中含雜質NaCl,取質量為ag的樣品,加入足量的稀鹽酸,充分反應后,加熱、蒸干、灼燒,得到bg固體物質,則此樣品中Na2CO3的質量分數為。組卷:170引用:8難度:0.7


