2020-2021學年北京市朝陽外國語學校高一(上)期中化學試卷
發(fā)布:2024/4/20 14:35:0
一.單項選擇題(本部分共14小題。在每小題列出的四個選項中,選出最符合題目要求的一項)
-
1.我國酒文化源遠流長.下列古法釀酒工藝中,以發(fā)生化學反應為主的過程是( )
A. 
酒曲搗碎B. 
酒曲發(fā)酵C. 
高溫蒸餾D. 
泉水勾兌組卷:251引用:12難度:0.9 -
2.下列物質(zhì)中,屬于非電解質(zhì)的是( )
A.CO2 B.NaOH溶液 C.Al D.CaCO3 組卷:11引用:1難度:0.7 -
3.對下列實驗事故或廢棄藥品的處理方法正確的是( )
A.金屬鈉意外著火時,應用干燥的沙土蓋滅 B.當有大量氯氣泄漏時,人應沿順風方向疏散 C.當少量濃硫酸沾在皮膚上,應立即用氫氧化鈉溶液沖洗 D.不小心碰倒燃著的酒精燈,應用大量的水澆滅 組卷:6引用:1難度:0.6 -
4.除去下列物質(zhì)所含的少量雜質(zhì)(括號內(nèi)為雜質(zhì))所用試劑(均為適量)合理的是( )
A.NaClO溶液(NaOH)--Cl2 B.Cl2 (HCl)--NaOH C.Na2CO3溶液(NaHCO3)--鹽酸 D.FeCl2溶液(FeCl3)--鐵粉 組卷:4引用:1難度:0.5 -
5.下列物質(zhì)長期露置于空氣中會變質(zhì),但不是發(fā)生氧化還原反應的是( )
A.NaOH B.Na C.NaCl D.氯水 組卷:7引用:1難度:0.8 -
6.可以證明次氯酸是弱酸的事實是( )
A.可與堿發(fā)生反應 B.次氯酸鈣與硫酸反應有次氯酸生成 C.能漂白有色布條 D.0.1mol/L的次氯酸溶液中,c(H+)=10-4mol/L 組卷:13引用:1難度:0.7
二、解答題
-
18.亞氯酸鈉(NaClO2)是一種高效氧化、殺菌及漂白劑,其生產(chǎn)工藝如圖:
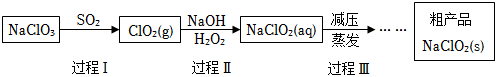
(1)NaClO2中氯元素的化合價是。從氧化還原角度推測NaClO2可能具有的化學性質(zhì)是。
(2)過程Ⅰ常伴有少量Cl2生成。
①Cl2的存在會造成產(chǎn)品中含有NaCl,請結(jié)合離子方程式解釋其原因。
②結(jié)合下面信息,請設(shè)計實驗方案除去ClO2中的Cl2。
(3)過程Ⅱ中H2O2的作用是ClO2 Cl2 在水中的溶解性 易溶 溶 在CCl4中的溶解性 難溶 溶 (填“氧化劑”或“還原劑”)。
(4)理論上每生成1 mol NaClO2,消耗SO2的體積是L(標準狀況下)。
(5)已知:
i.壓強越大,物質(zhì)的沸點越高。
ii.NaClO2飽和溶液在溫度低于38℃時析出NaClO2?3H2O 38~60℃時析出NaClO2晶體高于60℃時分解成NaClO3和NaCl。
①過程Ⅲ采用“減壓蒸發(fā)”操作的原因是。
②請將過程Ⅲ的操作補充完整。組卷:33引用:2難度:0.5 -
19.探究0.5mol/L FeCl3溶液(pH=1)與不同金屬反應時的多樣性的原因。
(各組實驗中:所用FeCl3溶液體積相同;金屬過量;靜置、不振蕩)
(1)根據(jù)實驗Ⅰ中的現(xiàn)象,推測紅褐色液體為膠體,并用光束照射該液體,在與光束垂直的方向觀察到編號 金屬 現(xiàn)象及產(chǎn)物檢驗 Ⅰ 鎂條 立即產(chǎn)生大量氣體,金屬表面變黑,該黑色固體能被磁鐵吸引,液體顏色由棕黃色逐漸變?yōu)榧t褐色;
片刻后氣泡減少,金屬表面覆蓋有紅褐色沉淀,此時取反應后的液體,滴加K3[Fe(CN)6]溶液,生成藍色沉淀。Ⅱ 銅粉 無氣體產(chǎn)生,溶液逐漸變?yōu)樗{綠色;
取反應后的溶液,滴加K3[Fe(CN)6]溶液,生成藍色沉淀。得以證實。
(2)已知:Fe和Fe3O4均能被磁鐵吸引。
①為了確定黑色固體的成分是否含有Fe與Fe3O4,重復實驗Ⅰ,及時取少量鎂條表面生成的黑色粉末,洗凈后進行實驗如下: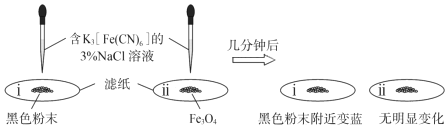
該實驗說明黑色固體中一定含有,結(jié)合現(xiàn)象寫出判斷的理由:。
②除上述結(jié)論外,分析實驗Ⅰ的現(xiàn)象,可知被還原得到的產(chǎn)物一定還有。
(3)實驗Ⅰ、Ⅱ中現(xiàn)象的差異,與Fe3+、Mg2+、Fe2+、H+、Cu2+的氧化性強弱有關(guān),其順序是Mg2+<Fe2+<。
(4)繼續(xù)探究0.5mol/L FeCl3溶液(pH=1)與Fe的反應。
①實驗Ⅲ中發(fā)生反應的離子方程式有編號 金屬 現(xiàn)象及產(chǎn)物檢驗 Ⅲ 鐵粉 持續(xù)產(chǎn)生少量氣體;一段時間后,溶液顏色變淺,底部有紅褐色沉淀,經(jīng)檢驗,溶液pH=4,含有Fe2+,無Fe3+. Ⅳ 鐵絲 無明顯的氣泡產(chǎn)生;一段時間后,溶液變?yōu)闇\綠色,經(jīng)檢驗,溶液pH=2,含有Fe2+和Fe3+;Fe3+被還原的量多于實驗Ⅲ. 。
②已知:相同條件下,H+在溶液中的移動速率遠大于Fe3+.結(jié)合實驗Ⅰ、Ⅱ,由反應中金屬表面離子濃度的變化,推測實驗Ⅲ、Ⅳ現(xiàn)象差異的原因:。組卷:69引用:3難度:0.4


