2019-2020學年寧夏育才中學高二(下)開學化學試卷
發布:2024/4/20 14:35:0
一、選擇題(本題共40小題,每題2分且各只有一項答案符合題意,共計80分)
-
1.下列分子中,既含有σ鍵又含有π鍵的是( )
A.CH4 B.HCl C.CH2═CH2 D.F2 組卷:54引用:10難度:0.9 -
2.具有下列電子排布式的原子中,半徑最小的是( )
A.1s22s22p63s23p3 B.1s22s22p3 C.1s22s22p2 D.1s22s22p63s23p4 組卷:1引用:4難度:0.9 -
3.下面的排序不正確的是( )
A.晶體熔點由低到高:CF4<CCl4<CBr4<CI4 B.硬度由大到小:金剛石>碳化硅>晶體硅 C.熔點由高到低:Na>Mg>Al D.熔點由高到低:NaF>NaCl>NaBr>NaI 組卷:138引用:8難度:0.9 -
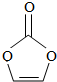 4.碳酸亞乙烯酯是鋰離子電池低溫電解液的重要添加劑,其結構如圖,下列有關該物質的說法正確的是( )
4.碳酸亞乙烯酯是鋰離子電池低溫電解液的重要添加劑,其結構如圖,下列有關該物質的說法正確的是( )A.分子式為C3H2O3 B.分子中含6個σ鍵 C.分子中只有極性鍵 D.8.6g該物質完全燃燒得到6.72LCO2 組卷:847引用:33難度:0.9 -
5.下列各組元素屬于p區的是( )
A.原子序數為1,2,7的元素 B.O,S,P C.Fe,Ar,Cl D.Na,Li,Mg 組卷:85引用:17難度:0.9 -
6.短周期元素的原子,處于基態時可能具有的電子是( )
A.只有s和p電子 B.只有s電子 C.只有p電子 D.有s、p和d電子 組卷:41引用:2難度:0.9 -
7.將盛有硫酸銅水溶液的試管中加入氨水,首先形成難溶物,繼續添加氨水難溶物溶解得到深藍色的透明溶液.下列對此現象說法正確的是( )
A.反應后溶液中不存在任何沉淀,所以反應前后Cu2+的濃度不變 B.沉淀溶解后將生成深藍色的配合離子[Cu(NH3)4]2+ C.向反應的溶液中加入乙醇溶液沒有發生變化 D.在[Cu(NH3)4]2+離子中,Cu2+給出孤對電子提供空軌道 組卷:47引用:2難度:0.7 -
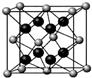 8.螢石(CaF2)晶體屬于立方晶系如圖所示,螢石中每個Ca2+被8個F-所包圍,則每個F-周圍最近距離的Ca2+數目為( )
8.螢石(CaF2)晶體屬于立方晶系如圖所示,螢石中每個Ca2+被8個F-所包圍,則每個F-周圍最近距離的Ca2+數目為( )A.2 B.4 C.6 D.8 組卷:124引用:11難度:0.7 -
9.某物質熔融狀態可導電,固態可導電,將其投入水中所形成的水溶液也可導電,則可推測該物質可能是( )
A.金屬單質 B.非金屬單質 C.可溶性堿 D.可溶性鹽 組卷:14引用:3難度:0.9 -
10.下列敘述正確的是( )
A.任何晶體中,若含有陽離子也一定含有陰離子 B.原子晶體中只含有共價鍵 C.離子晶體中只含有離子鍵 D.分子晶體中只存在分子間作用力,不含化學鍵 組卷:7引用:3難度:0.9 -
11.下列關于電子云的說法中,正確的是( )
A.電子云表示電子在原子核外運動的軌跡 B.電子云表示電子在核外單位體積的空間出現的機會多少 C.電子云界面圖中的小黑點密表示該核外空間的電子多 D.電子云可表示電子在核外運動的方向 組卷:136引用:16難度:0.9 -
12.鏷-239原子核內有148個中子.現有A元素的一種同位素,比鏷-239的原子核內少54個質子和100個中子,則A元素在周期表中的位置是( )
A.第3周期第ⅠA族 B.第4周期第ⅠA族 C.第5周期第ⅠA族 D.第3周期第ⅡA族 組卷:7引用:2難度:0.7 -
13.當鎂原子由1s22s22p63s2→1s22s22p63p2時,以下認識正確的是( )
A.鎂原子由基態轉化成激發態,這一過程中吸收能量 B.鎂原子由激發態轉化成基態,這一過程中釋放能量 C.轉化后位于p能級上的兩個電子處于同一軌道,且自旋方向相同 D.轉化后鎂原子與硅原子電子層結構相同,化學性質相似 組卷:519引用:27難度:0.7 -
14.在乙烯分子中有5個σ鍵、1個π鍵,它們分別是( )
A.碳原子sp2雜化軌道形成σ鍵、未雜化的2p軌道形成π鍵 B.碳原子sp2雜化軌道形成π鍵、未雜化的2p軌道形成σ鍵 C.C-H之間是sp2雜化軌道形成的σ鍵,C-C之間是未參加雜化的2p軌道形成的π鍵 D.C-C之間是sp2雜化軌道形成的σ鍵,C-H之間是未參加雜化的2p軌道形成的π鍵 組卷:91引用:6難度:0.7
二、填空題
-
42.如圖1是元素周期表中的前四周期,①~⑨為相應的元素,請從中選擇合適的元素回答問題:
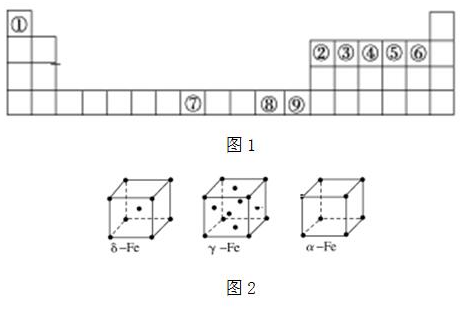
(1)根據元素原子的外圍電子排布特征,元素周期表可劃分為五個區域,元素⑦位于周期表的區。
(2)寫出元素③與元素⑤形成的穩定化合物的結構式。
(3)②、⑥兩元素形成的化合物其中心原子的雜化軌道類型為。
(4)元素⑦與CO可形成X(CO)5型化合物,該化合物常溫下呈液態,熔點為-20.5℃,沸點為103℃,易溶于非極性溶劑,據此可判斷該化合物晶體屬于晶體(填晶體類型)。
(5)元素⑨的離子的氫氧化物不溶于水,但可溶于氨水,該離子與NH3間結合的作用力為。
(6)將①、⑥形成的化合物溶于水,其與水間可能存在的氫鍵表示為(寫一種即可)。
(7)金屬⑦有δ、γ、α三種同素異形體,各晶胞如圖2,則δ和α中原子的配位數之比為。組卷:5引用:1難度:0.4 -
43.A、B、C、D、E都是短周期元素,原子序數依次增大,五種元素核電荷總數為42,B、C同周期,A、D同主族.A、B能形成兩種液態化合物甲和乙,原子個數比分別為2:1和1:1.根據以上信息回答下列問題:
(1)甲、乙兩分子中含有非極性共價鍵的物質的電子式是,C元素在周期表中的位置是.
(2)C和D的離子中,半徑較小的是(填離子符號).
(3)將D的單質投入甲中,待D消失后再向上述溶液中加入E的單質,此時發生反應的化學方程式是.
(4)C、D、E可組成離子化合物DxEC6,其晶胞(晶胞是在晶體中具有代表性的最小重復單元)結構如圖所示,陽離子D+(用〇表示)位于正方體的棱的中點和正方體內部;陰離子(用●表示)位于該正方體的頂點和面心.該化合物的化學式是ECx-6.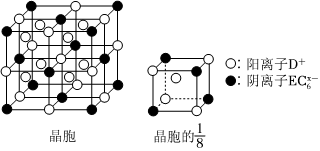 組卷:29引用:3難度:0.5
組卷:29引用:3難度:0.5


