魯科版(2019)選擇性必修1《1.2 化學能轉化為電能-電池》2020年同步練習卷(1)
發布:2024/4/20 14:35:0
-
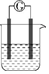 1.從稀硫酸、Fe2(SO4)3溶液、鐵棒、銅棒、鉑棒中選擇,組成下圖所示的原電池裝置(只有兩個電極),觀察到電流計的指針明顯偏轉,則其可能的組合共有( )
1.從稀硫酸、Fe2(SO4)3溶液、鐵棒、銅棒、鉑棒中選擇,組成下圖所示的原電池裝置(只有兩個電極),觀察到電流計的指針明顯偏轉,則其可能的組合共有( )A.6種 B.5種 C.4種 D.3種 組卷:19引用:1難度:0.8 -
2.下列裝置中,電流表指針不能發生偏轉的是( )
A. 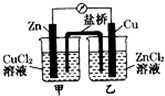
B. 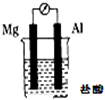
C. 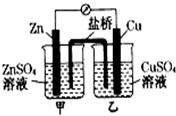
D. 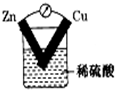 組卷:26引用:2難度:0.9
組卷:26引用:2難度:0.9 -
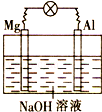 3.將鎂片、鋁片平行插入到一定濃度的NaOH溶液中,用導線連接成閉合回路,該裝置在工作時,下列敘述正確的是( )
3.將鎂片、鋁片平行插入到一定濃度的NaOH溶液中,用導線連接成閉合回路,該裝置在工作時,下列敘述正確的是( )A.鎂比鋁活潑,鎂失去電子被氧化成Mg2+ B.鋁是電池負極,開始工作時溶液中會立即有白色沉淀生成 C.該裝置的內、外電路中,均是電子的定向移動形成電流 D.該裝置開始工作時,鋁片表面的氧化膜可不必處理 組卷:75引用:6難度:0.7
-
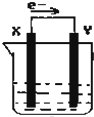 4.如圖,在盛有稀硫酸的燒杯中放入用導線連接的電極X、Y,外電路中電子流向如圖所示,下列 關于該裝置的說法正確的是( )
4.如圖,在盛有稀硫酸的燒杯中放入用導線連接的電極X、Y,外電路中電子流向如圖所示,下列 關于該裝置的說法正確的是( )A.外電路電流方向為:X→外電路→Y B.若兩極分別為鐵棒和碳棒,則X為碳棒,Y為鐵棒 C.X極上發生的是還原反應,Y極上發生的是氧化反應 D.若兩極都是金屬,則它們的活動順序為X>Y 組卷:258引用:18難度:0.9 -
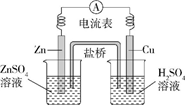 5.下列有關如圖所示原電池的說法正確的是( )
5.下列有關如圖所示原電池的說法正確的是( )A.隨著反應進行,左燒杯中Zn2+濃度上升,右燒杯中H+濃度下降 B.鹽橋的作用是讓電子通過,以構成閉合回路 C.隨著反應進行,右燒杯中溶液pH變小 D.總反應為2H++Zn═H2↑+Zn2+,且為吸熱反應 組卷:38引用:1難度:0.8
-
14.電化學氣敏傳感器可用于監測環境中NH3的含量,其工作原理如圖所示,下列說法不正確的是(

A.O2在電極b上發生還原反應 B.反應消耗的NH3與O2的物質的量之比為4:5 C.溶液中OH-向電極a移動 D.負極的電極反應式為2NH3+6OH--6e-═N2+6H2O 組卷:25引用:6難度:0.7
-
15.Ⅰ.高鐵酸鹽在能源、環保等方面有著廣泛的用途。高鐵酸鉀(K2FeO4)不僅是一種理想的水處理劑,而且在高鐵電池的研制中也有應用。如圖1是高鐵電池的模擬實驗裝置。
(1)該電池放電時正極的電極反應式為;若電池工作過程中通過電子的物質的量為0.01 mol,理論上消耗Zn的質量為g.(計算結果保留一位小數)
(2)鹽橋中含有KCl,此鹽橋中氯離子向(填“左”或“右”,下同)側燒杯移動;若用陽離子交換膜代替鹽橋,則鉀離子向側燒杯移動。
(3)圖2為高鐵電池和常用的高能堿性電池的放電曲線,由此可得出高鐵電池的優點有。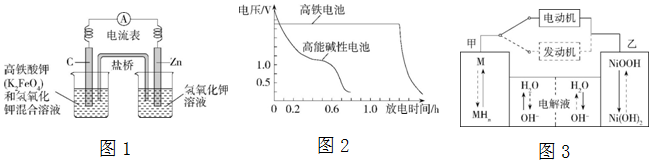
Ⅱ.第三代混合動力車,可以用電動機、內燃機或二者結合推動車輛。汽車上坡或加速時,電動機提供推動力,降低汽油的消耗;在剎車或下坡時,電池處于充電狀態。
(4)混合動力車的內燃機以汽油為燃料,在25℃、101kPa條件下,汽油[以辛烷C8H18(l)計]和氧氣充分反應,生成1mol水蒸氣放熱550kJ,若1g水蒸氣轉化為液態水放熱2.5kJ,則表示辛烷燃燒熱的熱化學方程式為。
(5)混合動力車目前一般使用鎳氫電池,該電池中鎳的化合物為正極,儲氫金屬(以M表示)為負極,堿(主要為KOH)液為電解質溶液。鎳氫電池充放電原理示意圖如圖3,其總反應式為H2+2NiOOH2Ni(OH)2.根據所給信息判斷,混合動力車上坡或加速時,乙電極周圍溶液的pH放電充電(填“增大”、“減小”或“不變”),該電極的電極反應式為。組卷:13引用:1難度:0.7


