2021-2022學年遼寧省沈陽五中高一(上)第一次月考化學試卷
發布:2024/4/20 14:35:0
一、單選題(每道選擇題只有一一個正確選項,每題3分)
-
1.中國傳統文化對人類文明貢獻巨大,很早就把化學技術應用到生產生活中。下列與化學有關的說法不正確的是( )
A.《本草綱目》中記載“(火藥)乃焰消(KNO3)、硫磺、杉木炭所合,以烽燧銃極“這是利用了“KNO3的氧化性” B.“日照香爐生紫煙“是指光照下香爐中升騰出紫色的煙,為化學變化 C.《神農本草經》中提到:“白青(Cu2(OH)2CO3)得鐵化為銅”,其中白青屬于鹽 D.《青花瓷》中“天青色等煙雨”是指在潮濕的環境下冶煉陶瓷才能出現的“天青色”是含鈷化合物的顏色 組卷:11引用:1難度:0.7 -
2.以下教材中出現的4句話錯誤的是( )
A.放電影時,放映室射到銀幕上的光柱屬于丁達爾效應 B.工業上制取NaOH一般采用電解飽和食鹽水的方法 C.金屬的冶煉、電鍍、燃料的燃燒、光合作用、易燃物的自燃、食物的腐敗、鋼鐵的銹蝕都是氧化還原 D.汽車尾氣系統中安裝的催化轉化器是為了減少尾氣中有機物的排放,減少大氣污染 組卷:15引用:1難度:0.7 -
3.某同學在實驗室進行如圖所示實驗,下列說法中不正確的是( )

A.X中的濃溶液滴入沸水中可得到Z中液體 B.X中分散系能產生丁達爾效應 C.用過濾和滲析的方法,可將Z中液體分離提純 D.Y中反應離子方程式:3CaCO3+2Fe3++3H2O=2Fe(OH)3(膠體)+3CO2↑+3Ca2+ 組卷:69引用:5難度:0.6 -
4.將下列各組物質,按單質、氧化物、酸、堿、鹽分類順序排列正確的是( )
A.銀、二氧化硫、硫酸、純堿、食鹽 B.碘酒、冰、硫酸氫鈉、燒堿、碳酸鈣 C.氫氣、干冰、硝酸、燒堿、硝酸鉀 D.銅、氧化銅、鹽酸、氨水、碳酸氫鈉 組卷:19引用:1難度:0.7 -
5.下列說法在一定條件下不能實現的是( )
A.酸性氧化物與金屬氧化物發生氧化還原反應 B.只有單質參與的氧化還原反應 C.沒有水生成,也沒有沉淀和氣體生成的復分解反應 D.有單質參加的非氧化還原反應 組卷:13引用:1難度:0.8 -
6.下列說法中不正確的有( )
①將硫酸鋇放入水中不能導電,所以硫酸鋇是非電解質;
②氨溶于水得到的溶液能導電,所以NH3是電解質;
③液態HCl不導電,所以屬于非電解質;
④NaHSO4電離時生成的陽離子有氫離子,但不屬于酸;
⑤電解質放在水中一定能導電,非電解質放在水中一定不導電;
⑥強電解質的導電能力比弱電解質強;
⑦物質可根據在水中或熔化狀態下的導電性分為電解質與非電解質。A.4個 B.5個 C.6個 D.全部 組卷:111引用:5難度:0.6
三、填空題(共55分)
-
 18.研究化學反應是為了更好的利用化學反應.回答下列問題:
18.研究化學反應是為了更好的利用化學反應.回答下列問題:
(1)在①置換反應 ②化合反應 ③分解反應 ④復分解反應 四種基本反應類型中,一定屬于氧化還原反應的是(填標號).
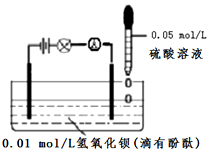
(2)探究離子反應的實驗裝置如圖.向滴有幾滴酚酞的0.01mol?L-1Ba(OH)2溶液中逐滴滴入0.05 mol?L-1H2SO4溶液,直至過量.
①Ba(OH)2的電離方程式為;開始滴加0.05 mol?L-1H2SO4時,反應的離子方程式為;
②酚酞由紅色變為無色時,觀察到的實驗現象還有.
(3)已知:a.向可溶性鹽MnSO4的酸性溶液中加入 NaBiO3溶液,溶液變成紫紅色,且有Bi3+離子生成;b.實驗室常用高錳酸鉀固體與濃鹽酸在常溫下反應制取氯氣
①寫出a中反應的離子方程式;
②KMnO4、NaBiO3、Cl2的氧化性由強到弱的順序為;
③某同學用鹽酸酸化NaBiO3溶液,你認為是否合理,你的判定及理由是.組卷:18引用:3難度:0.5 -
19.已知HNO2是一種弱酸,向NaNO2中加入強酸可生成HNO2。HNO2不穩定,易分解成NO和NO2氣體。HNO2是一種還原劑,能被常見的強氧化劑氧化;但在酸性溶液中它也是一種氧化劑,如能把Fe2+氧化成Fe3+。AgNO2是一種難溶于水、易溶于酸的白色沉淀。試回答下列問題:
(1)人體正常的血紅蛋白含有Fe2+。若誤食亞硝酸鹽如NaNO2,則導致血紅蛋白中的Fe2+轉化為Fe3+而中毒,可以服用維生素C解毒,維生素C在解毒的過程中表現出(填“氧化”或“還原”)性。“多C多漂亮”,在很多的飲料配料表中都會添加維生素C,添加維生素C的作用是。
(2)下列方法中,不能用來區分NaNO2和NaCl的是(填序號)。
A.加入鹽酸,觀察是否有氣泡產生
B.加入AgNO3溶液觀察是否有沉淀生成
C.分別在它們的酸性溶液中加入FeCl2溶液,觀察溶液顏色變化
(3)S2O32-可以與Fe2+反應制備Fe2O3納米顆粒。
①若S2O32-與Fe2+的物質的量之比為1:2,配平該反應的離子方程式:Fe2++S2O32-+H2O2+OH-═Fe2O3+S2O62-+H2O。
②下列關于該反應的說法中正確的是(填序號)。
A.該反應中S2O32-表現了氧化性
B.已知生成的Fe2O3納米顆粒直徑為10納米,則Fe2O3納米顆粒為膠體
C.該反應中H2O2作氧化劑
(4)NaNO2在酸性條件下與Fe2+發生反應后還原產物是N2,則離子方程式。組卷:48引用:1難度:0.5


