2015-2016學(xué)年江西省贛州市興國(guó)三中興國(guó)班高二(上)練習(xí)化學(xué)試卷(7.11)
發(fā)布:2024/4/20 14:35:0
一.選擇題
-
1.升高溫度能加快反應(yīng)速率的主要原因是( )
A.活化分子能量明顯增加 B.降低活化分子百分?jǐn)?shù) C.增加活化分子百分?jǐn)?shù) D.降低反應(yīng)所需要的能量 組卷:45引用:10難度:0.9 -
2.氯酸鉀晶體在①加熱,②研細(xì),③光照,④配成溶液,⑤摻入MnO2五項(xiàng)中,能使其充分釋放氧氣的速率達(dá)最快組合的是( )
A.①③④ B.①②⑤ C.③④⑤ D.②③⑤ 組卷:9引用:2難度:0.5 -
3.在10℃時(shí)某化學(xué)反應(yīng)速率為0.1mol?(L?s)-1,若溫度每升高10℃,反應(yīng)速率增加到原來(lái)的2倍.為了把該反應(yīng)速率提高到1.6mol?(L?s)-1,則該反應(yīng)需在什么溫度下進(jìn)行( )
A.30℃ B.40℃ C.50℃ D.60℃ 組卷:69引用:17難度:0.7 -
4.下列說(shuō)法正確的是( )
A.活化分子碰撞即發(fā)生化學(xué)反應(yīng) B.升高溫度會(huì)加快反應(yīng)速率,原因是增加了活化分子的碰撞次數(shù) C.某一反應(yīng)的活化分子百分?jǐn)?shù)是個(gè)定值 D.活化分子的碰撞不一定是有效碰撞 組卷:58引用:9難度:0.9 -
5.在CO(g)+H2O(g)=CO2(g)+H2(g)(放熱)的反應(yīng)中,改變下列條件,不能使v正增大的是( )
A.升高溫度 B.降低溫度 C.增大容器體積 D.使用催化劑 組卷:1引用:1難度:0.5 -
6.現(xiàn)有可逆反應(yīng)CaO(s)+CO2(g)
CaCO3(s),要使正、逆反應(yīng)速率都加快,可采取的措施是( )△A.升高溫度 B.增大壓強(qiáng) C.加入CO2 D.加入CaCO3 組卷:8引用:1難度:0.5 -
7.同質(zhì)量的鋅與鹽酸反應(yīng),欲使反應(yīng)速率增大,選用的反應(yīng)條件正確的組合是( )
①鋅粒
②鋅片
③鋅粉
④5%的鹽酸
⑤10%的鹽酸
⑥15%的鹽酸
⑦加熱
⑧用冷水冷卻
⑨不斷振蕩
⑩迅速混合后靜置.A.②⑥⑦⑩ B.①④⑧⑩ C.③⑤⑦⑨ D.③⑥⑦⑨ 組卷:53引用:9難度:0.7 -
8.A、B在溶液中進(jìn)行反應(yīng):A+B?C.現(xiàn)將A、B兩種反應(yīng)物進(jìn)行以下五個(gè)實(shí)驗(yàn),其中①~④在20℃時(shí)進(jìn)行,⑤在40℃時(shí)進(jìn)行,實(shí)驗(yàn)剛開(kāi)始時(shí),反應(yīng)速率由快到慢的順序正確的是( )
①20mL 0.2mol?L-1 A+20mL 0.2mol?L-1 B
②50mL 0.5mol?L-1 A+50ml 0.5mol?L-1 B
③10mL 1mol?L-1 A+10mL 1mol?L-1+30mL H2O
④20mL 1mol?L-1 A+60mL 0.4mol?L-1 B
⑤30mL 0.6mol?L-1 A+30ml 0.6mol?L-1 B。A.②④⑤①③ B.⑤④②③① C.④②⑤①③ D.③⑤④②① 組卷:12引用:1難度:0.6 -
9.下列實(shí)驗(yàn)中,反應(yīng)速率加快是由催化劑引起的是( )
A.在炭粉中加入KClO3,點(diǎn)燃時(shí)燃燒得更為劇烈 B.H2O2中加入少量MnO2,即可迅速放出氣體 C.把硫鐵礦粉碎后焙燒,燃燒更充分 D.電解水時(shí),在水中加少量的燒堿,產(chǎn)生氣泡速率迅速加快 組卷:16引用:1難度:0.6 -
10.下列說(shuō)法正確的是( )
A.增大壓強(qiáng),活化分子數(shù)增加,化學(xué)反應(yīng)速率一定增大 B.升高溫度,活化分子百分?jǐn)?shù)增加,化學(xué)反應(yīng)速率一定增大 C.活化分子間所發(fā)生的分子間的碰撞為有效碰撞 D.加入反應(yīng)物,使活化分子百分?jǐn)?shù)增加,化學(xué)反應(yīng)速率增大 組卷:344引用:18難度:0.7
一.選擇題
-
29.對(duì)可逆反應(yīng)4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列敘述正確的是( )
A.達(dá)到化學(xué)平衡時(shí),4υ正(O2)=5υ逆(NO) B.若單位時(shí)間內(nèi)生成x mol NO的同時(shí),消耗x mol NH3,則反應(yīng)達(dá)到平衡狀態(tài) C.達(dá)到化學(xué)平衡時(shí),若增加容器體積,則正反應(yīng)速率減少,逆反應(yīng)速率增大 D.化學(xué)反應(yīng)速率關(guān)系是:2υ正(NH3)=3υ正(H2O) 組卷:949引用:156難度:0.7
二.非選擇題
-
30.向含有H2SO4的H2O2溶液中滴加一定量的KMnO4溶液,反應(yīng)開(kāi)始時(shí),溶液中c(Mn2+)將隨時(shí)間的變化而變化.某學(xué)生在做實(shí)驗(yàn)前認(rèn)為,c(Mn2+)與時(shí)間的關(guān)系如圖①所示,做完實(shí)驗(yàn)后,得到的結(jié)果為圖②所示.請(qǐng)說(shuō)明下列問(wèn)題:
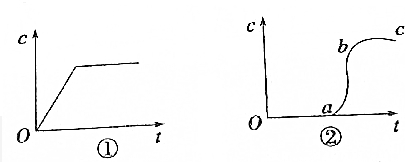
(1)寫(xiě)出H2O2與KMnO4溶液反應(yīng)的化學(xué)方程式:;
(2)Oa段的意義:;
(3)ab段的意義及ab段很陡的原因:;
(4)bc段的意義:.組卷:44引用:2難度:0.3


