2020-2021學年廣東省佛山市高二(上)期末化學試卷
發(fā)布:2024/12/26 7:30:2
一、選擇題
-
1.下列說法正確的是( )
A.氫能是二次能源 B.可以直接測量任一反應的反應熱 C.碳完全燃燒生成二氧化碳時,放出的熱量為碳的燃燒熱 D.測定中和熱時,為保證反應充分,可將NaOH溶液分批加入鹽酸中 組卷:25引用:1難度:0.6 -
2.化學與生產(chǎn)、生活關(guān)系密切,下列做法與調(diào)控化學反應速率無關(guān)的是( )
A.合成氨時使用鐵觸媒 B.用熱的純堿溶液去除油污 C.乘坐公共交通工具時需佩戴口罩 D.將聚餐打包的食物放入冰箱中 組卷:34引用:4難度:0.7 -
3.已知25℃、101kPa下,10kg丁烷完全燃燒生成CO2和液態(tài)水時,放出5×105kJ的熱量,下列熱化學方程式書寫正確的是( )
A.C4H10+ O2═4CO2+5H2O△H=-2900kJ?mol-1132B.C4H10(1)+ O2(g)═4CO2(g)+5H2O(1)△H=+2900kJ?mol-1132C.C4H10(1)+ O2(g)═4CO2(g)+5H2O(1)△H=+2900kJ132D.2C4H10(1)+13O2(g)═8CO2(g)+10H2O(1)△H=-5800kJ?mol-1 組卷:152引用:1難度:0.6 -
4.下列指定化學用語正確的是( )
A.Ba(OH)2的電離方程式:Ba(OH)2?Ba2++2OH- B.鋼鐵發(fā)生吸氧腐蝕時的正極反應:2H2O+4e-+O2═4OH- C.Na2S水解的離子方程式:S2-+2H2O?H2S+2OH- D.電解NaCl溶液的離子方程式:2Na++2Cl- 2Na+Cl2↑電解組卷:26引用:1難度:0.5 -
5.已知25℃下水的離子積Kw=1×10-14,此溫度下,下列說法錯誤的是( )
A.純水加入NaOH固體,水的電離程度減小 B.純水加入FeCl3固體,pH升高 C.0.005mol?L-1的硫酸溶液,pH=2 D.0.01mol?L-1的氫氧化鈉溶液,pH=12 組卷:55引用:1難度:0.8 -
6.常溫下,下列關(guān)于pH=3的H2C2O4溶液說法正確的是( )
A.c(H+)=c(C2O42-) B.加水稀釋時, 逐漸減小c(HC2O-4)c(H2C2O4)C.將pH=3的H2C2O4溶液稀釋10倍,溶液的pH<4 D.與0.001mol?L-1NaOH溶液按體積比1:2混合后,溶液呈堿性 組卷:37引用:1難度:0.7
二、非選擇題
-
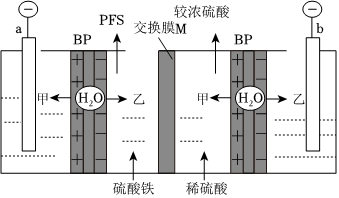 19.雙極膜(BP)是一種能將水分子解離為H+和OH-的特殊離子交換膜。應用雙極膜制取聚合硫酸鐵凈水劑[Fe2(OH)n(SO4)3-0.5n]m(PFS)的電化學裝置如圖所示。
19.雙極膜(BP)是一種能將水分子解離為H+和OH-的特殊離子交換膜。應用雙極膜制取聚合硫酸鐵凈水劑[Fe2(OH)n(SO4)3-0.5n]m(PFS)的電化學裝置如圖所示。
回答下列問題:
(1)圖中裝置為選填(“原電池”或“電解池”),a、b均為石墨電極,b極的電極反應式為。
(2)M為(填“陰離子”或“陽離子”)交換膜,圖中甲是離子。(填“H+”或“OH-”)
(3)電流密度過大,會使PFS產(chǎn)品的純度降低,可能原因是。
(4)一種含K2Cr2O7廢水的處理方法是將Cr2轉(zhuǎn)化成Cr3+或Cr(OH)3。已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.3×10-31。O2-7
①若a極區(qū)電解液改為含K2Cr2O7的廢水,可實現(xiàn)對含鉻廢水的初級處理。a極電極反應式為。
②若b極改為鐵電極,b極區(qū)電解液改為含K2Cr2O7的廢水,可實現(xiàn)對含K2Cr2O7廢水的深度處理,則b極電極反應式為。電解一段時間,b極附近產(chǎn)生沉淀的主要成分為。組卷:37引用:1難度:0.5 -
20.人體有多種常量元素和微量元素,每一種元素都有其重要的功能,其中血液中含有但不限于下列微粒:H2CO3、HCO3-、Cl-、Fe2+、Fe3+、Ca2+這些微粒處于一個平衡穩(wěn)定的狀態(tài),維持我們正常的生命活動。
(1)人體內(nèi)的含鐵化合物主要分為兩類:功能性鐵(Fe2+)和儲存鐵(Fe3+),功能性鐵和血紅蛋白一起參與氧的運輸,當人體中少量缺鐵時只需補充富含維生素C的水果即可,維生素C的作用是。
(2)正常情況下,人體血液的pH約為7.4,血液呈弱堿性的原因是(用離子方程式表示),腎臟通過分泌HCO3-調(diào)節(jié)血液pH,分泌HCO3-可使血液pH。(填“升高”或“降低”)
(3)當血液的pH=7.4[c(H+)=3.98×10-8mol?L-1]時,HCO3-和H2CO3濃度比值約為20:1,計算此狀態(tài)下H2CO3的Ka1=,查閱資料得知常溫下H2CO3的Ka1=4.5×10-7,解釋與計算所得數(shù)據(jù)存在差異的原因。
(4)血液中存在的鈣離子稱為血鈣。已知:Ksp(CaCO3)=2.8×10-9、Ksp(CaC2O4)=2.3×10-9。
①當血鈣濃度為2.5×10-3mol?L-1,c(CO32-)≥時,才有利于骨骼CaCO3(s)的形成。
②若血鈣的濃度低于2.25×10-3mol?L-1,需要補鈣。若在補鈣時食用菠菜等含有草酸的食物,血鈣不易轉(zhuǎn)化為骨骼,結(jié)合化學用語解釋原因。組卷:22引用:1難度:0.7


