2015-2016學年浙江省嘉興一中高一(下)開學化學試卷
發布:2024/4/20 14:35:0
一、選擇題(每小題只有一個正確答案)
-
1.下列說法不正確的是( )
A.現代化學元素分析測試中,可用元素分析儀確定物質中是否含有C、H、O、N、S、Cl、Br等元素,用紅外光譜儀確定物質中是否存在某些有機原子團,用原子吸收光譜確定物質中含有哪些金屬元素等 B.鈉鉀合金在常溫下是液體,可用于快中子反應堆作劑;鎂合金大量用于制造火箭、導彈和飛機的部件等 C.2015年浙江省多地遭遇霧霾天氣,有報道稱霧霾顆粒中汽車尾氣占20%以上,一致汽車尾氣中的主要污染物為NOx、CO、燃燒源超細顆粒(PM2.5)等有害物質,其中PM2.5(OM單位為百萬分之一米)顆粒大小約等于膠體粒子 D.如圖所示為四大基本反應及其關系,則反應4NH3+5O2 4NO+6H2O屬于區域3催化劑△ 組卷:3引用:1難度:0.9
組卷:3引用:1難度:0.9 -
2.下列有關化學用語表示正確的是( )
A.Ba (OH)2溶液與過量NaHCO3溶液混合離子方程式:Ba2++OH-+ ═BaCO3↓+H2OHCO-3B.Na+的結構示意圖: 
C.原子核內有10個中子的氧原子: O188D.氫氧化鐵的電離方程式:Fe(OH)3═Fe3++3OH- 組卷:5引用:1難度:0.9 -
3.在KClO3+6HCl=KCl+3Cl2↑+3H2O的反應中,被氧化的氯原子與被還原的氯原子的原子個數比是( )
A.1:6 B.1:5 C.6:1 D.5:1 組卷:330引用:20難度:0.5 -
4.下列實驗操作正確的是( )
A.可用托盤天平稱取10.20g氫氧化鈉 B.某實驗需要900mL的0.1mol/L的硫酸銅溶液,則配得該溶液需稱取22.5g膽礬晶體 C.用10mL量筒量取5.2mL硫酸,仰視時實際量得液體提及大于5.2mL D.焰色反應實驗中,連續做兩個樣品時,應將鉑絲用硫酸洗凈并灼燒到無特殊焰色 組卷:8引用:2難度:0.7 -
5.下列關于化學素養的說法中,正確的是( )
A.海水中含有豐富的碘元素,故碘被稱為“海洋元素” B.溴化銀是一種重要的感光材料,也可用于人工降雨 C.鈉在盛有氯氣的集氣瓶中燃燒,火焰呈蒼白色,產物為NaCl;鐵在盛有氯氣的集氣瓶中燃燒,火焰呈棕黃色,產物為FeCl3 D.工業煉鐵的設備是煉鐵高爐,過程中加入石灰石的作用是除脈石(SiO2)造渣 組卷:2引用:1難度:0.9 -
6.下列各組試劑在溶液中反應,當兩種試劑的量發生改變時,不能用同一離子方程式表示的是( )
A.氯化鎂、氫氧化鈉 B.硫酸鈉、氫氧化鋇 C.碳酸氫鈉、氫氧化鋇 D.氯化鋁、氨水 組卷:12引用:2難度:0.9 -
7.將足量SO2通入下列各溶液中,所含離子還能大量共存的是( )
A.K+、Na+、 、Cl-SiO2-3B.H+、 、Al3+、NH+4SO2-4C.Na+、 、CO2-3SO2-3SO2-4D.Na+、S2-、OH-、Cl- 組卷:2引用:1難度:0.7 -
8.下列除去雜質的操作方法不正確的是( )
A.鎂粉中含少量鋁粉:加足量氫氧化鈉溶液充分攪拌后過濾 B.碳酸鈉溶液中含少量碳酸氫鈉:加足量澄清石灰水 C.自來水中含少量Fe3+:蒸餾 D.硝酸鉀固體中含少量氯化鉀:配制80℃的飽和溶液,冷卻、結晶、過濾、洗滌干燥 組卷:23引用:4難度:0.7
二、填空題部分
-
25.某興趣小組為豐富課本所學的SO2性質,設計了下列系列實驗:
(1)用圖裝置制取并收集SO2以驗證其氧化性
①實驗時為控制SO2產生的快慢,應采取的措施是.
②燒杯中NaOH溶液的作用是.
③將燃著的Mg條迅速插入集滿SO2的集氣瓶中,發現Mg條繼續燃燒,則反應后生成的含硫物質可能是(填化學式).
④若將集氣瓶換成盛有Na2S溶液的廣口瓶,發現通氣一段時間后產生大量淡黃色渾濁,經測定,產物中還有一種相對分子質量為104的酸式鹽.則該反應的離子方程式為.
(2)用如圖裝置驗證H2SO3比H2CO3酸性強
⑤試劑X是,其作用是.
⑥當觀察到,即證明H2SO3比H2CO3酸性強.組卷:17引用:3難度:0.5 -
26.已知:①銅礦礦石中含有Cu2(OH)2CO3及含鐵元素的雜質;
②黃銨鐵礬的化學式為(NH4)xFey(SO4)m(OH)n,其中鐵為+3價.
某興趣小組利用該銅礦石制黃銨鐵礬的流程如下: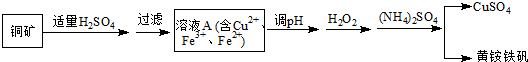
(1)以氧化物的形式表示Cu2(OH)2CO3的組成為,1mol Cu2(OH)2CO3與稀H2SO4反應時消耗H2SO4物質的量為.
(2)該小組為測定黃銨鐵礬的組成,進行了如下實驗:
a.稱取m g樣品,加鹽酸完全溶解后,將所得溶液分為兩等份;
b.向一份中加入足量NaOH溶液并加熱,收集到標況下56.00mL的氣體(假設氣體全部逸出).將所得沉淀過濾、洗滌、灼燒至恒重,得到紅色粉末0.600g.
c.向另一份中加足量BaCl2溶液充分反應后,過濾、洗滌、干燥得沉淀1.165g.
①黃銨鐵礬中NH4+與SO42-的個數比為.
②通過計算確定黃銨鐵礬的化學式(寫出計算過程).組卷:17引用:3難度:0.3


