人教新版九年級上冊《第5單元 化學方程式》2023年單元測試卷(十一)
發布:2024/8/17 4:0:1
一、選擇題
-
1.把一定質量的甲、乙、丙、丁四種物質放入一個密閉容器中,在一定條件下反應一段時間后,測得反應后各物質的質量如下表,下列說法不正確的是( )
物質 甲 乙 丙 丁 反應前質量/g 4.0 1.0 3.0 3.0 反應后質量/g x 1.0 2.4 6.2 A.x=1.4 B.甲和丙是反應物 C.丁一定是化合物 D.乙一定是該反應的催化劑 組卷:390引用:10難度:0.4 -
2.在一密閉容器內有四種物質,在一定條件下充分反應后,測得反應前后各物質的質量如下:
已知X的相對分子質量為n,Q的相對分子質量為2n.下列推理正確的是( )物質 X Y Z Q 反應前質量/g 4 10 1 21 反應后質量/g 0 12 15 待測 A.反應后生成15gZ B.反應中Y與Q發生改變的質量之比為1:1 C.反應后Q的質量為12g D.該反應方程式中X與Q的化學計量數之比為2:3 組卷:168引用:7難度:0.9 -
3.下列說法不能用質量守恒定律解釋的是( )
A.煤炭在空氣中燃燒質量減輕 B.細鐵絲在氧氣中燃燒生成物的質量比細鐵絲大 C.同溫同壓下,1L氫氣與1L氯氣在點燃的條件下完全反應生成2L氯化氫氣體 D.電解20g水得到的氫氣和氧氣的質量之和仍然是20g 組卷:20引用:2難度:0.5 -
4.下列對質量守恒定律的理解或運用,觀點合理的是( )
A.10g冰受熱融化成10g水,體現了這一變化遵循質量守恒定律 B.“2L氫氣和1L氧氣在一定條件下反應,一定會生成3L水”是由質量守恒定律決定的 C.3g碳放入裝有10g氧氣的密閉容器中,充分反應后一定生成13g二氧化碳 D.“蠟炬成灰淚始干”的描述涉及化學變化中物質質量變化的現象不違背質量守恒定律 組卷:29引用:2難度:0.9 -
5.如圖所示的四個圖象,能正確反映對應變化關系的是( )
A. 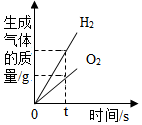
水的電解B. 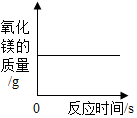
鎂條在密閉的容器內燃燒C. 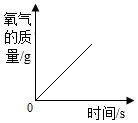
加熱一定量的氯酸鉀和二氧化錳的混合物制氧氣D. 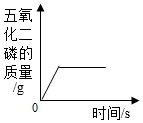
一定量的紅磷在空氣中燃燒組卷:54引用:5難度:0.5 -
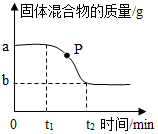 6.用氯酸鉀和二氧化錳的混合物制取氧氣,固體混合物的質量隨加熱時間的變化如圖所示。下列分析錯誤的是( )
6.用氯酸鉀和二氧化錳的混合物制取氧氣,固體混合物的質量隨加熱時間的變化如圖所示。下列分析錯誤的是( )A.反應結束時能生成(a-b)g氧氣 B.在0~t1時段,因二氧化錳未起作用,所以反應未開始 C.P點處固體的成分是氯酸鉀、二氧化錳和氯化鉀 D.在t1~t2時段,固體中氯元素的質量分數不斷增大 組卷:180引用:7難度:0.7
三、計算題
-
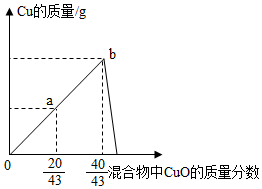 17.為探究CuO和C反應的最佳質量比(忽略副反應),化學興趣小組取 CuO和C的混合物17.2g,按不同的質量比進行實驗,實驗結果如圖所示,橫坐標表示混合物中CuO所占的質量分數,縱坐標表示生成物中Cu的質量。
17.為探究CuO和C反應的最佳質量比(忽略副反應),化學興趣小組取 CuO和C的混合物17.2g,按不同的質量比進行實驗,實驗結果如圖所示,橫坐標表示混合物中CuO所占的質量分數,縱坐標表示生成物中Cu的質量。
(1)分析可知,CuO和C的最佳質量比對應圖中的點。
(2)計算a點時,產生CO2的質量(寫出詳細計算過程)。組卷:693引用:9難度:0.6
四、科學探究題
-
 18.某興趣小組為驗證質量守恒定律,做了鎂條在空氣中燃燒的實驗,如圖1。
18.某興趣小組為驗證質量守恒定律,做了鎂條在空氣中燃燒的實驗,如圖1。
(1)小明認為根據質量守恒定律,燃燒產物的質量應大于反應物鎂條的質量。鎂條完全燃燒后,稱量發現石棉網上的燃燒產物質量反而比反應前鎂條質量小,以下解釋合理的是(填字母)。
a.氧氣不足
b.鎂條未反應完
c.部分燃燒產物散逸到空氣中
d.部分鎂條與除氧氣外的物質反應生成其他固體
(2)小紅按圖2裝置改進實驗,驗證了質量守恒定律,卻發現產物中還有一些黃色固體。
【提出問題】黃色固體是什么呢?
【查閱資料】①氧化鎂為白色固體,難溶于水且不與水反應;
②鎂能與氮氣反應生成黃色的氮化鎂(Mg3N2)固體;
③氮化鎂可與水反應,反應的化學方程式為Mg3N2+6H2O═3X+2NH3↑。X的化學式為;
④氫氧化鎂是不溶于水的固體,且受熱易分解生成氧化鎂和水。
【做出猜想】黃色固體為Mg3N2。
【實驗探究】
【反思與交流】實驗操作 實驗現象及結論 如圖,取燃燒產物于燒杯B中,加入適量水,然后用大燒杯罩住小燒杯A和B 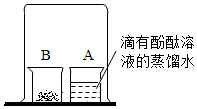
現象: ;
結論:燃燒產物含Mg3N2
(3)為什么在發生化學反應前后各物質的質量總和相等?請從微觀角度解釋:。
(4)兩位同學通過交流反思得到啟示:在探究化學反應前后物質的總質量是否發生改變時,對于有氣體參加或有氣體生成的反應一定要在裝置中進行。
【拓展延伸】
(5)如果用圖2裝置(氣密性良好)和藥品(足量)測定空氣中氧氣含量,該實驗所測得的氧氣體積分數(填“大于”“小于”或“等于”)。15
(6)2.40g鎂條在某氧氣和氮氣的混合氣體中完全燃燒,所得固體的質量可能是(填字母)。
A.3.33g
B.4.00g
C.3.28g
D.3.96g組卷:81引用:4難度:0.5


