2019-2020學(xué)年北京三中高三(上)期中化學(xué)試卷
發(fā)布:2024/4/20 14:35:0
一、每小題只有1個選項符合題意。
-
1.下列所加物質(zhì)的作用與其還原性有關(guān)的是( )
A B C D 



腌咸菜加氯化鈉 食用鹽中加碘酸鉀 紅酒中添加SO2 泡打粉加碳酸氫鈉 A.A B.B C.C D.D 組卷:29引用:3難度:0.9 -
2.下列表述合理的是( )
A.苯與乙炔的實驗式均是C2H2 B.H2O2的電子式是 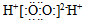
C.溴乙烷的比例模型是 
D.NH3?H2O的電離方程式是NH3?H2O═NH4++OH- 組卷:10引用:2難度:0.9 -
3.2018年國家文物局對北洋海軍軍艦“經(jīng)遠(yuǎn)艦”進(jìn)行海上考古,考古隊為艦體焊接鋅塊以實施保護(hù)。下列判斷不合理的是( )
A.焊接鋅塊后的負(fù)極反應(yīng):Fe-2e-═Fe2+ B.上述保護(hù)方法中可用鎂合金塊代替鋅塊 C.腐蝕的正極反應(yīng):2H2O+O2+4e-═4OH- D.考古隊采用的是犧牲陽極的陰極保護(hù)法 組卷:94引用:7難度:0.9 -
4.
P是一種放射性核素,可治療多種皮膚病。下列有關(guān)該核素說法正確的是( )3215A. P的摩爾質(zhì)量是323215B. P和3215P互稱為同位素3115C.1mol P含質(zhì)子數(shù)約為32×6.02×10233215D.由質(zhì)量數(shù)可以判斷其在周期表的位置 組卷:67引用:2難度:0.9 -
5.下列說法正確的是( )
A.Si、P、S、Cl原子半徑依次增大 B.HF、HCl、HBr、HI穩(wěn)定性依次減弱 C.C、N、O、F 元素的最高正化合價依次升高 D.NaOH、Mg(OH)2、Al(OH)3堿性依次增強(qiáng) 組卷:23引用:4難度:0.7 -
6.下列說法正確的是( )
A.1 mol NH3中含有的質(zhì)子數(shù)約為6.02×1023 B.0.5 mol?L-1 NaCl溶液中含Cl-的物質(zhì)的量為0.5 mol C.8 g S在足量O2中完全燃燒轉(zhuǎn)移的電子數(shù)約為9.03×1023 D.標(biāo)準(zhǔn)狀況下,22.4 L SO2和CO2的混合氣體所含原子數(shù)約為1.806×1024 組卷:45引用:5難度:0.7
二、解答題(共5小題,滿分58分)
-
18.某小組同學(xué)進(jìn)行實驗研究FeCl3溶液和Na2S溶液的反應(yīng)。
【實驗一】
已知:FeS、Fe2S3均為黑色固體,均能溶于鹽酸。H2S氣體有臭雞蛋氣味。
同學(xué)們對黑色沉淀的成分提出兩種假設(shè):
ⅰ.Fe3+與S2-反應(yīng)直接生成沉淀Fe2S3.ⅱ.Fe3+被S2-還原,生成沉淀FeS和S。
甲同學(xué)進(jìn)行如下實驗:
根據(jù)上述實驗現(xiàn)象和資料,甲得出結(jié)論:黑色沉淀是Fe2S3。操作 現(xiàn)象 取少量FeS固體,加入稀鹽酸 固體溶解,有臭雞蛋氣味氣體生成 取少量Fe2S3固體,加入稀鹽酸 固體溶解,出現(xiàn)淡黃色渾濁,有臭雞蛋氣味氣體生成
(1)0.1mol?L-1 Na2S溶液的pH為12.5.用離子方程式表示其顯堿性的原因:。
(2)乙認(rèn)為甲的結(jié)論不嚴(yán)謹(jǐn),理由是。
(3)進(jìn)一步研究證實,黑色沉淀的主要成分是Fe2S3.Na2S溶液呈堿性,F(xiàn)eCl3溶液與其反應(yīng)不生成Fe(OH)3而生成Fe2S3的可能原因是。
【實驗二】
(4)進(jìn)一步實驗證實,步驟I中局部產(chǎn)生少量的黑色沉淀是Fe2S3,黑色沉淀溶解的主要原因不是Fe2S3與溶液中Fe3+發(fā)生氧化還原反應(yīng)。步驟I中黑色沉淀溶解的反應(yīng)的離子方程式是步驟 操作 現(xiàn)象 I 
開始時,局部產(chǎn)生少量的黑色沉淀,振蕩,黑色沉淀立即消失,同時溶液中產(chǎn)生淡黃色渾濁和臭雞蛋氣味的氣體 II 繼續(xù)滴加Na2S溶液 一段時間后,產(chǎn)生大量的黑色沉淀,振蕩,沉淀不消失 。
(5)根據(jù)以上研究,F(xiàn)eCl3溶液和Na2S溶液反應(yīng)的產(chǎn)物與相關(guān)。組卷:56引用:4難度:0.7 -
19.M是合成抗生素灰黃霉素的中間產(chǎn)物,其合成路線如圖
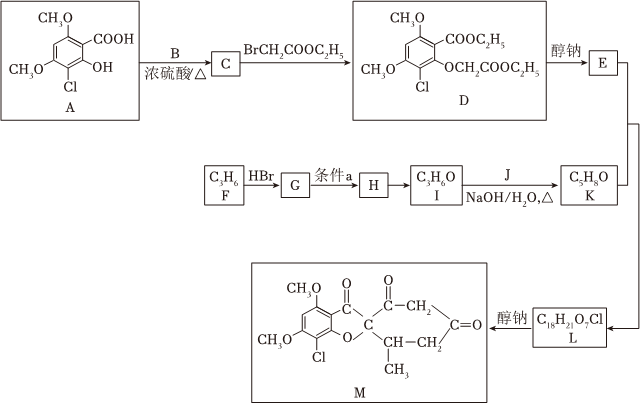
已知:
Ⅰ.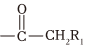 +
+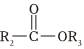 醇鈉
醇鈉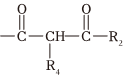 +R3OH
+R3OH
Ⅱ.R1—CHO+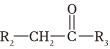 NaOH/H2O
NaOH/H2O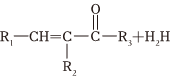 +H2O(R1、R2、R3代表烴基或氫原子)
+H2O(R1、R2、R3代表烴基或氫原子)
(1)A中含有的官能團(tuán)的名稱為醚鍵、氯原子、、。
(2)A→C反應(yīng)的化學(xué)方程式是。
(3)C→D的反應(yīng)類型是。
(4)E的結(jié)構(gòu)簡式是。
(5)I的核磁共振氫譜中只有一個吸收峰。
①條件a是。
②H→I反應(yīng)的化學(xué)方程式是。
③I→K反應(yīng)的化學(xué)方程式是。
(6)L的結(jié)構(gòu)簡式是。組卷:36引用:4難度:0.4


