2016-2017學年河北省衡水市武邑中學高三(下)開學化學試卷
發布:2024/4/20 14:35:0
一、選擇題
-
1.某有機化合物的結構簡式如圖所示,下列說法正確的是( )
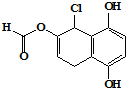
A.不能發生銀鏡反應 B.1mol 該物質最多可與2molBr2反應 C.1mol 該物質最多可與4mol NaOH反應 D.與NaHCO3、Na2CO3均能發生反應 組卷:236引用:15難度:0.9 -
2.下列化學用語正確的是( )
A.丙烯的實驗式:C3H6 B.CO2的電子式: 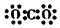
C.鎂離子的結構示意圖: 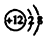
D.中子數為18 的氯原子符號:1718Cl 組卷:9引用:2難度:0.9 -
3.用NA表示阿伏加德羅常數的值,下列敘述正確的是( )
A.標準狀況下,33.6LHF中含有氟原子的數目為1.5NA B.16gO3和O2混合物中氧原子數為NA C.1mol的羥基與1mol 的氫氧根離子所含的電子數均為NA D.標準狀況下,0.1molCl2溶于水,轉移電子數為0.1NA 組卷:4引用:2難度:0.9 -
4.下列有關分類的說法正確的是( )
A.膠體的本質特征是具有丁達爾效應 B.陽離子、陰離子中均分別只含有一種元素,則由這樣的陰、陽離子組成的物質一定是純凈物 C.白磷轉化為紅磷是物理變化 D.堿性氧化物一定是金屬氧化物,酸性氧化物不一定是非金屬氧化物 組卷:64引用:8難度:0.7 -
5.8月12日天津港發生爆炸,專家對爆炸事故原因猜測認為硝化棉或者硫化鈉自燃是最可能的點火源,因此化學藥品的安全存放是非常重要的.下列有關化學藥品的存放說法不正確的是( )
A.液溴易揮發,應用水液封并放在冷暗處保存 B.金屬鈉遇到氧氣立即反應,應保存在煤油中或者液體石蠟里 C.硝酸見光易分解,應用棕色廣口試劑瓶保存 D.碳酸鈉雖然屬于鹽,但是其水溶液呈堿性,應用帶橡膠塞的試劑瓶保存 組卷:72引用:8難度:0.9 -
6.根據圖中包含的信息分析,下列敘述正確的是( )
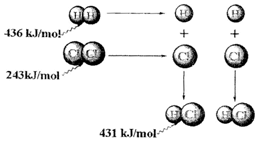
A.氫氣與氯氣反應生成1mol氯化氫氣體,反應吸收248kJ的能量 B.436kJ/mol是指斷開1molH2 中的H-H鍵需要放出436kJ的能量 C.431kJ/mol是指生成2molHCl中的H-Cl鍵需要放出431kJ的能量 D.氫氣與氯氣反應生成2mol氯化氫氣體,反應放出183kJ的能量 組卷:13引用:2難度:0.7 -
7.化學在生產和日常生活中有著重要的作用,下列有關說法不正確的是( )
A.硅酸鈉的水溶液俗稱水玻璃,可用作木材防火劑 B.采取“靜電除塵”、“燃煤固硫”、“汽車尾氣催化凈化”等方法,可提高空氣質量 C.含磷污水是很好的肥料,可灌溉莊稼,可直接排放到自然界水體中 D.高鐵酸鉀(K2FeO4)是一種新型、高效、多功能水處理劑,既能殺菌消毒又能凈水 組卷:6引用:1難度:0.7 -
8.下列離子方程式的書寫與所給條件不相符的是( )
A.將Cl2通入氫氧化鈉溶液制取消毒液:Cl2+2OH-═Cl-+ClO-+H2O B.已知亞硫酸(H2SO3)的二級電離常數K2比偏鋁酸(HAlO2)的電離常數K要大,則將少量的SO2氣體通入到偏鋁酸鈉溶液中發生的離子反應是:2AlO2-+SO2+3 H2O═2 Al(OH)3↓+SO32- C.在明礬溶液中加入氫氧化鋇溶液至沉淀的質量達到最大時發生的離子反應是:2Al3++3SO42-+3Ba2++6OH-═3BaSO4↓+2 Al(OH)3↓ D.利用酸性高錳酸鉀測居室中甲醛含量反應為:4MnO4-+5HCHO+12H+═4Mn2++5CO2↑+11H2O 組卷:8引用:1難度:0.7 -
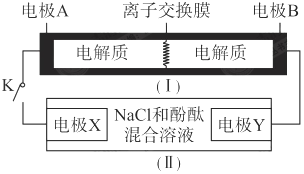 9.如圖裝置(I)為一種可充電電池的示意圖,其中的離子交換膜只允許K+通過,該電池放電、充
9.如圖裝置(I)為一種可充電電池的示意圖,其中的離子交換膜只允許K+通過,該電池放電、充
電的化學方程式為2K2S2+KI3K2S4+3KI.裝置(II)為電解池的示意圖。當閉合開關K時,電極X附近溶液先變紅。則閉合K時,下列說法正確的是( )放電充電A.當有0.1 mol K+通過離子交換膜,X電極上產生1.12 L氣體(標準狀況) B.電極A上發生的反應為:3I--2e-=I3- C.電極X上發生的反應為:2Cl--2e-=Cl2↑ D.K+從右到左通過離子交換膜 組卷:6引用:2難度:0.6
二、綜合題
-
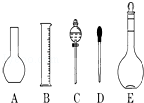 26.實驗室需要0.1mol/L NaOH溶液450mL和0.5mol/L硫酸溶液450mL.根據這兩種溶液的配制情況回答下列問題:
26.實驗室需要0.1mol/L NaOH溶液450mL和0.5mol/L硫酸溶液450mL.根據這兩種溶液的配制情況回答下列問題:
(1)如圖所示的儀器中配制溶液肯定不需要的是(填序號),儀器C的名稱是,本實驗所需玻璃儀器E規格和名稱是.
(2)下列操作中,容量瓶所不具備的功能有(填序號).
A.配制一定體積準確濃度的標準溶液 B.長期貯存溶液
C.用來加熱溶解固體溶質 D.量取一定體積的液體
(3)在配制NaOH溶液實驗中,其他操作均正確.若定容時仰視刻度線,則所配制溶液濃度0.1mol/L(填“大于”“等于”或“小于”,下同).若NaOH溶液未冷卻即轉移至容量瓶定容,則所配制溶液濃度0.1mol/L.
(4)根據計算得知,所需質量分數為98%、密度為1.84g/cm3的濃硫酸的體積為mL(計算結果保留一位小數).如果實驗室有10mL、25mL、50mL量筒,應選用mL規格的量筒最好.
(5)如果定容時不小心超過刻度線,應如何操作.組卷:79引用:9難度:0.5 -
27.某工廠對制革工業污泥中Cr元素的回收與再利用工藝如圖(硫酸浸取液中金屬離子主要是 Cr3+,其次是Fe3+、Fe2+、Al3+、Cu2+、Mg2+)
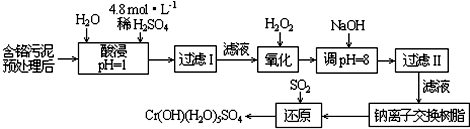
常溫下部分陽離子以氫氧化物形式沉淀時溶液的pH見表:
(1)酸浸時,為了提高浸取率可采取的措施是陽離子 Fe3+ Fe2+ Mg2+ Al3+ Cu2+ Cr3+ 開始沉淀時的pH 1.9 7.0 - _ 4.7 - 沉淀完全時的pH 3.2 9.0 11.1 8 6.7 9(>9溶解) (寫一條即可)。
(2)調pH=8是為了除去(填Fe3+、Al3+、Cu2+、Mg2+)。
(3)試配平氧化還原反應方程式:Na2Cr2O7+SO2+H2O═Cr(OH)(H2O)5SO4+Na2SO4;每生成1mol Cr(OH)(H2O)5SO4消耗SO2的物質的量為。
(4)印刷電路鋼板腐蝕劑常用FeCl3.腐蝕鋼板后的混合溶液中,若Cu2+、Fe3+和Fe2+的濃度均為0.10mol/L.請參照上表給出的數據和提供的藥品,簡述除去CuCl2溶液中Fe3+和Fe2+的實驗步驟:①;②;③過濾。(提供的藥品:Cl2、濃H2SO4、NaOH溶液、CuO、Cu)。組卷:3引用:2難度:0.4


