2015-2016學年湖南省長沙市瀏陽一中高二(上)入學化學試卷
發(fā)布:2024/4/20 14:35:0
一、選擇題(每小題只有一個正確選項,1-10題每小題2分,11-20題每小題2分)
-
1.構建和諧社會的總要求之一是人與自然和諧相處,下列做法不符合這一主題的是( )
A.中科院廣州化學所在利用二氧化碳制取可降解塑料的技術方面處于世界領先水平,該技術的成功應用將有效改善以二氧化碳為主的溫室氣體引發(fā)的“厄爾尼諾”、“拉尼娜”等全球氣候異常現象 B.許多國家對聚乙烯等塑料垃圾進行了深埋或者傾倒入海處理,達到消除“白色污染”的目的 C.山東單縣采用以雜草、秸稈等為原料的生物質發(fā)電,有效地減少了二氧化硫的排放 D.汽油中摻入酒精使用,可以降低對環(huán)境的污染和節(jié)約能源 組卷:6引用:1難度:0.9 -
2.某課外小組將海帶的灰燼浸泡后過濾,得到澄清的濾液,他們設計了如下幾種方案,你認為能證明灼燒海帶的灰燼中是否含有碘元素的是( )
A.取適量濾液,向其中加入H2O2溶液,再加入淀粉溶液,觀察 B.取適量濾液,加入CCl4,振蕩、靜置,觀察 C.取適量濾液,蒸干,觀察 D.取適量濾液,加入酸化的H2O2溶液,再加入淀粉溶液,觀察 組卷:18引用:3難度:0.9 -
3.下列說法中正確的是( )
A.物質發(fā)生化學反應時都伴隨著能量變化,伴隨能量變化的物質變化一定是化學變化 B.需要加熱的化學反應一定是吸熱反應,不需要加熱就能進行的反應一定是放熱反應 C.吸熱反應就是反應物的總能量比生成物的總能量高;也可以理解為化學鍵斷裂時吸收的能量比化學鍵形成時放出的能量多 D.因為3O2═2O3是吸熱反應,所以臭氧比氧氣的化學性質更活潑 組卷:137引用:14難度:0.5 -
4.堿性電池具有容量大、放電電流大的特點,因而得到廣泛使用,鋅-錳堿性電池以氫氧化鉀溶液為電解液,電池總反應為:Zn(s)+2MnO2(s)+H2O(l)═Zn(OH)2(s)+Mn2O3(s)下列說法錯誤的是( )
A.電池工作時,鋅失去電子 B.電池正極的電極反應式為:2MnO2(s)+H2O(l)+2e-═Mn2O3(s)+2OH-(aq) C.電池工作時,電子由正極通過外電路流向負極 D.外電路中每通過0.1mol電子,鋅的質量理論上減小6.5g 組卷:182引用:81難度:0.5 -
5.如圖所示裝置中,觀察到電流計指針偏轉;M棒變粗;N棒變細,由此判斷表中所列M、N、P物質,其中可以成立的是( )
M N P A Zn Cu 稀H2SO4溶液 B Cu Fe 稀HCl溶液 C Ag Zn AgNO3溶液 D Zn Fe Fe(NO3)3溶液 
A.A B.B C.C D.D 組卷:164引用:33難度:0.9 -
6.從南方往北方長途運輸水果時,常常將浸泡有高錳酸鉀溶液的硅藻土放置在盛放水果的容器中,其目的是( )
A.利用高錳酸鉀溶液吸收水果產生的乙烯,防止水果早熟 B.利用高錳酸鉀溶液吸收水果周圍的氧氣,防止水果腐爛 C.利用高錳酸鉀溶液的氧化性,催熟水果 D.利用高錳酸鉀溶液殺死水果周圍的細菌,防止水果霉變 組卷:211引用:13難度:0.9 -
7.反應A+3B═4C+2D,在不同條件下反應,其平均反應速率v(X)(表示反應物的消耗速率或生成物的生成速率)如下,其中反應速率最快的是( )
A.v(A)=0.4mol/(L?s) B.v(B)=0.8mol/(L?s) C.v(C)=1.2mol/(L?s) D.v(D)=0.7mol/(L?s) 組卷:81引用:10難度:0.9 -
8.將淀粉水解,并用新制的氫氧化銅懸濁液檢驗其水解產物的實驗中,要進行的主要操作是( )
①加熱 ②滴入稀硫酸 ③加入新制的氫氧化銅懸濁液 ④加入足量的氫氧化鈉溶液.A.①→②→③→④→① B.②→①→④→③→① C.②→④→①→③→① D.③→④→①→②→① 組卷:484引用:19難度:0.5
二、非選擇題(50分)
-
24.如圖是利用廢銅屑(含雜質)制備膽礬(硫酸銅晶體)的過程
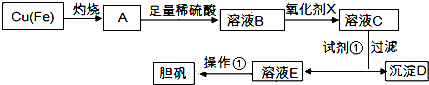
已知:
請回答:溶液中被沉淀的離子 Fe3+ Fe2+ Cu2+ 完全生成氫氧化物的沉淀時,溶液的pH ≥3.7 ≥6.4 ≥4.4
(1)下列物質中最適宜作氧化劑X的是(填字母).
A.NaClO B.H2O2 C.KMnO4
(2)加入試劑①是為了調節(jié)pH,試劑①可以選擇(填化學式).
(3)操作①的名稱是.
(4)沉淀D加入鹽酸可以得到FeCl3溶液,關于FeCl3溶液的性質中說法不正確的是.
A.將FeCl3飽和溶液逐滴加入沸水中,并繼續(xù)加熱得到紅褐色液體,該液體能產生丁達爾效應
B.向FeCl3溶液滴加NaOH溶液,出現紅褐色沉淀
C.將FeCl3溶液滴加NaOH溶液,將沉淀干燥灼燒,得到Fe(OH)3固體
D.向FeCl3溶液中滴加KSCN溶液,溶液變?yōu)榧t色
(5)沉淀D加入鹽酸和鐵粉,可以制得FeCl2溶液,實驗室保存FeCl2溶液,需加入過量的鐵粉防止FeCl2溶液變質,其原因是(用離子方程式表示).組卷:18引用:5難度:0.3 -
25.在2L和密閉容器中放入4molN2O5,發(fā)生如下反應:2N2O5(g)═4NO2(g)+O2(g)反應進行到5min時,測得N2O5轉化了20%,求:
(1)5min時,剩余N2O5的物質的量;
(2)前5min,v(NO2)為多少;
(3)5min時,N2O5的物質的量占混合氣體總物質的量的百分比.組卷:1引用:2難度:0.5


