2020-2021學(xué)年遼寧省沈陽市實驗學(xué)校中學(xué)部九年級(上)第四次月考化學(xué)試卷
發(fā)布:2024/4/20 14:35:0
一、選擇題(每題只有一個正確答案,共29小題,每題2分,共60分)
-
1.實驗室中的破碎玻璃可以回爐制作新的玻璃儀器,碎玻璃屬于( )
A. 
B. 
C. 
D.  組卷:101引用:5難度:0.8
組卷:101引用:5難度:0.8 -
2.世界是不斷變化的,下列變化中分子種類發(fā)生改變的是( )
A. 
水的沸騰B. 
電解水C. 
水的凈化D.  干冰升華組卷:106引用:5難度:0.8
干冰升華組卷:106引用:5難度:0.8 -
3.下列實驗操作或設(shè)計中正確的是( )
A. 
用量筒量取25mL水B. 
用排水法收集CO2氣體C. 
驗證質(zhì)量守恒定律D. 
分離水中的二氧化錳組卷:75引用:4難度:0.8 -
4.物質(zhì)的用途和性質(zhì)密切相關(guān),下列用途主要是利用其化學(xué)性質(zhì)的是( )
A.石墨用于制作鉛筆 B.薯片包裝填充氮氣用作防腐 C.活性炭用于防毒面具 D.氫氣用作充灌探空氣球 組卷:6引用:2難度:0.8 -
5.下列實驗中,有關(guān)現(xiàn)象的描述正確的是( )
A.紅磷在空氣中燃燒產(chǎn)生大量的白霧 B.鐵絲在空氣中劇烈燃燒,火星四射,生成黑色固體 C.鎂條在空氣中燃燒發(fā)出耀眼的白光 D.硫粉在空氣中燃燒產(chǎn)生藍紫色火焰 組卷:11引用:2難度:0.6 -
6.下面是實驗室依次制備,收集,驗證、驗滿CO2的裝置,其中正確的是( )
A. 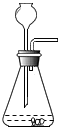
B. 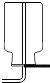
C. 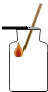
D.  組卷:839引用:64難度:0.9
組卷:839引用:64難度:0.9 -
7.我們在日常生活中都要食用碘鹽,許多人喜歡購買增鐵醬油、高鈣牛奶、富硒茶葉等.這里所說的碘、鐵、鈣、硒指的是( )
A.單質(zhì) B.化合物 C.元素 D.原子 組卷:23引用:26難度:0.9 -
8.下列化學(xué)用語與所表達的意義或理解相符合的是( )
A.構(gòu)成金剛石和C60微粒的類型相同 B.  和
和 化學(xué)性質(zhì)相似
化學(xué)性質(zhì)相似C.2個硫酸根離子:2SO42- D.C60:60個碳原子 組卷:7引用:2難度:0.5 -
9.高鐵酸鉀(K2FeO4)是一種新型、高效、多功能水處理劑,高鐵酸鉀與水反應(yīng)的化學(xué)方程式是:4K2FeO4+10H2O═4X↓+8KOH+3O2↑,下列說法錯誤的是( )
A.高鐵酸鉀中鐵+6價 B.高鐵酸鉀屬于氧化物 C.X的化學(xué)式是Fe(OH)3 D.高鐵酸鉀應(yīng)密封、防水保存 組卷:249引用:13難度:0.7 -
10.R元素的一種粒子的結(jié)構(gòu)示意圖為
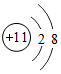 ,則下列說法的正確的是( )
,則下列說法的正確的是( )A.該粒子是陰離子 B.該粒子的核內(nèi)有11個中子 C.R元素為金屬元素 D.R元素的原子有10個電子 組卷:34引用:12難度:0.7 -
 11.錳(Mn)是維持人體正常生命活動所必須的微量元素,含錳化合物在生產(chǎn)、生活中也被廣泛應(yīng)用。結(jié)合圖中信息,下列敘述正確的是( )
11.錳(Mn)是維持人體正常生命活動所必須的微量元素,含錳化合物在生產(chǎn)、生活中也被廣泛應(yīng)用。結(jié)合圖中信息,下列敘述正確的是( )A.錳原子核內(nèi)有25個質(zhì)子,一個錳原子的質(zhì)量是54.94g B.錳元素位于第4周期,其化學(xué)性質(zhì)由最內(nèi)層電子數(shù)決定 C.MnO2屬于氧化物,能做所有化學(xué)反應(yīng)的催化劑 D.錳原子易失去電子 組卷:8引用:1難度:0.6
二.填空題(每空1分,方程式1.5分,共32分)
-
32.某校化學(xué)興趣小組學(xué)習(xí)了氣體的制取和收集后,對相關(guān)知識進行總結(jié),請你一起參與,并完成下面題目內(nèi)容:
 (1)寫出下列儀器名稱:b 。
(1)寫出下列儀器名稱:b 。
(2)寫出實驗室用A裝置制取氧氣的化學(xué)方程式:,若用F裝置收集氧氣,則氧氣應(yīng)從口通入(填“c”或“d”)。
③裝置B、C都可用來制取二氧化碳,裝置C相對于裝置B在操作方面的優(yōu)勢是。
(4)制取二氧化碳也可用加熱碳酸氫鈉(NaHCO3)固體的方法,生成物為碳酸鈉、二氧化碳和水,該反應(yīng)的化學(xué)方程式,若用此法來制取CO2,應(yīng)選用的發(fā)生裝置為。
(5)若用G測量生成的CO2氣體的體積,其中在水面上放一層植物油目的是;植物油上方原有的空氣對實驗結(jié)果(填“有”或“無”)明顯影響。
(6)乙炔(C2H2)是一種重要的化工原料,實驗室常用碳化鈣(CaC2)與水在常溫下反應(yīng)制取乙炔氣體,反應(yīng)非常劇烈。實驗室制取乙炔應(yīng)選擇的發(fā)生裝置為,該裝置的優(yōu)點是。組卷:27引用:2難度:0.4
三、計算題(共8分)
-
33.鈣是人體必需的常量元素,如圖是某種品牌的補鈣藥品的部分說明書,為探究人體每天補鈣量,小明同學(xué)進行實驗測定,請回答下列問題:
(1)該實驗中,裝置的氣密性對測定結(jié)果(填“有”或“無”)影響。
(2)實驗過程中生成CO2克。
(3)計算該補鈣劑中碳酸鈣的質(zhì)量分數(shù)。(請根據(jù)化學(xué)方程式計算并書寫計算步驟) 組卷:337引用:3難度:0.4
組卷:337引用:3難度:0.4


