2022年湖北省卓越千校聯盟高考化學押題試卷
發布:2024/12/24 1:0:2
一、選擇題:本題共15小題,每小題3分,共45分.在每小題給出的四個選項中,只有一項是符合題目要求的.
-
1.2022年北京冬奧會和冬殘奧會通過科技助力,體現環保理念.下列說法正確的是( )
A.全部餐具均由可降解聚乳酸生物新材料制作,因其美觀大方 B.全部場館首次采用100%綠色電力,所產生的碳排放量全部實現碳中和 C.冬奧火炬外殼首次使用有機高分子的碳纖維材料制作,堅持綠色辦奧 D.國家速滑館使用的二氧化碳跨臨界直冷制冰系統,與傳統制冷劑氟利昂相比,更不環保 組卷:69引用:1難度:0.9 -
2.2021年我國在載人航天、北斗、探月、探火工程上取得重大進展,航天成就驚艷全球.下列有關說法不正確的是( )
A.長征五號火箭采用液氫作為燃料,其燃燒產物對環境無污染 B.“天問一號”火星車使用的保溫材料--納米氣凝膠,具有丁達爾效應 C.月壤中含有 He,其中子數為132D.宇航服“液冷層”所用的尼龍材料,屬于天然有機高分子材料 組卷:40引用:1難度:0.9 -
3.設阿伏加德羅常數的值為NA.下列說法正確的是( )
A.17g羥基(-OH)所含質子總數為10NA B.標準狀況下,2.24LH2O中含有O-H鍵的個數為0.2NA C.78gNa2O2與足量的SO2反應,轉移電子數為2NA D.0.5mol乙酸乙酯在堿性條件下水解,生成乙醇的分子數小于0.5NA 組卷:85引用:1難度:0.6 -
4.下列實驗設計能夠完成且結論合理的是( )
A.可用玻璃棒蘸取氯水點在pH試紙上,待變色后和標準比色卡比較測出氯水的pH B.向AgCl懸濁液中滴2滴Na2S稀溶液,產生黑色沉淀,證明AgCl的溶解度大于Ag2S C.將50mL稀NaOH溶液緩慢倒入盛有等量鹽酸的燒杯中,記錄溫度可測定中和熱 D.將少量溴水滴加入苯酚溶液中,未見到白色沉淀,表明苯酚已經變質 組卷:29引用:2難度:0.7 -
5.下列離子方程式正確的是( )
A.用小蘇打治療胃酸過多:CO32-+2H+═CO2↑+H2O B.向石灰石上滴加稀醋酸:CaO+2CH3COOH═Ca2++2CH3COO-+H2O C.向氯化鋁溶液滴加過量的氨水:Al3++4OH-═AlO2-+2H2O D.向Ba(OH)2溶液中逐滴滴加NaHSO4溶液至中性:Ba2++2OH-+SO42-+2H+═BaSO4↓+2H2O 組卷:172引用:1難度:0.5 -
 6.一種光刻膠樹脂單體的結構簡式如圖所示。下列說法正確的是( )
6.一種光刻膠樹脂單體的結構簡式如圖所示。下列說法正確的是( )A.該有機物分子式為C12H19O2 B.分子中存在3個手性碳原子 C.與足量氫氣加成,消耗2molH2 D.該單體水解產物不能發生消去反應 組卷:44引用:1難度:0.7
二、非選擇題:本題共4小題,共55分.
-
18.對氯苯氧乙酸是一個常用的植物生長調節劑,俗稱“防落素”,可以減少農作物或瓜果蔬菜的落花落果,有明顯的增產作用.其實驗原理為
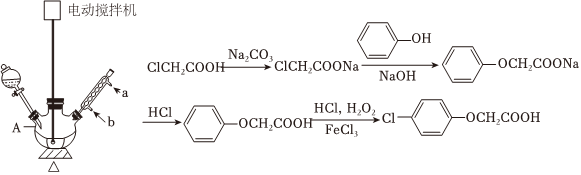
實驗步驟:①在反應器中,加入3.8g氯乙酸和5mL水,開始攪拌,慢慢滴加飽和碳酸鈉溶液,至溶液的pH為7~8,然后加入2.5g苯酚,再慢慢滴加35%氫氧化鈉溶液至pH=12;
②將反應器置于油浴中緩慢加熱,維持此溫度20min;
③移去油浴,用濃鹽酸調pH=4,析出固體,抽濾,水洗2~3次,再用乙醇溶液洗滌,得到粗產品;
④加入少量三氯化鐵和10mL濃鹽酸,升溫至60~70℃,滴加雙氧水,反應20~30min,升溫使固體溶解,慢慢冷卻,析出固體,抽濾,洗滌,重結晶.
完成下列問題:
(1)裝置中A的名稱是,球形冷凝管的出水口是(填“a”或“b”).
(2)步驟②中采用油浴加熱,不采用直接加熱的原因是.
(3)步驟④升溫至60~70℃,溫度不宜過低也不宜過高的主要原因是.
(4)用乙醇溶液洗滌粗產品的目的是.
(5)步驟③和④均涉及抽濾,下列關于抽濾的說法中正確的是.
A.抽濾的主要目的是得到較多的沉淀
B.濾紙的直徑應略小于漏斗內徑,又能蓋住全部小孔
C.圖中沒有明顯出錯
D.抽濾結束,從吸濾瓶的支管口倒出濾液
(6)步驟④中加入濃鹽酸的目的是,有時需要將“粗產品用沸水溶解,冷卻結晶,抽濾”的操作進行多次,其目的是.組卷:25引用:2難度:0.7 -
19.以CO2和H2O為原料可以制得淀粉,實現“喝西北風”吃飽;CO2與H2O可在不同催化劑和反應條件下生成CO和CH3OH等多種化合物,在減少溫室氣體、減少化石能源使用、新能源開發利用等方面有重要的作用.
(1)單個CO2分子與H2在催化劑的作用下反應歷程如圖甲所示:(吸附在催化劑表面的物質用?標注,如?CO2表示CO2吸附在催化劑表面;圖中Ts表示過渡態分子).
反應歷程中活化能(能壘)最小的化學方程式為,CO2(g)+H2(g)=CO(g)+H2O(g)ΔH=eV/mol
(2)CO2與H2在某催化劑的作用下反應如圖乙所示:
寫出該反應的熱化學方程式:化學鍵 




鍵能(kJ/mol) 436 326 803 464 414 ,體系達到平衡后,若要使平衡向正反應方向移動,可以改變的條件是(任寫一種).
(3)在相同的恒容容器中,10min內三種不同的催化劑對CO2與H2反應的影響如圖丙所示:
①下列說法正確的是.
a.使用催化劑Ⅰ,反應轉化率最高
b.由圖得出此反應一定是放熱反應
c.最佳催化劑是催化劑Ⅰ
d.a、b、c三點的速率大小關系一定為:Va(CO2)>Vb(CO2)>Vc(CO2)
②若此反應起始投料為5molCO2和15molH2,在10L恒容密閉容器中進行,且反應時間足夠長,得到如圖關系式,則T3溫度下,反應的平衡常數K=(用分數形式表示),在催化劑Ⅰ作用下,從起始到a點H2的平均反應速率為.組卷:51引用:1難度:0.5


