2016-2017學年浙江省杭州十三中九年級(上)期初化學試卷
發布:2024/4/20 14:35:0
一、選擇題(每小題3分,共54分,每小題只有一個選項符合題意)
-
1.下列各組離子中,由酸電離產生的是( )
A.H+、Cl- B.H+、K+、SO42- C.Cu2+、SO42- D.Na+、OH- 組卷:90引用:3難度:0.7 -
2.下列各組物質的名稱、俗稱、化學式均表示同一種物質的是( )
A.硫酸銅晶體,膽礬,CuSO4?5H2O B.氯化鈉,蘇打,NaCl C.氫氧化鈉,純堿,NaOH D.碳酸鈣,生石灰,Ca(OH)2 組卷:76引用:4難度:0.9 -
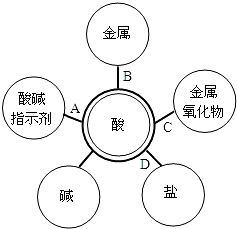 3.歸納總結是學習的重要方法。小明同學在學習“應用廣泛的酸、堿、鹽”知識后,結合常見酸(HCl、H2SO4)的性質與變化繪制出圖。圖中“-”兩端的物質都能夠反應,其中酸堿中和反應生成鹽和水,則其他連線的產物也都是鹽和水的是( )
3.歸納總結是學習的重要方法。小明同學在學習“應用廣泛的酸、堿、鹽”知識后,結合常見酸(HCl、H2SO4)的性質與變化繪制出圖。圖中“-”兩端的物質都能夠反應,其中酸堿中和反應生成鹽和水,則其他連線的產物也都是鹽和水的是( )A.A B.B C.C D.D 組卷:219引用:14難度:0.9 -
4.下列實際應用中,利用中和反應原理的是( )
①用生石灰作食品干燥劑;②用熟石灰和硫酸銅配制波爾多液;③施用熟石灰改良酸性土壤;④用氫氧化鈉溶液處理泄漏的濃硫酸。A.①② B.③④ C.①④ D.②③ 組卷:208引用:46難度:0.9 -
5.如何減少溫室氣體二氧化碳的含量是科學家一直在探究的課題,最近中國科學技術大學的專家找到一種新型催化劑,可將二氧化碳轉化為液體燃料甲酸(CH2O2),下列說法中,不正確的是( )
A.地球上二氧化碳含量上升的主要原因是植物的呼吸作用 B.二氧化碳能阻擋地面輻射,對地球有保溫作用 C.二氧化碳轉化為甲酸的過程屬于化學變化 D.這種新型催化劑在反應前后質量不變 組卷:672引用:27難度:0.9 -
6.下表記錄了在物質 X 的溶液中分別加入三種物質的溶液后產生的現象.由此可知,物質 X 可能是( )
加入的物質 氫氧化鈉 碳酸鈉 紫色石蕊試液 物質X中的現象 無明顯現象 產生氣泡 溶液變紅 A.Ca(OH)2 B.CO2 C.CuSO4 D.HCl 組卷:30引用:3難度:0.7 -
7.下列各組物質,能在pH=1的溶液中大量共存,且形成無色溶液的是( )
A.NaCl、Na2SO4、Na2CO3 B.NaOH、BaCl2、Na2SO4 C.NaNO3、HCl、Na2SO4 D.NaNO3、NaCl、CuSO4 組卷:50引用:52難度:0.7
四、分析計算題(本大題共30分,29題11分,30題10分,31題9分)
-
22.某化學興趣小組為了測定鎂銅合金中鎂的質量分數,取出3g合金樣品,將60g稀硫酸分6次加入樣品中,充分反應后過濾、洗滌、干燥、稱重,得到的實驗數據如下:
(1)測定過程中發生反應的化學方程式為稀硫酸用量 剩余固體質量 第一次加入10g mg 第二次加入10g 2.0g 第三次加入10g 1.5g 第四次加入10g 1.0g 第五次加入10g 0.6g 第六次加入10g 0.6g ;
(2)從以上數據可知,最后剩余的0.6g固體的成分是;這六次實驗中,第次加入稀硫酸時樣品中的鎂已經完全反應;表格中,m=。
(3)計算合金樣品中鎂的質量分數。
(4)計算所用稀硫酸中H2SO4的質量分數。組卷:314引用:27難度:0.5 -
23.圖甲中A是一種常見的酸,它能與黑色固體B反應,B質量為8克,將NaOH溶液漸漸加入到C中,生成藍色沉淀E的質量與加入NaOH溶液的質量關系如圖乙所示,在D中加入Ba(NO3)2溶液能生成一種不溶于稀硝酸的白色沉淀。
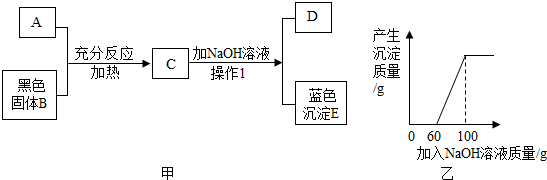
(1)A溶液中溶質的化學式為;
(2)操作1的名稱是;
(3)NaOH溶液中溶質的質量分數是多少?
(4)C溶液中加入NaOH溶液至恰好完全反應時,所得溶液溶質的質量是多少?組卷:1208引用:70難度:0.5


