元素周期表是學習和研究化學的重要工具。下圖是元素周期表的一部分。
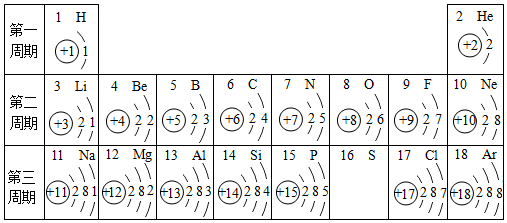
(1)很多科學家對元素周期表的發(fā)現(xiàn)和完善做出了重大貢獻,請寫出其中一位科學家的名字:門捷列夫門捷列夫。
(2)表中與鈹(Be)元素化學性質(zhì)相似的元素為鎂鎂。
(3)在化學反應(yīng)中,鎂元素的原子容易失去電子變成陽陽(填“陰”或“陽”)離子;S2-的核外電子排布和氬氬原子的核外電子排布相同,一個過氧化氫分子中共有2020個質(zhì)子。
(4)一般地說,電子層數(shù)相同的原子(稀有氣體除外),原子的半徑隨原子序數(shù)的遞增而減小;最外層電子數(shù)相同的原子,原子的半徑隨電子層數(shù)的增大而增大。請比較:氧原子、氮原子和磷原子的半徑由大到小的順序為P>N>OP>N>O(用“<”或“>”連接)。
(5)研究表明:在同一周期中,從左到右,原子失去電子的能力逐漸減弱,得到電子的能力逐漸增強。由此推斷:第三周期中得電子能力最強的是氯氯原子;具有相對穩(wěn)定結(jié)構(gòu)的是氬氬原子。
【答案】門捷列夫;鎂;陽;氬;20;P>N>O;氯;氬
【解答】
【點評】
聲明:本試題解析著作權(quán)屬菁優(yōu)網(wǎng)所有,未經(jīng)書面同意,不得復制發(fā)布。
發(fā)布:2024/6/27 10:35:59組卷:9引用:1難度:0.6
相似題
-
1.如圖是元素周期表的部分,根據(jù)如圖的信息回答下列問題。
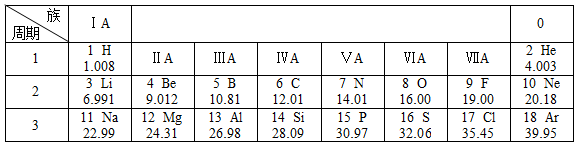
(1)相對原子質(zhì)量為28.09的元素屬于(填“金屬”或“非金屬”)元素,F(xiàn)的相對原子質(zhì)量為。
(2)不同種元素的本質(zhì)區(qū)別是。
A.質(zhì)子數(shù)不同
B.相對原子質(zhì)量不同
C.中子數(shù)不同
(3)如圖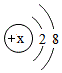 為R3+粒子結(jié)構(gòu)示意圖,則x=,該元素位于周期表中第周期。
為R3+粒子結(jié)構(gòu)示意圖,則x=,該元素位于周期表中第周期。
(4)表中與鈉元素化學性質(zhì)相似的金屬元素是(填元素符號)。發(fā)布:2025/1/18 8:0:1組卷:11引用:1難度:0.5 -
2.根據(jù)下列粒子結(jié)構(gòu)示意圖,回答問題。
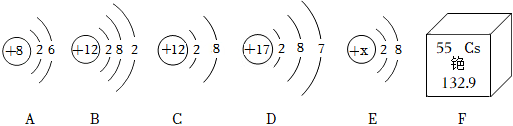
(1)A、B、C、D所示粒子共表示種元素。
(2)D所示粒子在化學反應(yīng)中容易電子(填“得到”或“失去”)。
(3)若E中x=10時,則該粒子屬于(填“原子”或“離子”)。
(4)F的相對原子質(zhì)量為。
(5)與元素的化學性質(zhì)關(guān)系最密切的是(填序號)。
①原子的核外電子數(shù)
②元素的相對原子質(zhì)量
③元素的原子序數(shù)
④原子的最外層電子數(shù)發(fā)布:2025/1/18 8:0:1組卷:36引用:2難度:0.5 -
3.根據(jù)下列粒子結(jié)構(gòu)示意圖,回答問題。
?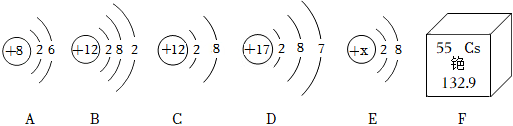
(1)A、B、C、D所示粒子共表示種元素。
(2)D所示粒子在化學反應(yīng)中容易電子(填“得到”或“失去”),B、D形成化合物的化學式。
(3)若E中x=10時,則該粒子屬于(填“原子”或“離子”)。
(4)F的相對原子質(zhì)量為。
(5)與元素的化學性質(zhì)關(guān)系最密切的是(填序號)。
①原子的核外電子數(shù)
②元素的相對原子質(zhì)量
③元素的原子序數(shù)
④原子的最外層電子數(shù)發(fā)布:2025/1/18 8:0:1組卷:7引用:1難度:0.5
相關(guān)試卷


