化學教材“尋找新的催化劑”研究性實驗,引起了化學探究小組的興趣。
【實驗探究一】氧化鐵能否作過氧化氫溶液分解的催化劑?
甲同學依次設計了三個實驗:
實驗一:取一定量的H2O2溶液于試管中,觀察到有極少量氣泡產生,伸入帶火星的木條,沒有復燃。說明H2O2溶液常溫下緩慢分解。
實驗二:在實驗一的試管中加入WgFe2O3粉末,有大量氣泡產生,然后伸入帶火星的木條,木條復燃。說明 Fe2O3粉末能加快過氧化氫分解的速率Fe2O3粉末能加快過氧化氫分解的速率。
實驗三:待反應結束后,將試管里的不溶物濾出,并洗滌、干燥、稱量,固體質量仍為Wg。說明 反應前后Fe2O3的質量沒有改變反應前后Fe2O3的質量沒有改變。
【實驗結論】甲同學認為,Fe2O3粉末可以作為H2O2分解的催化劑。
【反思評價】乙同學認為要證明甲同學的結論正確,僅做這三個實驗還不充分,需要再補充一個探究實驗。該實驗是 在裝有一定量過氧化氫溶液的試管中加入實驗三得到的固體,然后伸入帶火星的木條在裝有一定量過氧化氫溶液的試管中加入實驗三得到的固體,然后伸入帶火星的木條。
【實驗探究二】催化劑的質量大小是否對過氧化氫溶液分解的速率產生影響?
興趣小組同學設計如圖1所示實驗裝置,利用壓強傳感器測不同質量二氧化錳對雙氧水分解快慢的影響。在8mL3%的雙氧水中分別加入了0.08g,0.12g,0.24gMnO2.測得容器內壓強的變化曲線如圖2所示(曲線的斜率表征催化反應的速率)。據此回答問題:
?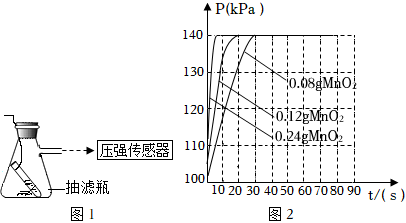
(1)根據圖2可發現:該實驗條件下,30s內催化分解8mL濃度為3%的雙氧水,MnO2的最小用量為 0.080.08克。
(2)根據圖2,下列說法正確的是 abcabc。(填字母)
a.一定范圍內,二氧化錳用量越多,雙氧水分解越快;
b.反應容器的氣密性,對實驗所測數據的精確度有影響;
c.稱量的二氧化錳質量的精確度對實驗裝置中最終的壓強大小沒有影響。
【實驗探究三】過氧化氫溶液質量分數是否對過氧化氫溶液分解的速率產生影響?
用注射器加入不同濃度的H2O2溶液(見下表),實驗中使用傳感器裝置測算生成O2的質量(如圖3所示)(圓底燒瓶內氣壓變化在安全范圍),繪制氧氣質量隨時間變化的曲線,如圖4所示。
| 實驗編號 | H2O2的質量分數(%) | H2O2溶液的體積(mL) | 對應曲線 |
| Ⅰ | 3.4 | 10.0 | a |
| Ⅱ | 2.4 | 10.0 | b |
| Ⅲ | 1.7 | 10.0 | c(待繪制) |
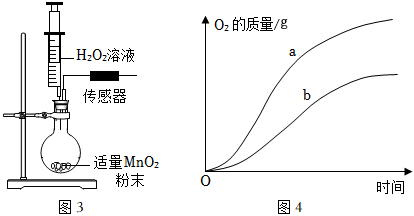
(1)根據實驗探究目的,從圖4曲線a、b中,可得出的結論是
過氧化氫溶液的質量分數越大,分解的速率越快
過氧化氫溶液的質量分數越大,分解的速率越快
。(2)在圖4中畫出曲線c的大致位置及趨勢。
【考點】影響化學反應速率的因素探究;催化劑的特點與催化作用.
【答案】Fe2O3粉末能加快過氧化氫分解的速率;反應前后Fe2O3的質量沒有改變;在裝有一定量過氧化氫溶液的試管中加入實驗三得到的固體,然后伸入帶火星的木條;0.08;abc;過氧化氫溶液的質量分數越大,分解的速率越快
【解答】
【點評】
聲明:本試題解析著作權屬菁優網所有,未經書面同意,不得復制發布。
發布:2024/9/26 2:0:2組卷:23引用:1難度:0.5
相似題
-
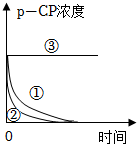 1.Fenton法常用于處理含難降解有機物的工業廢水。其原理是利用Fe2+和H2O2的反應產生能降解污染物的活性成分。現運用該方法降解有機污染物p-CP,探究有關因素對降解反應速率的影響。實驗探究:控制p-CP的初始濃度相同,實驗溫度恒定在25℃或40℃(其余實驗條件見下表)。
1.Fenton法常用于處理含難降解有機物的工業廢水。其原理是利用Fe2+和H2O2的反應產生能降解污染物的活性成分。現運用該方法降解有機污染物p-CP,探究有關因素對降解反應速率的影響。實驗探究:控制p-CP的初始濃度相同,實驗溫度恒定在25℃或40℃(其余實驗條件見下表)。
(1)請結合上述介紹將表中空格補充完整。
(2)實驗測得p-CP的濃度隨時間變化的關系如圖所示,根據實驗①、②圖像可得出結論:實驗編號 實驗目的 溫度/℃
pH濃度/(mg?L﹣1) H2O2 Fe2+ ① 為②③提供參照 25 3 204 16.8 ② 探究溫度對降解反應速率的影響
3 204 16.8 ③ 探究溶液pH對降解反應速率的影響 25 10 204 16.8 。
(3)為測定不同時間內有機物降解的濃度,需在不同時間從反應器中取樣,并使所取樣品中的降解反應立即停止下來。根據本題信息,將樣品從反應器中取出后應立即將其放入某藥品中,反應會迅速停止,該藥品可能是。
A鹽酸溶液 B氫氧化鈉溶液 C稀硫酸溶液 D碳酸鈉溶液發布:2024/11/25 8:0:2組卷:4引用:0難度:0.3 -
2.據圖1裝置圖回答問題
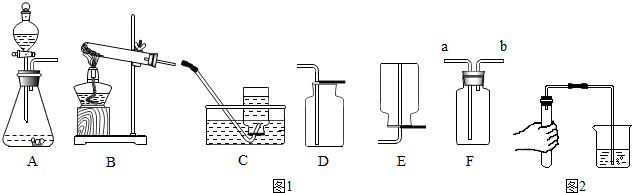
(1)甲同學用氯酸鉀和二氧化錳共熱制備和收集氧氣,他應選用的氣體發生裝置是(填序號).他用裝置C來收集的原因是,當看到導管口的時他才開始收集氧氣.
(2)該同學用如圖2所示的方法進行氣密性檢查,如果裝置不漏氣,可以看到,將手松開一段時間后(導管仍插入水中),可以看到導管中會形成一段水柱.
(3)因為氧氣的密度比空氣的稍大,所以還可以選用(填序號)來收集氧氣,其驗滿的方法是.
(4)老師提醒可以用F(萬能瓶)來收集氣體,則甲同學應將發生裝置的導管與F的導管(選填a或b)相連接.
(5)乙同學稱取一定質量的KMnO4固體放入大試管中,將溫度控制在250℃加熱制取O2.實驗結束時,這位同學發現用排水法收集到的O2大于理論產量.針對這一現象,同學們進行了如下探究:
【提出猜想】猜想Ⅰ:反應生成的二氧化錳(MnO2)分解放出O2;
猜想Ⅱ:反應生成的錳酸鉀(K2MnO4)分解放出O2;
【實驗驗證】同學們分成兩組,分別進行下列實驗:
第一組同學取一定質量的MnO2,在250℃條件下加熱一段時間,冷卻后測得MnO2的質量不變,則猜想(選填Ⅰ或Ⅱ)錯誤;
第二組同學取K2MnO4在250℃條件下加熱,沒有用測定質量的方法得出了猜想Ⅱ正確的結論.該組同學選擇的實驗方法是.
【拓展延伸】實驗發現,KClO3固體加熱制取O2的反應速率很慢,但如果將KMnO4固體與KClO3固體混合加熱,則KClO3的分解速率大大加快,請說明KMnO4在KClO3的分解反應中是否作催化劑,為什么?.
(6)丙同學選擇用雙氧水和二氧化錳混合來制氧氣,則他應選用的氣體發生裝置是(填序號).以下是他探究影響該反應速率因素的相關實驗數據.
通過以上實驗數據的分析,可知,過氧化氫分解制氧氣的化學反應速率與實驗
序號H2O2溶液濃度% H2O2溶液體積/mL 溫度℃ MnO2用量/g 收集到的
氧氣體積/mL反應所需的
時間/s① 5 1 20 1 30.29 ② 5 1 20 0.1 4 16.75 ③ 15 1 20 0.1 4 6.04 ④ 30 1 55 2 10.76 、、等因素有關;發生裝置中的(填儀器名稱)也可以幫助控制反應的速率.發布:2024/12/18 8:0:1組卷:12引用:2難度:0.5 -
3.下列探究影響化學反應速率因素的實驗中,實驗方案正確的是( )
選項 影響因素 實驗方案 A 接觸面積 將1g塊狀石灰石和20mL10%的稀鹽酸、1g粉末狀石灰石與20mL10%的稀硫酸混合,比較產生氣泡的快慢 B 催化劑的種類 將0.5g二氧化錳、1g氧化鐵分別與10mL6%的過氧化氫溶液混合,比較產生氣泡的快慢 C 反應物的種類 分別將木炭在空氣中、氧氣中燃燒,比較反應的劇烈程度 D 反應物的性質 分別用酒精燈加熱表面積相同的鎂片和鐵片,比較在空氣中能否被點燃 A.A B.B C.C D.D 發布:2024/12/25 13:0:1組卷:114引用:4難度:0.7


