2017年安徽省阜陽市太和縣中考化學一模試卷
發布:2025/6/29 12:0:10
一、本大題包括10小題,每小題2分,共20分.每小題的4個選項中只有1個符合題意,請將選出的選項序號填入下面的答題框內.
-
1.根據如圖所示的信息判斷,下列說法正確的是( )

A.硫原子的核內中子數為32 B.在化學反應中,硫原子容易失去電子 C.硫離子的符號為S2+ D.硫屬于非金屬元素 組卷:19引用:1難度:0.6 -
2.阿司匹林(化學式為C3H8O4)是常用緩解輕度或中度疼痛藥物,對預防心腦血管疾病也有一定作用。水溶液顯酸性。以下說法正確的是( )
A.阿司匹林屬于有機物 B.阿司匹林由21個原子構成 C.阿司匹林中氫、氧元素的質量比為2:1 D.石蕊溶液滴入阿司匹林水溶液中顯藍色 組卷:6引用:1難度:0.7 -
 3.甲、乙兩種不含結晶水的固體物質的溶解度曲線如圖,下列說法中錯誤的是( )
3.甲、乙兩種不含結晶水的固體物質的溶解度曲線如圖,下列說法中錯誤的是( )A.t1℃時,50g甲的飽和溶液中溶解了10g的甲 B.將t2℃時的甲、乙兩種物質的飽和溶液升溫至t3℃(溶劑的量不變),兩種溶液中溶質的質量分數相等 C.t2℃時,要使接近飽和的乙溶液達到飽和狀態,可以用蒸發溶劑的方法 D.甲物質的飽和溶液中含有少量乙,可采用降溫結晶的方法分離提純甲 組卷:176引用:63難度:0.7 -
4.各組物質能反應,而且充分反應后所得溶液的質量比反應前溶液的總質量增大的是( )
A.鋁和硫酸銅溶液 B.氯化鈉溶液和稀硫酸 C.把二氧化碳通入澄清的石灰水 D.碳酸鈣固體和稀鹽酸 組卷:332引用:13難度:0.7 -
5.下列化學方程式與事實相符且正確的是( )
A.酸雨形成的原因CO2+H2O═H2CO3 B.潔凈的銅絲浸入硝酸銀溶液中Cu+2AgNO3═Cu(NO3)2+2Ag C.在氧氣中點燃細鐵絲可發生劇烈燃燒Fe+O2═FeO2 D.加熱混有二氧化錳的氯酸鉀固體2KClO3═2KCl+O2↑ 組卷:46引用:1難度:0.6 -
6.2022年北京冬奧會是全球的冰雪盛會,下列舉措不符合“綠色冬奧”的是( )
A.開發新能源,減少化石燃料的使用 B.推廣使用清潔能源車輛 C.為方便運動員用餐,大量使用一次性木筷 D.使用不破壞臭氧層的二氧化碳作制冷劑制冰 組卷:13引用:3難度:0.8 -
7.下列用于存儲固體藥品的是( )
A. 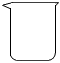
B. 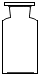
C. 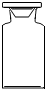
D. 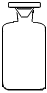 組卷:223引用:9難度:0.7
組卷:223引用:9難度:0.7 -
8.“樹藝五谷,五谷熟而民人育”。“五谷”中的小麥富含的營養素是( )
A.蛋白質 B.油脂 C.維生素 D.糖類 組卷:68引用:3難度:0.9 -
9.“一帶一路”是跨越時空的宏偉構思,賦予古絲綢之路嶄新的時代內涵。古絲綢之路將中國的發明和技術傳送到國外。下列涉及化學變化的是( )
A.雕刻玉器 B.火藥爆破 C.蠶絲織布 D.手剪紙花 組卷:11引用:1難度:0.5 -
10.下列涉及化學觀念中有關說法正確的是( )
A.微粒觀:水是由氫原子和氧原子構成的 B.分類觀:氧氣和二氧化碳都屬于氧化物 C.結構觀:氦原子和鎂原子最外層電子數相同,化學性質相似 D.變化觀:水和氫氣在一定條件下可相互轉化 組卷:13引用:2難度:0.7
二、本大題包括5小題,共34分.
-
 11.特快電熱壺由于快捷方便,被許多家庭、賓館使用。請據圖示回答:
11.特快電熱壺由于快捷方便,被許多家庭、賓館使用。請據圖示回答:
(1)制作材料中屬于金屬材料的是,屬于合成材料的是(填序號,寫出一種即可)。
(2)制作手柄的塑料屬于塑料(填“熱塑性”或“熱固性”)。
(3)用銅質材料制作電源插頭的插腳是利用銅具有性。組卷:1引用:2難度:0.7 -
12.下列裝置常用于實驗室制取氣體,請回答下列問題。

(1)寫出儀器①的名稱。
(2)小明同學用大理石和稀鹽酸制取二氧化碳,選擇B裝置作為發生裝置,長頸漏斗下端管口應,應選擇的收集裝置是(填字母代號)。
(3)將燃著的木條放在集氣瓶口,發現木條,說明二氧化碳已收集滿。組卷:286引用:3難度:0.6 -
13.某工廠廢液中含有NaCl、CuCl2和FeCl2,某化學興趣小組想廢物再利用,要從廢液中回收銅并得到鐵紅(主要成分Fe2O3 )。已知物質A是目前世界上年產量最大的金屬。他們設計的實驗方案如圖:
 回答下列問題:
回答下列問題:
(1)步驟Ⅰ進行的操作名稱為,在該操作中使用了多種玻璃儀器,其中玻璃棒的作用是;
(2)步驟①反應的化學方程式為;
(3)固體甲的成分有(填化學式);
(4)步驟④發生的化學反應方程式為:4Fe(OH)2+O2+2X=4Fe(OH)3,X的化學式為,該反應屬于反應(填基本反應類型);
(5)Fe(OH)3 加熱發生分解反應即可得到鐵紅的主要成分和水,寫出該反應的化學方程式是。組卷:51引用:1難度:0.5 -
14.近幾年我國某些工業城市酸雨污染較為嚴重,主要是因為大量燃燒含硫量高的煤而形成的,此外,各種機動車排放的尾氣也是形成酸雨的重要原因。
【提出問題】通過實驗證明煤中含有碳元素和硫元素。
【查閱資料】
(1)“二氧化硫能使高錳酸鉀溶液褪色(由紫紅色變為無色),該反應的化學方程式為:5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2X. 化學方程式中最后一種物質X的化學式是:。
(2)“二氧化硫和二氧化碳一樣,也能使澄清石灰水變渾濁。”請寫出二氧化硫與澄清石灰水反應的化學方程式:。
根據上述資料,甲同學、乙同學和丙同學分別設計實驗方案進行探究。
【實驗探究】(3)甲同學:“實驗操作”:甲同學進行了如圖1所示A、B兩步實驗:
“實驗現象”:A中稀高錳酸鉀溶液褪色,B中澄清石灰水變渾濁。
“得出結論”:煤燃燒生成二氧化硫和二氧化碳,證明煤中含有碳元素和硫元素。
(4)乙同學認為甲同學的實驗方案不合理,其理由是:。
(5)丙同學:“實驗操作”:丙同學進行了如圖2所示實驗(部分裝置在圖中略去):
【探究與結論】
(6)圖C裝置的作用是。
(7)要證明煤中含有碳元素和硫元素的現象是:丙同學的實驗中B中,C中的溶液不褪色,D中。
【定量計算】(8)用石灰石漿也能吸收廢氣中的二氧化硫,其反應原理是:
2CaCO3+O2+2SO22CaSO4+2CO2,一座小型火力發電廠每天要燃燒100t煤炭,其中硫元素的質量分數約為6.4%。高溫
①如果尾氣不處理,發電廠每月將向大氣中排放多少噸SO2(按30天計算)?
②每天至少需要含80%碳酸鈣的石灰石多少噸才能將其完全吸收?(寫出解題過程)組卷:23引用:1難度:0.4 -
15.小華在學習了鹽的相關知識后,將一定量的NaHCO3溶液和CaCl2溶液混合,沒有觀察到明顯現象。
【提出問題】NaHCO3溶液和CaCl2溶液能否發生反應?
【查閱資料】①在相同條件下,反應的劇烈程度與反應物的濃度有關;
②mol/L是一種表示溶液濃度的單位。
【實驗探究】向盛有相同體積的CaCl2溶液的4支試管中分別加入等體積的NaHCO3溶液,充分混合,觀察并記錄實驗現象:
【實驗分析】實驗裝置圖 實驗
序號CaCl2溶液濃度
(mol/L)NaHCO3溶液濃度
(mol/L)實驗現象 
① 0.01 0.01 無明顯現象 ② 0.01 0.09 產生白色沉淀 ③ x 0.45 產生白色沉淀并伴有氣泡 ④ 0.01 1.14 產生白色沉淀,有大量氣泡
(1)表中x=。
(2)經檢驗,實驗中產生的氣體能使澄清石灰水變渾濁,該氣體是。
【實驗結論】
(3)NaHCO3溶液和CaCl2溶液反應,除生成白色沉淀及氣體外,還會生成水和一種生活中常見的鹽,該反應的化學方程式為。
【交流反思】
(4)實驗②中不能觀察到氣泡的原因是。
(5)該實驗過程中,若要觀察到明顯的現象,還可采取的措施有(任寫一條)。組卷:26引用:2難度:0.6
三、本大題共6分.
-
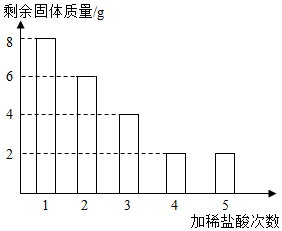 16.某化學興趣小組欲測定某石灰石樣品中碳酸鈣的質量分數,先將10g樣品放入燒杯中,再把100g稀鹽酸平均分成5份,分5次加入該樣品中(該實驗條件下,雜質不與酸反應,也不溶解于水;忽略稀鹽酸揮發;充分反應),得實驗數據如圖。
16.某化學興趣小組欲測定某石灰石樣品中碳酸鈣的質量分數,先將10g樣品放入燒杯中,再把100g稀鹽酸平均分成5份,分5次加入該樣品中(該實驗條件下,雜質不與酸反應,也不溶解于水;忽略稀鹽酸揮發;充分反應),得實驗數據如圖。
(1)10g石灰石樣品中碳酸鈣的質量分數是。
(2)求稀鹽酸的溶質質量分數(寫出計算過程,結果精確到0.1%)。組卷:135引用:5難度:0.5


