2024年廣東省廣州市從化區中考化學二模試卷
發布:2025/6/29 23:0:9
一、選擇題:本題包括14小題,每小題3分,共42分。每小題給出的四個選項中,只有一項最符合題意。錯選、不選、多選或涂改不清的,均不給分。
-
1.“艾葉香,香滿堂:粽子香,香廚房。”據研究,粽子的香味源于粽葉的主要成分一一對乙烯基苯酚(化學式為C8H8O)。下列說法不正確的是( )
A.對乙烯基苯酚屬于有機物 B.對乙烯基苯酚由3種元素組成 C.對乙烯基苯酚由8個C原子、8個H原子、1個O原子構成 D.對乙烯基苯酚中C、H、O三種元素的原子個數比為8:8:1 組卷:11引用:1難度:0.6 -
2.化學工業生產硫酸過程中的某一步反應用微觀模型圖表示如圖,下列說法正確的是( )
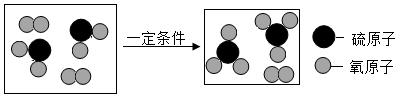
A.該反應是置換反應 B.該反應生成了三氧化硫和氧氣 C.該反應中兩種生成物的個數比是2:1 D.該反應中兩種反應物的質量比為4:1 組卷:32引用:2難度:0.5 -
3.下列人體所必須的元素中,缺乏或過量都會引起甲狀腺腫大的是( )
A.鈣 B.鐵 C.碘 D.硒 組卷:210引用:8難度:0.7 -
4.有Mg、Al、Zn的混合物共3.6g,與足量鹽酸反應,生成H2的質量可能是( )
A.0.1g B.0.3g C.0.4g D.0.5g 組卷:243引用:4難度:0.5 -
5.下列不屬于凈水方法的是( )
A.電解 B.沉淀 C.吸附 D.過濾 組卷:50引用:5難度:0.8 -
6.生活中一些常見物質的pH如下表,其中堿性最強的是( )
物質 廁所清潔劑 蒸餾水 肥皂水 爐具清潔劑 pH 2 7 10 12 A.廁所清潔劑 B.蒸餾水 C.肥皂水 D.爐具清潔劑 組卷:29引用:4難度:0.7 -
7.用水和適量洗滌劑或在油漬處涂抹汽油,均可去除衣服上沾有的油漬,原因是( )
A.加入洗滌劑后,使油漬溶于水 B.加入洗滌劑后,發生乳化,使油漬均勻地分散在水中 C.涂抹汽油后,吸附了油漬 D.涂抹汽油后,使油漬和汽油充分反應,瓦解油漬 組卷:261引用:11難度:0.9 -
8.2.8g某有機物充分燃燒,生成8.8g CO2和3.6g H2O,則有關該有機物組成的說法中正確的是( )
A.一定含有碳、氫、氧三種元素 B.一定含有碳、氫兩種元素,可能含有氧元素 C.一定含有碳、氫兩種元素,不含有氧元素 D.無法確定 組卷:50引用:2難度:0.5 -
9.下列知識整理的內容不正確的一組是( )
A 空氣是寶貴的資源 B 實驗操作安全常識 氮氣一填充食品袋防變質
氧氣一用于醫療急救
稀有氣體一制作霓虹燈不可將鼻孔湊到容器口去聞藥品氣味
不可觸摸藥品和品嘗味道
停止加熱時,不要用嘴吹滅酒精燈C 加熱時試管破裂原因 D 空氣中氧氣含量小于 的原因15加熱前一沒有給試管預熱
加熱時一試管底部接觸燈芯
加熱后一立即用冷水沖洗裝置氣密性不好
藥品(紅磷)不足
點燃紅磷伸入集氣瓶后沒有立即蓋好瓶塞A.A B.B C.C D.D 組卷:6引用:2難度:0.7 -
10.下列對“化學與生活、環境”的認識,科學的是( )
A.廚房燃氣泄漏,迅速打開排氣扇 B.加大燃煤發電,保障電力供應 C.催化處理尾氣,減輕空氣污染 D.大量使用農藥和化肥,提高農作物產量 組卷:27引用:2難度:0.7 -
11.請你用所學化學知識判斷下列做法符合安全要求的是( )
A.家用電器著火,立即用水澆滅 B.發現煤氣泄漏,立即打開抽油煙機排氣 C.為了防止CO中毒,在火爐旁放一盆水 D.遭遇火災時,要用濕毛巾住口鼻逃離著火區域 組卷:23引用:10難度:0.5 -
12.下列物種中,屬于有機合成材料的是( )
A.棉花 B.塑料 C.羊毛 D.蠶絲 組卷:41引用:3難度:0.9 -
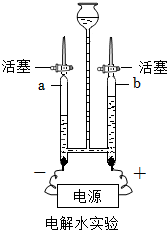 13.如圖所示為電解水的實驗裝置圖,下列說法正確的是( )
13.如圖所示為電解水的實驗裝置圖,下列說法正確的是( )A.由該實驗得出生成氫氣和氧氣的質量比為2:1 B.a管內產生的氣體能使帶火星的木條復燃 C.該實驗說明水由氫氣和氧氣組成 D.兩電極上均產生氣泡,a、b兩管內氣體的體積比約為2:1 組卷:77引用:5難度:0.8 -
14.氫氣密度比空氣小,難溶于水,以下收集氫氣的方法不正確的是( )
A. 
B. 
C. 
D.  組卷:76引用:1難度:0.8
組卷:76引用:1難度:0.8
二、非選擇題:本題包括6小題,共48分。
-
15.(1)化學與生產生活聯系緊密。現有:A.金剛石 B.硝酸鈉 C.熟石灰 D.稀硫酸,選擇適當的物質填空(填字母序號)。
①農業上可以用作肥料的是。
②能夠用來截玻璃的是。
(2)濕衣服在陽光下比在陰涼處干得快,這是因為(用分子的觀點解釋)。
(3)發生森林火災時,在大火蔓延路線前砍掉一片樹木,形成隔離帶,其滅火原理是。
(4)生活中熱水瓶用久后,瓶膽內壁常附著一層水垢【主要成分為CaCO3和Mg(OH)2】,可以用鹽酸來洗滌,寫出其中發生的中和反應(方程式表示)。組卷:30引用:1難度:0.8 -
16.金屬及金屬材料在生產、生活中應用廣泛。
早在春秋戰國時期,我國就開始生產和使用鐵器。煉鐵原理是利用一氧化碳與氧化鐵在高溫條件下反應,該反應的化學方程式為。現有CO和CO2的混合物氣體共36g,通過足量的灼熱的氧化銅,充分反應后,得到氣體的質量為44g,則原混合氣體中碳元素和氧元素的質量比是。組卷:13引用:2難度:0.6 -
17.綜合題
(一)鐵材料的有關知識
(1)人類使用金屬先后經歷了“青銅”、“鐵器”時代,到近代才開始大量使用鋁材料。這也反映出Cu、Fe、Al三種金屬的活動性由強到弱的順序是。
(2)在西漢時期就有“曾青得鐵則化為銅”之說,用化學方程式表示其原理。
(3)鋼鐵露置在空氣中易生銹,寫出一種防止鋼鐵生銹的方法。
以下是同學對鐵銹的成分、鐵銹制草酸亞鐵晶體及草酸亞鐵晶體熱分解的研究。
(二)用上述鐵銹制草酸亞鐵晶體(FeC2O4?nH2O)
資料:①FeSO4遇到氧氣氧化,會轉化為Fe2(SO4)3 .
②FeSO4的溶解度如下表:
【制備流程】溫度/℃ 0 10 30 50 60 70 80 90 溶解度/g 14.0 17.0 25.0 33.0 35.3 33.0 30.5 27.0 
(1)溶液加入過量鐵粉,發生的反應有:2Fe+Fe2(SO4)3=3FeSO4、。
充分反應后要趁熱過濾的目的是。
(2)流程中產生草酸亞鐵晶體反應的化學方程式為。
(3)制備過程中,溶液中通入氮氣的作用是。
(三)探究FeC2O4?nH2O熱分解的產物及n的值
【實驗裝置】
資料:①FeC2O4?nH2O為淡黃色粉末;FeO和Fe3O4都是黑色固體,其中FeO易被氧氣氧化。
②FeC2O4?nH2O加熱至300℃完全失去結晶水;繼續加熱至400℃,剩余固體受熱分解產生黑色固體、CO2和CO。
【實驗分析】
(1)若通過E裝置中澄清石灰水變渾濁來證明草酸亞鐵晶體熱分解產生CO,則需在B和C裝置之間增加盛有(填試劑名稱)的洗氣瓶。
(2)先鼓入氮氣,再加熱分解裝置的原因是。
3)指出上述實驗裝置不足之處。
(4)取3.60gFeC2O4?nH2O,按上述實驗步驟進行實驗,測得熱分解裝置中固體質量隨溫度變化曲線如圖所示:
①FeC2O4?nH2O中n的值為。
②反應后,熱分解裝置中殘留的黑色物質為(填化學式)。
③草酸亞鐵晶體受熱分解的方程式為。
④若將圖中1.44g固體在空氣中充分加熱,固體增加0.16g,此固體(鐵的氧化物)為。組卷:196引用:2難度:0.2 -
18.工業煙氣脫硫就是將煙氣中含有的二氧化硫除去,“雙堿法“脫硫的工業流程示意圖如圖【提示:SO2對應的酸是亞硫酸(H2SO3)】。分析流程回答下列問題:

(1)吸收塔中,發生反應的化學方程式為,該設備中有利于充分吸收SO2的做法是。
(2)沉淀室中,發生反應的基本類型是。
(3)整個流程中發生化合價變化的元素是,可以循環利用的物質是。組卷:94引用:1難度:0.5 -
 19.某化學興趣小組開展的酸、堿、鹽性質系列探究活動。
19.某化學興趣小組開展的酸、堿、鹽性質系列探究活動。
【探究1】變色實驗
(1)將鹽酸加入到紫色石蕊溶液中,觀察溶液變為紅色,將氫氧化鈉加入到無色酚酞溶液中,溶液變成色。由此得出:酸、堿溶液能使指示劑變色。
(2)將碳酸鈉加入到無色酚酞溶液中,溶液變成紅色,說明碳酸鈉溶液呈性。(填“酸”、“堿”或“中”)。
【探究2】配制溶液
(3)用98%濃硫酸來配制100g10%稀硫酸溶液,無需用到的玻璃儀器有(填標號)。
A.膠頭滴管
B.酒精燈
C.量筒
D.燒杯
E.玻璃棒
【探究3】酸堿中和反應微觀模擬示意圖:
(4)從微觀的角度分析,甲、乙兩處應填入的離子符號分別為。
(5)分析HCl和NaOH反應的實質,寫出該反應的本質:。
【探究4】
(6)如圖2實驗觀察到的現象是,說明堿溶液能與某些鹽反應。該反應的化學方程式為。
(7)自然界并不缺少鎂,缺少的是發現鎂的眼睛。某化學興趣小組開啟尋鎂之旅,現邀請你參與并完成相關內容。
①第一站:初識金屬鎂。①金屬鎂的物理性質:(寫一條);②金屬鎂的化學性質:鎂能與氧氣反應,反應的化學方程式為。
②第二站:再遇金屬鎂。將打磨過的鎂條放入稀鹽酸中,反應現象是,化學方程式為。
③第三站:制備金屬鎂。小組同學模擬工業上從海水曬鹽剩下的苦鹵中提取鎂,流程如下:苦鹵Mg(OH)2NaOHMgCl2→Mg,流程中X為X。
④第四站:再探金屬鎂。
【提出問題】鎂能否與熱水反應?如果反應,產物是什么?
【相關信息】①Mg+2H2O=Mg (OH)2+H2↑;②氫氧化鎂在熱水中能部分溶解實驗操作 實驗現象 實驗結論 鎂能與熱水反應,生成氫氧化鎂和氫氣 組卷:112引用:1難度:0.3 -
20.為了防止食品腐敗,在許多食品包裝盒中都有一包黑色粉末。這種粉末是一種除氧劑。該粉末沒有失效時呈黑色,失效后帶有紅棕色。為了確定成分,小明做出了以下的猜想:
【猜想】1.該粉末是木炭粉;
【猜想】2.該粉末是鐵粉;
【猜想】3.。
小明取沒有失效的該粉末,分別用不同的方法進行如下實驗,填寫表中空格:
【交流與反思】根據失效后的顏色判斷,該粉末失效的原因是試驗操作 實驗現象 猜想是否成立 實驗1 加入足量的硝酸銀溶液 猜想1:不成立 實驗2 加入足量的 猜想2:成立 實驗3 用磁鐵吸引 粉末被全部吸引 猜想3: ,變質后得到的紅棕色粉末的主要成分是(填物質的化學式)。
采用什么實驗方法可以使失效的粉末“再生”?(用化學方程式表示):。組卷:6引用:2難度:0.3


