2021-2022學年浙江省杭州市余杭區九年級(上)月考化學試卷(10月份)
發布:2025/6/30 1:0:8
一、選擇題(每小題3分,共60分,每小題只有一個選項最符合題意)
-
1.分析推理是化學學習中常用的思維方法。下列說法正確的是( )
A.根據質量守恒定律,1g氫氣與9g氧氣反應一定生成10g水 B.酸性溶液的pH<7,所以pH<7的溶液一定是酸性溶液 C.中和反應生成鹽和水,有鹽和水生成的反應一定是中和反應 D.洗滌劑去油污是利用了乳化作用,汽油去油污也是利用了乳化作用 組卷:19引用:2難度:0.6 -
2.有三瓶失去標簽的白色固體,分別是CaCO3、Na2CO3和NaCl,要把它們區分開來,應該選試劑或方法是( )
A.水 B.水和鹽酸 C.鹽酸 D.嘗味道 組卷:13引用:1難度:0.7 -
3.2022年吉林省糧食總產量達到816.16億斤,比上年增產8.32億斤。下列說法中錯誤的是( )
A.從外觀上可區別磷礦粉和硫酸鉀 B.化肥和農藥對農業高產有重要作用 C.NH4NO3不能與堿性物質混合使用 D.用NaOH改良酸性土壤 組卷:6引用:4難度:0.8 -
4.小燒杯中盛有某無色液體,向該燒杯中滴加2~3滴無色酚酞溶液并攪拌,燒杯中液體不變色,則下列結論正確的是( )
A.小燒杯中盛的一定是蒸餾水 B.小燒杯中盛的一定是稀鹽酸 C.小燒杯中盛的一定是NaOH溶液 D.小燒杯中盛的不可能是堿性溶液 組卷:263引用:5難度:0.9 -
5.學會識圖能發展科學思維。下列圖像與反應過程的變化趨勢對應正確的有( )
序號 ① ② ③ ④ 圖像 
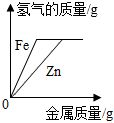


反應過程 KMnO4受熱分解 向含等質量HCl的稀鹽酸中分別加入Zn和Fe至過量 向NaOH溶液中逐滴加入稀鹽酸至過量 木炭在充滿O2的集氣瓶中燃燒 A.1個 B.2個 C.3個 D.4個 組卷:48引用:2難度:0.5 -
6.下面四個圖像的變化趨勢,分別對應四種操作過程,其中正確的是( )
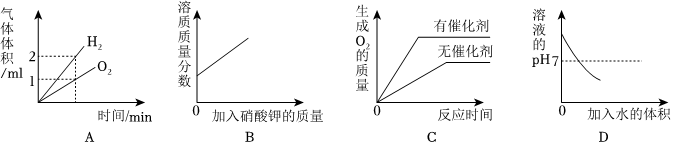
A.將水通電一段時間,相同狀況下產生氣體的體積變化 B.某溫度下,向一定量接近飽和的硝酸鉀溶液中不斷加入硝酸鉀晶體 C.用等質量的雙氧水制取氧氣 D.氫氧化鈉溶液加足量的水稀釋 組卷:41引用:2難度:0.6 -
7.化肥對提高農作物的產量具有重要作用。為了增強作物的抗倒伏能力,建議施用的化肥是( )
A.Ca(H2PO4)2 B.NH4HCO3 C.KCl D.CO(NH2)2 組卷:79引用:3難度:0.7 -
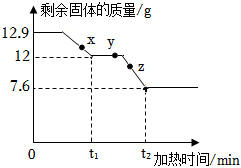 8.已知溫度高于350℃時,氫氧化鎂開始分解為氧化鎂和水,溫度高于850℃時,碳酸鈣開始分解。取12.9g兩者的混合物加熱,剩余固體質量隨時間變化如圖所示。下列說法錯誤的是( )
8.已知溫度高于350℃時,氫氧化鎂開始分解為氧化鎂和水,溫度高于850℃時,碳酸鈣開始分解。取12.9g兩者的混合物加熱,剩余固體質量隨時間變化如圖所示。下列說法錯誤的是( )A.由題可知碳酸鈣的熱穩定性優于氫氧化鎂 B.x點,剩余固體為MgO、Mg(OH)2和CaCO3 C.y點,剩余固體中鎂元素質量為1.2g D.若剩余固體中ωCa=36.0%,則剩余固體的成分為CaCO3和MgO 組卷:124引用:3難度:0.5 -
9.根據下列反應事實推理出的結論不正確的是( )
選項 化學反應事實 結論 A 二氧化碳與水反應生成碳酸,但在光照和葉綠體作用下生成氧氣 反應條件不同,產物不同 B 塊狀和粉狀石灰石與同體積濃度鹽酸反應時產生氣泡的速率不同 反應物接觸面積不同,反應快慢不同 C 硫在空氣中燃燒產生淡藍色火焰,在氧氣中燃燒產生藍紫色火焰 反應物濃度不同,反應現象不同 D 通常木炭充分燃燒生成二氧化碳,不充分燃燒生成一氧化碳 反應溫度不同,產物不同 A.A B.B C.C D.D 組卷:55引用:1難度:0.5 -
10.下列圖像能正確反映對應關系的是( )
A. 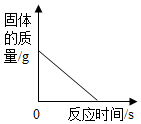
加熱氯酸鉀和二氧化錳的混合物B. 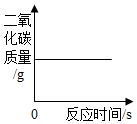
木炭在密閉的容器內燃燒C. 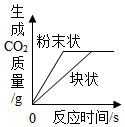
等質量CaCO3分別與足量等體積等濃度的稀鹽酸反應D. 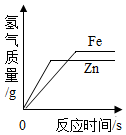
足量的鋅、鐵分別放入等質量等濃度的稀鹽酸中組卷:205引用:6難度:0.5 -
11.下列對實驗現象的描述正確的是( )
A.鐵絲在空氣中劇烈燃燒,火星四射,生成黑色固體 B.硫在空氣中燃燒產生微弱的淡藍色火焰,并生成無色無味的氣體 C.在軟水中滴入肥皂水會產生浮渣 D.向用石蕊溶液染成紫色干燥的紙花上噴稀醋酸,紙花變成紅色 組卷:87引用:3難度:0.9 -
12.下列試劑能將氯化鈉、碳酸鈉、氯化鋇三種溶液一次鑒別出來的是( )
A.鐵片 B.稀硫酸 C.氫氧化鈉溶液 D.石蕊試液 組卷:148引用:2難度:0.5 -
13.如圖為硫酸性質的知識歸納,下列表達不正確的是( )

A.若活潑金屬為鐵,可觀察到溶液變黃 B.若金屬氧化物為氧化銅,可觀察到溶液變藍 C.若指示劑為石蕊溶液,可觀察到溶液變紅 D.若堿為氫氧化鈉溶液,可以借助酚酞溶液,證明兩者發生了反應 組卷:193引用:2難度:0.7 -
14.下列說法正確的是( )
A.赤鐵礦不是金屬材料 B.酒精溶液的導電性很好 C.溶液中的溶劑只能是水 D.NH4NO3溶于水放熱使水的溫度升高 組卷:6引用:1難度:0.6 -
15.如圖是氫氧化鈉溶液與稀鹽酸恰好完全反應的微觀示意圖,下列結論正確的是( )
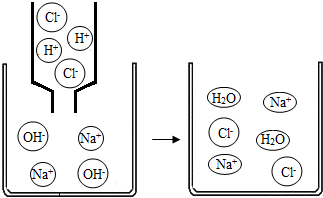
A.反應后溶液的pH大于7 B.反應前后原子種類發生了變化 C.反應后溶液中存在的粒子只有Na+和Cl- D.兩種溶液混合時,氫離子與氫氧根離子結合生成了水 組卷:34引用:2難度:0.6 -
16.下列實驗現象描述正確的是( )
A.點燃紅磷后,產生大量的白霧 B.二氧化碳氣體通入紫色石蕊試液中,溶液變藍色 C.澄清石灰水中滴加氯化鐵溶液,產生紅褐色沉淀 D.細鐵絲在氧氣中劇烈燃燒,火星四射,生成四氧化三鐵 組卷:30引用:2難度:0.7 -
17.下列實驗操作正確的是( )
A. 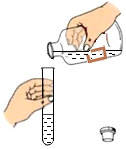
傾倒液體B. 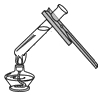
加熱液體C. 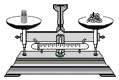
稱量固體D. 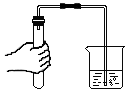
檢查氣密性組卷:17引用:10難度:0.9 -
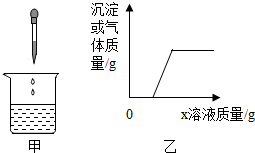 18.向燒杯中逐滴加入x溶液至過量(圖甲),生成沉淀或氣體的質量與加入x溶液的質量關系符合圖乙的是( )
18.向燒杯中逐滴加入x溶液至過量(圖甲),生成沉淀或氣體的質量與加入x溶液的質量關系符合圖乙的是( )燒杯中的物質 x溶液 A 稀鹽酸和硫酸銅溶液 燒堿溶液 B 稀硫酸和稀鹽酸 氯化鋇溶液 C 鎂鋁合金 稀鹽酸 D 氯化鈉和碳酸氫鈉溶液 稀鹽酸 組卷:560引用:76難度:0.7 -
19.關于中和反應的說法,錯誤的是( )
A.一定沒有沉淀生成 B.一定有氧化物生成 C.一定是放熱反應 D.一定是復分解反應 組卷:461引用:12難度:0.7 -
20.下列反應屬于復分解反應的是( )
A.CO+CuO Cu+CO2△B.HCl+NaOH═NaCl+H2O C.Zn+H2SO4═ZnSO4+H2↑ D.4P+5O2 2P2O5點燃組卷:68引用:6難度:0.9
二、填空題(每空2分,共54分)
-
21.某些鹽以結晶水形式存在,如CuSO4?5H2O、NiSO4?6H2O等.這些物質在受熱時會失去結晶水變為無水鹽,如CuSO4?5H2O加熱后失去結晶水而變為無水CuSO4.
(1)已知室溫時,NiSO4?6H2O為藍色,硫酸鎳為黃綠色.將NiSO4?6H2O加熱至280℃時,得黃綠色固體,請用化學方程式表示該化學反應過程:;反應的基本類型是;
(2)在硫酸鎳的水溶液中滴入兩滴紫色石蕊溶液,溶液變為紅色,則硫酸鎳的水溶液呈性;硫酸鎳屬于(填“酸”、“堿”、“鹽”).組卷:13引用:1難度:0.7 -
22.實驗室中有一包固體粉末可能含有NaCl、NaNO3、BaCl2、KNO3中的一種或幾種,為確定固體粉末的成分:①取少量樣品,加入足量水充分溶解,得到無色溶液;②向所得溶液中滴加足量稀硫酸,有白色沉淀產生,則該固體中一定含有的是
。組卷:4引用:2難度:0.6 -
23.通過海水晾曬可得粗鹽,粗鹽除 NaCl 外,還含有 MgCl2、CaCl2、Na2SO4以及泥沙等雜質.以下是制備精鹽的實驗方案,各步操作流程如圖:
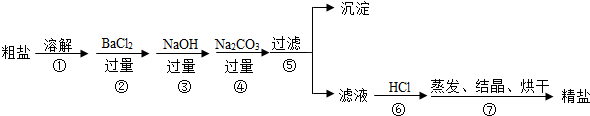
(1)在第①步粗鹽溶解操作中要用玻璃棒攪拌,作用是.
(2)第④步操作加入過量的 Na2CO3目的是除去(填化學式).
(3)在第③步操作中,選擇的除雜的試劑不能用 KOH 代替 NaOH,理由是.
(4)在利用粗鹽制備精鹽過程的第⑥步操作中,加入適量鹽酸的目的是.組卷:26引用:2難度:0.3 -
24.酸溶液
呈酸性,酸性溶液是酸溶液(填“一定”或“不一定”)組卷:9引用:1難度:0.9 -
25.如圖為加熱“銅綠”的實驗裝置圖,試回答下列問題:
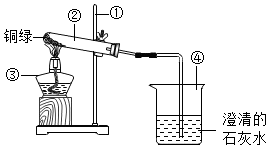
(1)指出有關儀器的名稱:
①②③④
(2)加熱后,觀察到的現象是。
(3)試分析在實驗時試管破裂的原因有哪些?寫出三條。組卷:7引用:1難度:0.5 -
26.在化學實驗中,有時藥品的滴加順序不同會導致實驗現象不同。某同學使用圖甲所示實驗裝置進行實驗,廣口瓶內氣球的體積變化與滴加藥品體積的關系如圖乙所示,其中 A 點表示開始滴加某種藥品,B 點表示開始滴加另一種藥品(不考慮由于滴入液體的體積 及反應導致的溫度變化對集氣瓶內氣壓的影響)。據圖回答:
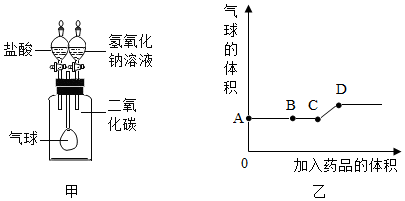
(1)實驗中首先加入試劑是。
(2)試從加入藥品的種類、順序及發生的化學反應等角度來解釋氣球體積的變化情況。組卷:581引用:6難度:0.5 -
27.某溶液中可能含有以下幾種離子Na+、Ca2+、Ba2+、Cl-、
、SO2-4中的幾種,為確定溶液中含有的離子,進行以下實驗探究:CO2-3
①取少量未知溶液,滴加AgNO3溶液產生白色沉淀;
②另取少量未知溶液,加入足量的Ba(NO3)2溶液,產生白色沉淀,靜置過濾,向沉淀中加入過量的稀硝酸,沉淀部分溶解。
請你根據實驗現象,推測:
(1)原溶液中一定含有的離子為(填符號,下同),一定不存在的離子為。
(2)為驗證可能存在的離子,你設計的實驗方案為。組卷:77引用:2難度:0.6 -
28.某推銷員這樣向你推銷他的產品“我廠生產的濃鹽酸質優價廉,濃度高達90%…”,你會買他的鹽酸嗎?
為什么?.組卷:53引用:3難度:0.7 -
29.(1)用化學方程式解釋下列問題:工業上用稀鹽酸除去鐵制品表面的鐵銹(鐵銹的成分Fe2O3)
;
(2)電解水實驗中,在水中加入稀硫酸或氫氧化鈉的作用是增強水的導電性,在電源的負正兩極分別產生和,其體積比是.組卷:11引用:1難度:0.7
三、實驗探究題(每空2分,共30分)
-
30.實驗室經常需要將濃硫酸稀釋成稀硫酸,稀硫酸是化學反應的常用的藥品。
(1)20℃時,在實驗室用98%的濃硫酸配制20%的硫酸溶液:
①若要配制49g質量分數為20%硫酸,所需要水的質量為g。
②用到的儀器有:燒杯、玻璃棒和。(填儀器的序號)
A.托盤天平(帶砝碼盒) B.藥匙 C.膠頭滴管
D.200mL量筒 E.50mL量筒 F.10mL量筒
③從下表中找出稀釋過程需要用到的數據:g/cm3。
硫酸溶液的密度(單位:g/cm3)
(2)為探究98%的濃硫酸和20%的稀硫酸的性質差別,某同學進行了如圖1實驗:質量分數/% 10℃ 20℃ 30℃ 20% 1.145 1.139 1.133 98% 1.846 1.836 1.826 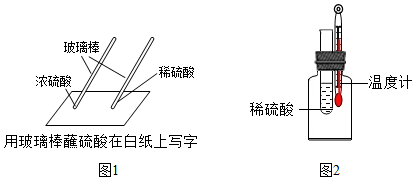
該同學觀察實驗現象是(填“濃”或“稀”)硫酸使白紙炭化,說明即使是同種酸,由于不同,它們的性質不完全相同。
(3)某化學學習小組研究硫酸的性質,將20%硫酸溶液放入試管中,如圖2所示(裝置氣密性良好),再向試管中加入某物質后,溫度計溫度升高,該物質是。
A.鋅粒 B.冰塊 C.銅塊
D.氯化鈉 E.氫氧化鈉。組卷:166引用:2難度:0.3 -
31.硝酸鈣的營養液可用于無土栽培。工業上,常用石灰石為原料制取硝酸鈣,具體流程如圖:
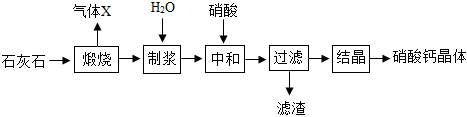
(1)“煅燒”步驟產生的氣體X是。
(2)“制漿”時須控制好加水的量。加水太少導致制漿困難,加水太多會導致。
(3)“中和”步驟發生反應的化學方程式:。組卷:14引用:4難度:0.5 -
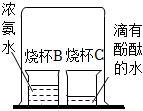 32.圖為“探究微粒運動的實驗”裝置圖。
32.圖為“探究微粒運動的實驗”裝置圖。
(1)燒杯B中氨水的濃度變(選填“大”或“小”)。
(2)燒杯C中的現象為。組卷:54引用:4難度:0.8 -
 33.為了測定某牛奶樣品中蛋白質的含量,現采用“蓋爾達法”分解其中的蛋白質。其原理是把蛋白質中的氮元素完全轉化成氨氣(化學式為:NH3),再用稀硫酸吸收氨氣,反應的化學方程式:2NH3+H2SO4=(NH4)2SO4
33.為了測定某牛奶樣品中蛋白質的含量,現采用“蓋爾達法”分解其中的蛋白質。其原理是把蛋白質中的氮元素完全轉化成氨氣(化學式為:NH3),再用稀硫酸吸收氨氣,反應的化學方程式:2NH3+H2SO4=(NH4)2SO4
現取該牛奶樣品30mL,用“蓋爾達法”分解其中的蛋白質,產生的氨氣用A9.5g溶質質量分數為4.9%的稀硫酸恰好完全吸收。計算并回答下列問題:
(1)產生氨氣的質量是多少克?(計算結果精確到0.01g,下同)
(2)30mL牛奶中含氮元素的質量是多少克?
(3)下圖是該牛奶包裝標簽的部分內容。已知牛奶中的蛋白質含氮元素的質量分數為16%,請你通過計算確定,該牛奶樣品中蛋白質的含量是否達到了包裝標簽所標示的蛋白質的質量標準。組卷:15引用:3難度:0.5
四、分析與計算題(共16分)
-
34.某工廠廢液中含氫氧化鈉的質量分數為2%,用質量分數為9.8%的稀硫酸5t,將其恰好中和處理,處理的廢液質量是多少?(寫出計算過程)
組卷:60引用:1難度:0.5 -
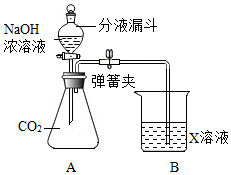 35.學習小組同學用如圖裝置進行實驗。打開分液漏斗的活塞,將NaOH濃溶液加入錐形瓶A中,關閉活塞,打開彈簧夾,觀察到A中產生白色沉淀,燒杯B中液面降低。
35.學習小組同學用如圖裝置進行實驗。打開分液漏斗的活塞,將NaOH濃溶液加入錐形瓶A中,關閉活塞,打開彈簧夾,觀察到A中產生白色沉淀,燒杯B中液面降低。
(1)寫出CO2與NaOH溶液發生反應的化學方程式:。
(2)若X是一種堿,其化學式可能是(只寫一種)。
(3)學習小組同學用的X是CaCl2,實驗結束后,同學們又分別做了以下三組實驗:
①取少量A中溶液,測其pH,pH>7
②取少量A中溶液,向其中加入CaCl2溶液,無明顯現象,再測其pH,pH>7
③取少量A中溶液,測其pH,pH>7,再向其中加入K2CO3溶液,產生白色沉淀
查閱資料可知CaCl2溶液呈中性。
以上三組實驗事實中,能說明A中溶液一定含有NaOH的是(填序號)。組卷:709引用:6難度:0.3


