2024-2025學年山東省濟寧市北湖區九年級(上)期中化學試卷
發布:2025/6/30 3:0:10
一、選擇題(每題只有一個正確答案。每題2分,共30分)
-
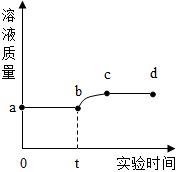 1.向一定量稀硫酸中加入一定量銅粉,無氣泡冒出;用導管向稀硫酸中通入空氣并加熱,銅粉逐漸減少,溶液由無色變為藍色,測得溶液質量與實驗時間的關系如圖。下列說法錯誤的是( )
1.向一定量稀硫酸中加入一定量銅粉,無氣泡冒出;用導管向稀硫酸中通入空氣并加熱,銅粉逐漸減少,溶液由無色變為藍色,測得溶液質量與實驗時間的關系如圖。下列說法錯誤的是( )A.ab段說明Cu不能置換出硫酸中的氫元素 B.從b點到c點,說明銅粉參與化學反應 C.從c點到d點,溶液中的溶質只有一種 D.bc段發生的反應為:2Cu+2H2SO4+O2 2CuSO4+2H2O△組卷:83引用:3難度:0.4 -
2.化學反應要符合一定的原理和條件,下列認識正確的是( )
A.化合反應和分解反應一定有單質參加或生成 B.置換反應只能發生在金屬與金屬的化合物之間 C.復分解反應要有沉淀或氣體或水生成 D.有鹽和水生成的反應一定是中和反應 組卷:94引用:12難度:0.9 -
3.下列物品屬于溶液的是( )
A.白醋 B.番茄醬 C.牛奶 D.蒸餾水 組卷:24引用:2難度:0.8 -
4.下列物質加入水中,不能形成溶液的是( )
A.味精 B.酒精 C.花生油 D.白糖 組卷:23引用:2難度:0.5 -
5.下列實驗操作中,能達到實驗目的的是( )
A.檢驗氫氣純度時,沒有聽到任何響聲,表明氫氣已純凈 B.用適量的水能區分硫酸鋇固體和氯化鋇固體 C.粗鹽提純實驗中,蒸發結晶直到濾液蒸干時停止加熱 D.用pH試紙測定溶液酸堿度時,先將pH試紙用水潤濕,然后再測定 組卷:7引用:1難度:0.9 -
6.在下列物質的溶液中,滴加氫氧化鈉溶液能產生藍色沉淀的是( )
A.CuSO4 B.HCl C.H2SO4 D.Na2CO3 組卷:13引用:1難度:0.7 -
7.現有5種物質:①濃鹽酸 ②燒堿 ③食鹽 ④濃硫酸 把它們長期露置在空氣中,其中發生化學變化且質量增加的是( )
A.①② B.② C.③④ D.③ 組卷:13引用:4難度:0.7 -
8.甲、乙兩種固體的溶解度曲線如圖所示。下列說法中,不正確的是( )
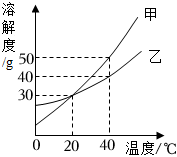
A.甲的溶解度隨溫度升高而增大 B.20℃時,甲、乙溶解度相等 C.將20℃時乙的飽和溶液升溫至40℃,溶液質量不變 D.40℃時,分別在100g水中加入40g甲、乙,所得溶液均為飽和溶液 組卷:149引用:3難度:0.8 -
9.已知某鹽在不同溫度下的溶解度如下表,若把溶質質量分數為32%的該鹽溶液,由50℃逐漸冷卻,則開始有晶體析出的溫度范圍是( )
溫度(℃) O 10 20 30 40 溶解度(g) 13.3 20.9 31.6 45.8 63.9 A.0℃~10℃ B.10℃~20℃ C.20℃~30℃ D.30℃~40℃ 組卷:232引用:11難度:0.9 -
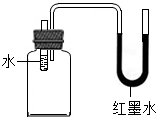 10.如圖所示裝置,向試管里的水中加入某種物質后,U形管右邊支管的紅墨水液面上升,左邊支管的紅墨水液面降低,則加入的物質可能是( )
10.如圖所示裝置,向試管里的水中加入某種物質后,U形管右邊支管的紅墨水液面上升,左邊支管的紅墨水液面降低,則加入的物質可能是( )A.氫氧化鈉溶液 B.硝酸銨 C.氯化鈉 D.濃硫酸 組卷:15引用:5難度:0.7 -
11.如圖所示實驗操作,正確的是( )
A. 
稱量固體氫氧化鈉B. 
稀釋濃硫酸C. 
測溶液pHD. 
干燥CO2組卷:112引用:10難度:0.7 -
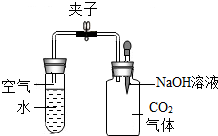 12.在如圖所示的裝置中,夾子處在關閉狀態。現將NaOH溶液滴入廣口瓶中,待充分反應后,打開夾子,試管中剛停止沸騰的水又重新沸騰了。對上述現象的是( )
12.在如圖所示的裝置中,夾子處在關閉狀態。現將NaOH溶液滴入廣口瓶中,待充分反應后,打開夾子,試管中剛停止沸騰的水又重新沸騰了。對上述現象的是( )A.試管內的氣壓減小,沸點升高 B.試管內的氣壓增大,沸點升高 C.試管內的氣壓減小,沸點降低 D.試管內的氣壓增大,沸點降低 組卷:69引用:7難度:0.7 -
13.將二氧化碳、生石灰、氯化鈉分別溶于水中,分別滴入紫色石蕊試液,溶液呈現的顏色依次為( )
A.紅色、藍色、無色 B.紅色、紫色、藍色 C.紅色、藍色、紫色 D.紫色、藍色、紅色 組卷:678引用:6難度:0.9 -
14.下列圖像不能正確反映對應變化關系的是( )
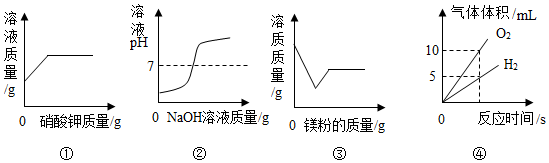
A.①室溫下,向一定量硝酸鉀的不飽和溶液中不斷加入硝酸鉀固體 B.②向一定量的稀鹽酸中不斷加入過量的NaOH溶液 C.③向一定量氯化亞鐵和氯化鋁的混合溶液中不斷加入鎂粉至過量 D.④將一定量的水通電分解一段時間 組卷:199引用:7難度:0.5 -
15.分析推理是化學學習中常用的思維方法。下列分析正確的是( )
A.堿溶液顯堿性,所以顯堿性的溶液一定是堿溶液 B.CO2和CO的分子構成不同,所以它們的化學性質一定不同 C.單質中含有一種元素,所以含一種元素的物質一定是單質 D.酸雨的pH小于7,所以pH小于7的雨水一定是酸雨 組卷:25引用:1難度:0.6
二、填空與簡答(共36分)
-
 16.2008年北京奧運會火炬的燃料是丙烷,丙烷的分子模型如圖所示:
16.2008年北京奧運會火炬的燃料是丙烷,丙烷的分子模型如圖所示:
(1)丙烷的化學式是;
(2)一個丙烷分子中有個原子;
(3)丙烷完全燃燒后生成水和二氧化碳,試寫出丙烷完全燃燒的化學方程式.組卷:27引用:14難度:0.9 -
17.多角度認識物質,能幫助我們更全面了解物質。
(一)性質活潑的氧氣
(1)工業制取氧氣的原料是空氣。空氣中主要組分的沸點如下表,根據空氣中液氧和液氮的不同加以分離得到氧氣。
(2)揭開盛有液態空氣的保溫瓶蓋,并將燃著的木條置于瓶口上方,觀察到組分 氮氣 氧氣 沸點(℃) -196 -183 (填字母)。
A.木條熄滅B.木條燃燒更旺C.木條先熄滅,后燃燒更旺
(二)奇妙的二氧化碳
(3)燒杯內有燃著的兩支高低不同的蠟燭,沿著燒杯慢慢地傾倒CO2,觀察到的現象是,說明CO2的化學性質有,所以CO2可用于。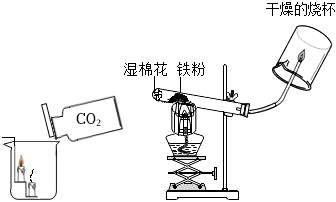
(三)收獲之旅
(4)在常溫下,鐵易生銹,是因為鐵與水、O2反應生成色的鐵銹。
但在高溫下,鐵與水蒸氣能反應生成一種常見鐵的氧化物和一種氣體。乙同學設計了如上圖所示的實驗,探究鐵粉與水蒸氣反應后的產物。
(5)①試管尾部放一團濕棉花的目的是。
②探究生成的氣體是什么?
待氣體驗純后點燃,觀察到管口有淡藍色火焰,將干燥的冷燒杯倒罩在火焰上方,燒杯內壁出現水霧。說明生成的氣體是。
③探究試管中剩余固體成分是什么?
【查閱資料】
【初步驗證】試管中剩余固體為黑色,能全部被磁鐵吸引。鐵與常見鐵的氧化物 Fe粉 FeO Fe2O3 Fe3O4 顏色、狀態 黑色粉末 黑色粉末 紅棕色粉末 黑色晶體 能否被磁鐵吸引 能 否 否 能 能否溶于稀鹽酸 能溶,冒氣泡 能溶,無氣泡 能溶,無氣泡 能溶,無氣泡
【猜想假設】猜想1:剩余固體是Fe3O4;猜想2:剩余固體是。
【實驗探究】丙同學取樣品于試管中,滴加稀鹽酸,發現固體全部溶解,有氣泡冒出,丙同學認為猜想正確。
【實驗結論】鐵和水蒸氣反應化學式表達式為。組卷:34引用:2難度:0.5 -
18.為探究Fe、Cu、Ag的金屬活動性強弱,某興趣小組做了如下實驗:
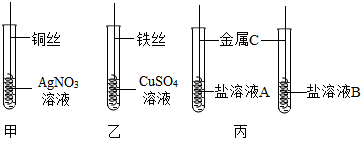
(1)實驗前需將金屬絲打磨,目的是。
(2)甲實驗中發生反應的化學方程式為;乙實驗中觀察到的現象為。
(3)通過甲、乙實驗探究,可得出三種金屬活動性由強到弱的順序為。
(4)若采用丙實驗方案也可得出相同結論,則金屬C是,A溶液與B溶液分別是和。
(5)如果只用兩種金屬絲和一種溶液,來探究三種金屬的活動性強弱,則所需要的金屬和溶液分別是。組卷:195引用:4難度:0.5 -
19.閱讀材料,回答問題。
出現新冠病毒以來,過氧乙酸作為高效消毒劑而被廣泛使用。過氧乙酸(化學式為CH3COOOH)在常溫下是一種無色有刺激性氣味的液體,易揮發。它對呼吸道黏膜有刺激性,高含量的過氧乙酸溶液對皮膚有腐蝕性。商品過氧乙酸是40%的醋酸溶液,使用前通常先用蒸餾水等將其稀釋,消毒時可用噴霧法消毒,也可將其配制成0.2%的水溶液洗手消毒。過氧乙酸不穩定,易分解生成無毒物質,若用噴霧法消毒,過氧乙酸在半小時內就可完全分解。
(1)過氧乙酸是(填“無機化合物”或“有機物”)。
(2)在過氧乙酸溶液中,溶劑是(寫化學式)。
(3)分別指出過氧乙酸的物理性質和化學性質(各寫一點即可)。
物理性質:,化學性質:。
(4)100g溶質質量分數為0.2%的過氧乙酸洗手液中,含過氧乙酸g。
(5)在稀釋40%的醋酸溶液時應注意的是。組卷:10引用:2難度:0.6 -
20.我國航空航天事業取得令人矚目的成就,閱讀以下相關主題科普材料,回答問題。
材料一:神舟十三號載3名宇航員在太空執行任務,時長180天,空間站中常用水氣整合系統實現CO2的清除和O2的再生(簡易流程如圖),科學家通過縝密計算,為了提供3名宇航員在太空生活所需的O2,至少需從地球帶486kg的水進行電解。
材料二:我國探月工程實現“六戰六捷”。未來還將探索在月球建設基地的可能,其中一個前提就是在月球上大規模制造O2,在月球上可以電解熔融月壤(含SiO2、FeO、CaO、Al2O3等)制造氧氣。
(1)分析材料一流程可知,可循環利用的化合物有(填物質的化學式),航天員呼吸屬于緩慢過程,并熱量。
(2)請計算電解486kg水能產生氧氣的質量(填寫具體計算過程)。
(3)月壤成分CaO中含氧的質量分數為%(結果保留小數點后一位)。理論上,電解等質量的下列氧化物,產生氧氣最多的是。
A.SiO2
B.FeO
C.CaO組卷:117引用:2難度:0.5
三、實驗與探究(共22分)
-
21.氫氧化鈉有強腐蝕性,用天平稱量固體氫氧化鈉時要用容器盛裝才能稱量,若用質量為23.1g的小燒杯作容器,在托盤天平上稱取質量為40g的氫氧化鈉固體。
(1)標尺上游碼的位置有A、B、C三種指示,正確的是。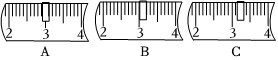
(2)如圖是某學生在稱量氫氧化鈉固體時使用天平的操作示意圖,指出其中的錯誤: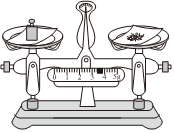
①、②。組卷:11引用:1難度:0.8 -
22.溶液與人類生產、生活密切相關。
(1)把下列物質分別放入水中,充分攪拌,不能得到溶液的是(填字母序號)。
A.氯化鈉
B.蔗糖
C.酒精
D.面粉
(2)圖1為甲、乙、丙均不含結晶水的三種固體物質在水中的溶解度曲線。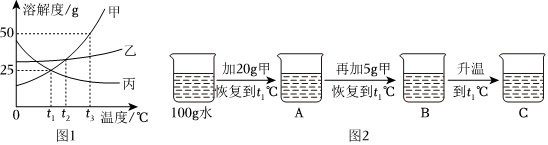
①t2℃時,甲、乙兩種物質的溶解度(填“相等”或“不相等”)。
②甲物質中混有少量的乙物質,若提純甲物質,常采用的結晶方法是。
③某同學在t1℃時開始如圖2實驗,得到相應的溶液A、B、C,在溶液A、B、C中,屬于飽和溶液的是(填字母序號);在溶液C中再加入30g甲后,充分攪拌,恢復到t3℃,所得溶液中溶質質量分數為(結果精確到0.1%)。
(3)甲、乙、丙三種固體物質的溶解度曲線如圖所示,下列說法正確的是。
A.丙溶解度隨溫度升高而增大
B.將t3℃時甲、丙的飽和溶液分別降溫至t1℃,甲成為不飽和溶液
C.t3℃時,用等質量的甲、丙分別配制成飽和溶液,所得溶液的質量甲>丙
D.t3℃時,將150g甲的飽和溶液稀釋成質量分數為20%的溶液,需水的質量為100g組卷:101引用:2難度:0.5
四、分析與計算(共12分)
-
23.化學在生產和生活中應用廣泛,請用化學方程式解釋下列原理:
(1)實驗室用酒精作燃料。
(2)正常雨水的pH值約為5.6的原因。組卷:12引用:2難度:0.6 -
24.取34g過氧化氫溶液過氧化氫和水的混合物和2g二氧化錳(難溶于水)混合制取氧氣,充分反應后,稱量剩余液體和固體的總質量為34.4g。請計算:
(1)充分反應后,生成氧氣的質量為g。
(2)被分解的過氧化氫的質量。(按格式寫出具體計算過程)組卷:173引用:3難度:0.8


