2024年重慶市中考化學試卷(A卷)
發布:2025/7/1 23:0:8
一、選擇題(本大題包括16個小題,每小題2分,共32分)每小題只有一個選項符合題意。
-
1.2011年央視《每周質量報告》的3?15特別節目曝光:河南生豬主產區采用違禁藥品瘦肉精,有毒豬肉流向雙匯分公司.“瘦肉精”的化學式C12H19Cl3N2O,則下列有關瘦肉精的說法中不正確的是 ( )
A.瘦肉精分子中含有氮分子 B.瘦肉精中碳元素的質量分數最大 C.瘦肉精是有機物 D.瘦肉精由碳、氫、氧、氯、氮五種元素組成 組卷:10引用:5難度:0.7 -
2.空氣中,稀有氣體的體積分數約為( )
A.0.03% B.78% C.21% D.0.94% 組卷:67引用:3難度:0.7 -
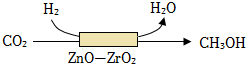 3.《科學》刊登了用CO2為原料。不依賴光合作用人工合成淀粉的成果,其中第一步反應如圖所示。下列說法正確的是( )
3.《科學》刊登了用CO2為原料。不依賴光合作用人工合成淀粉的成果,其中第一步反應如圖所示。下列說法正確的是( )A.該反應為置換反應 B.反應前后分子數目不相等 C.反應前后原子數目不相等 D.反應前后ZnO-ZrO2的質量不相等 組卷:414引用:14難度:0.6 -
4.下列有關物質的用途和性質之間的關系相符的是( )
A.因為氧氣具有助燃性,因此可用作燃料 B.金剛石用于切割玻璃是因為金剛石化學性質穩定 C.稀有氣體可用作保護氣是因其化學性質穩定 D.氫氣是未來最清潔的能源之一,因為相同條件下氫氣的密度最小 組卷:8引用:1難度:0.6 -
5.下列說法正確的是( )
A.10%的食鹽溶液是指100g水中溶解了10g食鹽 B.某物質只含有一種元素,則該物質不可能是混合物 C.世界是由物質組成的,物質都是由分子和原子構成 D.生鐵和鋼是含碳量不同的鐵的兩種合金 組卷:23引用:1難度:0.9 -
6.我國的海洋國土面積有300萬平方公里。海水中含量最多的元素是( )
A.氫元素 B.氧元素 C.鋁元素 D.鈉元素 組卷:54引用:4難度:0.6 -
7.下列相關制作過程中一定發生了化學變化的是( )
A.玉器雕琢 B.骨笛打孔 C.金筒刻字 D.彩陶燒制 組卷:19引用:1難度:0.8 -
8.下列有關玻璃棒作用的描述錯誤的是( )
A.過濾時:引流 B.測溶液pH時:蘸取 C.搗碎固體時:研細 D.加速固體溶解時:攪拌 組卷:73引用:12難度:0.7 -
9.下列實驗操作能達到相應實驗目的的是( )
實驗目的 實驗操作 A 除去CO2中的少量CO 點燃 B 鑒別CuO粉末和木炭粉 觀察顏色 C 鑒別H2和CH4 分別點燃,在火焰上方罩一干冷燒杯 D 鑒別雙氧水和蒸餾水 取樣,分別加入二氧化錳 A.A B.B C.C D.D 組卷:68引用:4難度:0.5 -
 10.2023年9月21日,天宮課堂第四課在夢天艙上進行授課。夢天艙載有世界上第一套由冷原子鍶光鐘等組成的空間冷原子鐘。鍶元素(5個電子層)在元素周期表中的信息與鍶離子(Sr2+)結構示意圖如圖所示,下列說法正確的是( )
10.2023年9月21日,天宮課堂第四課在夢天艙上進行授課。夢天艙載有世界上第一套由冷原子鍶光鐘等組成的空間冷原子鐘。鍶元素(5個電子層)在元素周期表中的信息與鍶離子(Sr2+)結構示意圖如圖所示,下列說法正確的是( )A.m=38,x=2 B.鍶原子的質量為87.62 C.易失去2個電子 D.鍶離子有5個電子層 組卷:21引用:1難度:0.6 -
11.下列表示兩個氫原子的是( )
A.H2 B.2H C.2H+ D.H2O 組卷:58引用:4難度:0.6 -
12.下列對生活中的一些現象解釋錯誤的是( )
A.“遙知不是雪,為有暗香來”,因為分子在不斷地運動 B.喝汽水時容易打嗝,因為氣體的溶解度隨溫度升高而減小 C.吃松花蛋時可加入少量食醋,因為食醋能消除蛋中所含堿性物質的澀味 D.鐵制品比鋁制品易銹蝕,因為鐵的活動性比鋁強 組卷:12引用:2難度:0.7 -
 13.如圖是鐵元素在元素周期表中的部分信息及原子結構示意圖。下列有關鐵的說法不正確的是( )
13.如圖是鐵元素在元素周期表中的部分信息及原子結構示意圖。下列有關鐵的說法不正確的是( )A.鐵原子中質子數為26 B.鐵原子在化學反應中易失去電子 C.生鐵的含碳量比鋼的含碳量高 D.鐵與稀鹽酸反應的產物為FeCl3和H2 組卷:70引用:4難度:0.6 -
14.2023年世界環境日中國主題為“建設人與自然和諧共生的現代化”。下列做法與這一主題不相符的是( )
A.使用新能源公交車 B.垃圾分類處理 C.積極參與植樹造林 D.直接排放生活污水 組卷:6引用:5難度:0.7 -
15.“鹵汁豆腐干”是蘇州特產。豆制品所含的主要營養物質是( )
A.糖類 B.油脂 C.蛋白質 D.維生素 組卷:211引用:4難度:0.7 -
16.化學與生活息息相關。下列說法中,不合理的是( )
A.熟石灰常用于改良酸性土壤 B.二氧化碳大量排放會形成酸雨 C.液氯可用于自來水的殺菌消毒 D.甲醛、重金屬離子會使人體中毒 組卷:7引用:1難度:0.5
二、填空題(本大題包括5個小題,共21分)
-
17.化學就在我們身邊,人類的生產、生活離不開化學。請運用化學知識回答下列問題:
(1)請從下列物質中選擇合適的物質代號填空。
A.干冰 B.可燃冰 C.C60
①可以用于超導領域的是;
②可以用于人工降雨的是;
③我國從海底開采的新能源是。
(2)家里長時間使用井水后的燒水壺出現了大量的水垢,小華認為該水是(填“硬水”或“軟水”),若要證明小華的猜想是否正確,可以使用進行檢驗。
(3)重鉻酸鉀在鞋業上可供鞣革之用,鉻是一種有毒的重金屬,一些不法分子將回收的膠鞋提煉出的工業明膠用作藥用膠囊,危害人體健康。該物質在高溫下反應的化學方程式:4K2Cr2O74R+2Cr2O3+3O2↑,R物質的化學式是高溫。
(4)低碳,意指較低(更低)的溫室氣體排放。這里的溫室氣體主要指的是。組卷:32引用:3難度:0.5 -
 18.中國古代化學和化學工藝歷史悠久、成就卓越,是勞動人民生產、生活智慧的結晶。
18.中國古代化學和化學工藝歷史悠久、成就卓越,是勞動人民生產、生活智慧的結晶。
(1)下列成就不屬于我國古代化學工藝成就的是(填序號)。
①青銅器的制造
②納米技術
③火藥的發明
④指南針的使用
⑤陶瓷的燒制
(2)《夢溪筆談》記載“熬膽礬鐵釜久亦化為銅”,膽礬溶于水主要成分是硫酸銅,請寫出該過程發生的化學反應方程式。
(3)西晉《蜀都賦》中有“火井沈熒于幽谷,高焰飛煽于天垂,”描寫的是天然氣燃燒時的現象,天然氣屬于(選填“可再生”或“不可再生”)能源。
(4)如圖是古代煉鐵郵票,它顯現了古代我國金屬冶煉技術,畫中是生、熟煉鐵爐,原理跟現代高爐煉鐵相似,中部是古代編鐘,編鐘一般用青銅鑄造。
①從制作編鐘的材料角度看,青銅是(填“金屬”或“合成”)材料;
②從泥爐中流淌出的“墮子鋼”,實際是現代所指的(填序號)。
A.純鐵
B.鋼
C.生鐵組卷:21引用:2難度:0.5 -
19.氨氣極易溶于水,它的水溶液叫氨水,氨水呈堿性,是一種速效肥料.
(1)實驗室可用加熱氯化銨和消石灰的固體混合物來制取氨氣,生成物除氨氣外,還有氯化鈣和水,該化學方程式為,收集氨氣的方法是.
(2)請列舉分別屬于氮肥、磷肥、鉀肥和復合肥個一種.、、、.組卷:10引用:1難度:0.5 -
20.為了提高原料的利用率,現從含有金屬鎂、鐵、銅的粉末中分離和提取出重要化工原料MgSO4和有關金屬,實驗過程如下:請回答:
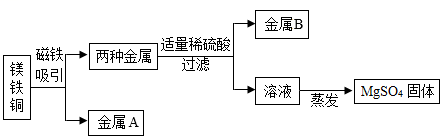
(1)金屬B是。
(2)寫出上述實驗過程中發生反應的化學方程式。組卷:86引用:2難度:0.8 -
21.如圖1所示是以空氣為主要原料合成碳酸氫銨(NH4HCO3)的流程.
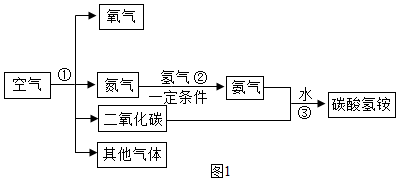
(1)現代工業常利用氮分子大于氧分子的特性,使用特制的分子篩把空氣中的氧氣分離出來,此過程屬于(選填“物理”、“化學”)變化.
(2)如圖2可以表示步驟②的反應過程: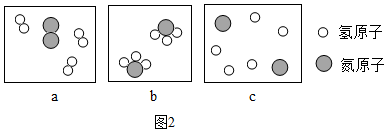
①從反應開始到完成的排列順序為(填字母).
②根據圖2信息判斷,氨氣的化學式可能為.
③寫出步驟②所表示的反應的文字表達式.
(3)步驟③的反應屬于(填基本反應類型).
(4)請根據碳酸氫銨(NH4HCO3)的化學式進行計算:
①NH4HCO3的相對分子質量為.
②NH4HCO3中氮、氫、碳、氧四種元素的質量比.
③158kg NH4HCO3中含氮元素的質量.(寫出計算過程)
(6)如圖3是某種化肥的標簽,根據標簽有關信息,下列說法正確的有.
A.含氮量的“氮”是指元素
B.該化肥易溶于水,受熱易分解
C.該化肥是由四種元素組成的純凈物
D.通過計算可判斷該化肥為混合物組卷:30引用:1難度:0.5
三、實驗題(本大題包括2個小題,共11分)
-
22.學習了二氧化錳對過氧化氫分解有催化作用的知識后。某同學從新聞報道中得知有一種黑色粉末廢鉑碳也能做催化劑,現在市場上正在高價回收,他想:廢鉑碳真的能起到類似二氧化錳的催化作用嗎?于是該同學在老師和同學的幫助下找到了一些廢鉑碳進行了以下探究。
【猜想】
Ⅰ.廢鉑碳不是催化劑,也不參與反應,反應前后質量和化學性質不變;
Ⅱ.廢鉑碳參與反應產生氧氣,反應前后質量和化學性質發生了變化;
Ⅲ.廢鉑碳是反應的催化劑,反應前后。
【實驗】用天平稱量0.2g廢鉑碳,取5mL5%的過氧化氫溶液于試管中,進行如下實驗: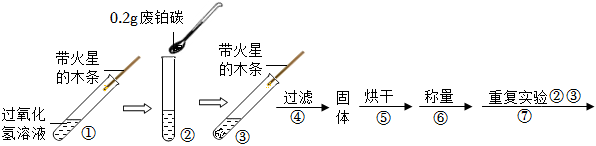
(1)填寫下表:
(2)步驟①的目的是步驟③現象 步驟⑥結果 步驟⑦現象 結論 ,帶火星的木條復燃溶液中有氣泡放出, 猜想Ⅰ、Ⅱ不成立;猜想Ⅲ成立 。
(3)小南同學在探究影響過氧化氫分解因素時記錄了部分數據。用足量等體積過氧化氫溶液制取相同體積氧氣所需的時間。
通過對數據的分析,你能得出的結論是濃度
時間(min)
催化劑30%過氧化氫溶液 15%過氧化氫溶液 5%過氧化氫溶液 加入wg廢鉑碳粉末 0.2 0.8 2.0 。組卷:15引用:1難度:0.5 -
23.小明配制的是100g10%的氫氧化鈉溶液。如圖是配制的實驗操作示意圖。
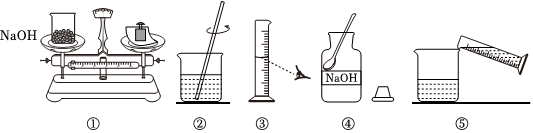
(1)小明用質量為23.1g的燒杯盛放固體,用托盤天平稱取NaOH和燒杯的總質量為克。
(2)若在實驗中③采取此操作,配得的溶液溶質的質量分數會(填“偏高”、“偏低”、“無影響”)。
(3)用托盤天平正確稱量所需的氯化鈉時,最后發現托盤天平的指針偏向左盤,應。
A.增加適量氯化鈉固體
B.減少適量氯化鈉固體
C.調節平衡螺母
D.向右移動一點游碼
(4)向小明配制好的氫氧化鈉溶液中,再加入10g氫氧化鈉完全溶解后,溶液溶質的質量分數為。(精確到0.1%)組卷:0引用:2難度:0.5
四、計算題(本大題包括1個小題,共6分)
-
24.為測定某碳酸氫銨化肥中的含氮量,某同學在實驗室里取用8.5g該化肥樣品與15gNaOH溶液放入燒杯中共熱,恰好完全反應(樣品中雜質不與堿反應,也不溶于水),生成的氨氣全部逸出后,測得燒杯中殘留物為21.8g (反應的化學方程式為NH4HCO3+2NaOH
Na2CO3+2H2O+NH3↑).試求:△
(1)生成氨氣的質量.
(2)該化肥中氮元素的質量分數(計算結果精確到0.1%).
(3)所得溶液中溶質的質量分數(計算結果精確到0.1%).組卷:5引用:1難度:0.3


