人教版(2024)九年級下冊《課題3金屬資源的利用和保護》2025年同步練習(xí)卷
發(fā)布:2025/7/3 18:0:9
一、選擇題
-
1.煉鐵的原料是( )
①焦炭②生石灰③石灰石④空氣⑤鐵礦石⑥一氧化碳。A.②④⑥ B.①②④⑤ C.①③④⑥ D.①③④⑤ 組卷:83引用:8難度:0.7 -
2.鐵、銅、鋁這三種金屬在人類的生產(chǎn)、生活中發(fā)揮著重要的作用。下列說法錯誤的是( )
A.鋁的化學(xué)性質(zhì)活潑,因而鋁在自然界中以單質(zhì)的形式存在 B.黃銅的硬度比銅的硬度大,其抗腐蝕性也比銅好很多 C.生活中常把鋁塊制成鋁箔,這是利用了鋁的延展性 D.炒菜用的鐵鍋應(yīng)在干燥的地方存放 組卷:56引用:2難度:0.6 -
3.在下列情況下,埋在地下的鑄鐵管道腐蝕速度最慢的是( )
A.在含鐵元素較多的酸性土壤中 B.在干燥、致密不透氣的土壤中 C.在潮濕、疏松透氣的土壤中 D.在潮濕、疏松不透氣的土壤中 組卷:33引用:4難度:0.9 -
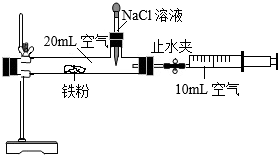 4.某小組利用如圖所示的裝置(裝置氣密性良好)進行實驗。實驗時先觀察一段時間,發(fā)現(xiàn)無明顯現(xiàn)象,然后用膠頭滴管向裝置中加入氯化鈉溶液,8min后打開止水夾,發(fā)現(xiàn)注射器活塞向左移動。下列說法不合理的是( )
4.某小組利用如圖所示的裝置(裝置氣密性良好)進行實驗。實驗時先觀察一段時間,發(fā)現(xiàn)無明顯現(xiàn)象,然后用膠頭滴管向裝置中加入氯化鈉溶液,8min后打開止水夾,發(fā)現(xiàn)注射器活塞向左移動。下列說法不合理的是( )A.鐵的銹蝕是氧化反應(yīng) B.使用氯化鈉溶液的目的是加快鐵的銹蝕 C.此實驗?zāi)芡茢喑鲨F的銹蝕需要水的參與 D.此實驗?zāi)軠y出空氣中氧氣含量 組卷:413引用:8難度:0.7 -
5.保護金屬資源的途徑不包括下列的( )
A.合理開采礦物 B.尋找金屬替代品 C.禁止使用鐵制品 D.回收利用金屬 組卷:156引用:8難度:0.8
二、填空題
-
6.我國冶煉金屬的歷史悠久,請根據(jù)所學(xué)知識回答下列問題。
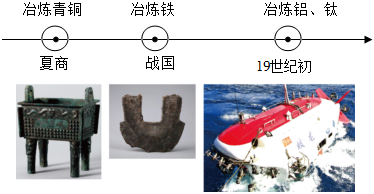
(1)后母戊鼎是由青銅制作,青銅屬于(填“金屬”或“合金”)。
(2)人類大規(guī)模使用金屬的先后順序跟(填字母)關(guān)系最大。
a.地殼中金屬元素的含量
b.金屬的導(dǎo)電性
c.金屬的活動性
(3)我國在春秋時期就開始了鐵的冶煉,漢代出現(xiàn)了最早的煉鐵高爐。如圖是鐵及其化合物的“價態(tài)一類別”二維圖。高爐煉鐵的反應(yīng)原理為反應(yīng)①~⑨中的(填序號),利用CO的性冶煉赭石(主要成分為Fe2O3)。其化學(xué)方程式為。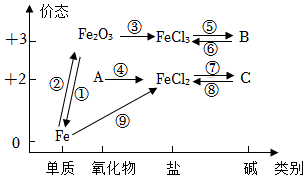
(4)反應(yīng)①~⑨中,其中既屬于復(fù)分解反應(yīng),又屬于中和反應(yīng)的為(填序號)。
(5)鈦和鈦合金是21世紀(jì)的重要的金屬材料。工業(yè)上冶煉金屬鈦的原理是:在氬氣環(huán)境和高溫條件下,利用金屬鎂和TiCl4,反應(yīng)生成氯化鎂和金屬鈦,該反應(yīng)的方程式為。氬氣作為保護氣防止生成的金屬鈦被氧化,是因為氬氣的化學(xué)性質(zhì)。組卷:25引用:2難度:0.6 -
7.青綠山水巨作《千里江山圖》中的顏料都是來自天然礦石,其中的4種礦石及其主要成分如下。據(jù)此回答下列問題:

(1)上述各礦石所含主要成分屬于氧化物的是(填化學(xué)式)。
(2)孔雀石的主要成分Cu 2(OH)2CO3中銅元素的化合價為。
(3)朱砂中含有的非金屬元素的原子結(jié)構(gòu)示意圖為。
(4)綠松石的主要成分中含有種元素。組卷:27引用:4難度:0.6 -
8.2014年3月8日馬航“730”失蹤引起世界關(guān)注,目前多個國家正在全力搜索中,其中飛機的“黑匣子”是搜尋的重點之一.制取“黑匣子”的材料之一是鈦合金,鈦具有硬度大、密度小、熔點高、抗腐蝕性強遠優(yōu)于不銹鋼的優(yōu)良性能,地球表面富含鈦鐵礦石,鈦鐵礦石的主要成分是FeTiO3.請回答:已知FeTiO3中鈦的化合價位+4價,則鐵的化合價為
.冶煉金屬鈦時可分為兩步:①將鈦鐵礦石轉(zhuǎn)化為TiCl4②將TiCl4再與Na在“一定條件下”反應(yīng)生成Ti和NaCl.請寫出②中的化學(xué)反應(yīng)方程式:.組卷:22引用:1難度:0.5
三、實驗題
-
9.一些金屬易生銹,某小組同學(xué)設(shè)計如下實驗,對金屬銹蝕進行探究。
【實驗一】取5枚去油去銹的潔凈鐵釘,分別裝入如表所示的試管中,進行實驗。
(1)通過上述實驗可知,溫度越高鐵釘生銹速率越實驗圖示 
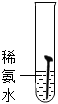
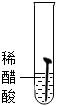
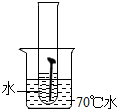
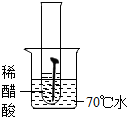
生銹時間 8min 較長時間不生銹 5min 3min 1min (填“慢”或“快”);在(填“酸性”“堿性”或“中性”)環(huán)境中鐵釘生銹速率較快。
【實驗二】為探究鐵銹的成分,用圖1所示裝置(夾持儀器已省略)進行實驗(每步反應(yīng)和吸收均完全)。
【查閱資料】無水硫酸銅能吸收水而變藍,堿石灰既能吸收水也能吸收CO2。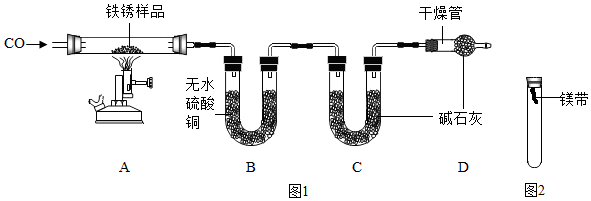
(2)請指出圖1所示實驗裝置的一個明顯缺陷:。
(3)加熱前,先通入CO一段時間,目的是。
(4)將鐵銹樣品加熱,樣品逐漸變黑,無水硫酸銅逐漸變藍,由此推知鐵銹中一定含有元素,從而推斷出空氣中的參加了鐵生銹反應(yīng)。
【實驗記錄】
(5)根據(jù)如表所示數(shù)據(jù)推算,可確定鐵銹的成分,用FexOy?nH2O表示,則n=鐵銹樣品的質(zhì)量/g 裝置B的質(zhì)量/g 裝置C的質(zhì)量/g 反應(yīng)前 23.2 232.4 198.2 反應(yīng)后 - 239.6 211.4 ;若缺少D裝置,x:y的值(填“偏大”“偏小”或“無影響”)。
(6)欲通過實驗探究鎂帶在空氣中銹蝕的條件,用圖2所示裝置,試管內(nèi)可選用的物質(zhì)如下:
至少需要選用①O2 ②水 ③CO2 ④O2和CO2 ⑤CO2和水 ⑥O2和水 ⑦O2、CO2和水 (填數(shù)字序號),才能達到探究鎂帶銹蝕的條件。
(7)請寫出鎂帶在空氣中銹蝕,生成堿式碳酸鎂[Mg3(OH)2(CO3)2]的化學(xué)方程式:。組卷:61引用:2難度:0.3
四、工藝流程題
-
10.金屬鎢(W)可做白熾燈泡的燈絲,用黑鎢礦[主要含有鎢酸亞鐵(FeWO4)]制得金屬鎢的工藝流程如圖所示。
已知:WO3是難溶于水的固體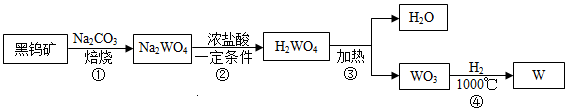
(1)FeWO4中鎢元素的化合價為。
(2)反應(yīng)②的化學(xué)方程式為:Na2WO4+2HClH2WO4+2X,X的化學(xué)式為一定條件。
(3)反應(yīng)③的化學(xué)方程式為,反應(yīng)類型為。組卷:25引用:1難度:0.5 -
11.某煉鐵廠用于高爐煉鐵的主要原料是赤鐵礦石、焦炭、空氣等,主要過程如圖所示:

②中焦炭的作用是提供能量和;③中反應(yīng)的化學(xué)方程式為。組卷:13引用:1難度:0.7
五、科學(xué)探究題
-
12.化學(xué)興趣小組在實驗室用氯酸鉀和二氧化錳混合加熱制取氧氣,實驗時偶然發(fā)現(xiàn)制得的氣體有刺激性氣味,這一現(xiàn)象引起了同學(xué)們的興趣,于是在老師的指導(dǎo)下對該氣體成分進行探究。
【提出問題】氯酸鉀與二氧化錳混合加熱后產(chǎn)生的氣體成分是什么?
【查閱資料】①氯酸鉀與二氧化錳混合加熱時,元素的種類不變,鉀、錳元素不能形成氣體,產(chǎn)生的氣體只含有一種元素;②氯氣(Cl2)是有刺激性氣味的氣體,能溶于水,能使?jié)駶櫟牡矸鄣饣浽嚰堊兯{。
【猜想假設(shè)】猜想一:該氣體為氧氣;猜想二:該氣體為;猜想三:該氣體為氧氣和氯氣的混合物。
【實驗探究】
【反思評價】為什么兩種方案得出的結(jié)論不一致?哪個是正確的?序號 操作 現(xiàn)象 結(jié)論 方案Ⅰ 用排水集氣法收集A、B兩瓶氣體,將帶火星的木條伸入A瓶,濕潤的淀粉碘化鉀試紙伸入B瓶 木條復(fù)燃,淀粉碘化鉀試紙不變色。 猜想一成立 方案Ⅱ 向上排空氣法收集A、B兩瓶氣體,將帶火星的木條伸入A瓶,濕潤的淀粉碘化鉀試紙伸入B瓶 木條 ,淀粉碘鉀試紙猜想三成立。
(1)同學(xué):方案Ⅰ結(jié)論不正確,其操作不合理,不合理之處是。
(2)老師:不需要另外進行實驗操作,就能排除猜想一,理由是。
【拓展應(yīng)用】
(1)實驗結(jié)束后,該組同學(xué)準(zhǔn)備回收固體剩余物中的不溶物二氧化錳,實驗的主要步驟為:a.溶解、、c.洗滌干燥、d.稱量得出二氧化錳的質(zhì)量保持不變。若要證明二氧化錳是該反應(yīng)的催化劑,還需要證明。
(2)再次查詢資料得知,氯酸鉀和二氧化錳共熱會發(fā)生以下變化:
Ⅰ.二氧化錳首先和氯酸鉀反應(yīng)生成高錳酸鉀和氯氣和氧氣;
Ⅱ.高錳酸鉀接著分解;
Ⅲ.錳酸鉀再和氯氣反應(yīng)生成氯化鉀、二氧化錳和氧氣。
通過本次探究,大家認(rèn)為以下說法正確的是。
A.對于實驗出現(xiàn)的意外現(xiàn)象,根本不要去理會
B.催化劑起催化作用時,往往會參加反應(yīng)
C.學(xué)習(xí)物質(zhì)的性質(zhì)上網(wǎng)查詢即可,沒必要進行實驗探究
D.某個化學(xué)反應(yīng)可能同時伴隨著多個反應(yīng)組卷:15引用:1難度:0.4 -
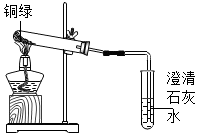 13.銅器長時間暴露在空氣中會生成銅綠[Cu2(OH)2CO3],銅綠不穩(wěn)定,受熱會生成三種氧化物。
13.銅器長時間暴露在空氣中會生成銅綠[Cu2(OH)2CO3],銅綠不穩(wěn)定,受熱會生成三種氧化物。
(1)根據(jù)銅綠的化學(xué)式,你認(rèn)為銅綠的形成是銅與、和氧氣共同作用的結(jié)果,你判斷的依據(jù)是。
(2)為探究銅綠的組成,小芳同學(xué)從銅器上取下適量的銅綠放入下圖所示的裝置中,加熱后,可能出現(xiàn)的現(xiàn)象是。
(3)請你設(shè)計一個實驗證明銅綠的組成中含有銅元素(寫出操作步驟、現(xiàn)象和結(jié)論)操作步驟 現(xiàn)象 結(jié)論 組卷:28引用:1難度:0.4
六、綜合應(yīng)用題
-
14.如圖是實驗室常見的制取氣體的裝置

(1)寫出儀器名稱:②。
(2)實驗室用加熱氯酸鉀和二氧化錳的混合物制取氧氣時應(yīng)選用的發(fā)生裝置,反應(yīng)的化學(xué)方程式為。
(3)若要分離上步反應(yīng)后的剩余物,應(yīng)采用的操作是(提示MnO2不溶于水KCl可溶于水),該操作需要用到的玻璃儀器有。
(4)若在裝置A上加一只注射器后,其優(yōu)點是。
(5)實驗室常用鋅粒(固體)和稀硫酸(液體)在常溫下反應(yīng)制得氫氣,且氫氣難溶于水,密度比空氣小,則實驗室制取氫氣的組合裝置為。
(6)某煉鐵廠需要冶煉560t的鐵,需要含氧化鐵80%的赤鐵礦多少噸?組卷:2引用:1難度:0.6


