2020-2021學年江蘇省南通市崇川區(qū)八一中學九年級(上)段考化學試卷(12月份)
發(fā)布:2025/7/4 9:0:10
一、選擇題(共10題,每題2分,共20分,每題只有一個正確答案)
-
1.兩會報告提出:加強生態(tài)環(huán)境保護,促進綠色低碳發(fā)展。下列做法與之相悖的是( )
A.積極參加植樹造林 B.隨手關燈,節(jié)約用電 C.提倡使用一次性木筷 D.垃圾分類,回收利用 組卷:27引用:4難度:0.7 -
2.物質的性質決定物質的用途,下列物質的用途是由其物理性質決定的是( )
A.洗潔精能乳化油污 B.氯氣可以用于自來水消毒 C.二氧化碳用于滅火 D.氮氣可以做保護氣 組卷:28引用:2難度:0.6 -
 3.中國高鐵是一張閃亮的“名片”。某款高鐵的有關信息如圖所示。下列說法中錯誤的是( )
3.中國高鐵是一張閃亮的“名片”。某款高鐵的有關信息如圖所示。下列說法中錯誤的是( )A.石墨電刷通過電網給動車供電,說明石墨具有良好的導電性 B.車窗使用的玻璃鋼屬于有機合成材料 C.錳鋼是一種鐵合金,硬度比純鐵更大 D.高鐵的車體材料要求強度大、密度小、耐腐蝕 組卷:25引用:6難度:0.6 -
4.實驗室制取二氧化碳,相關圖示正確的是( )
A. 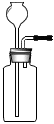
發(fā)生裝置B. 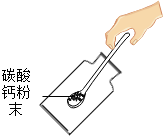
加入固體藥品C. 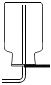
收集D. 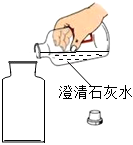
驗滿組卷:71引用:2難度:0.5 -
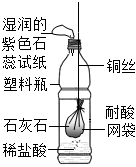 5.某同學設計了制取并檢驗CO2性質的簡易裝置(如圖所示),推動銅絲,把網袋浸入稀鹽酸中,有氣泡產生。下列有關敘述正確的是( )
5.某同學設計了制取并檢驗CO2性質的簡易裝置(如圖所示),推動銅絲,把網袋浸入稀鹽酸中,有氣泡產生。下列有關敘述正確的是( )A.該實驗裝置中的銅絲可以換為鋁絲 B.反應一段時間,瓶內溶液的pH一定變小 C.該實驗中只發(fā)生了復分解反應 D.濕潤的紫色石蕊試紙變紅,不能證明容器內產生了CO2氣體 組卷:6引用:3難度:0.5 -
6.世界上最輕材料“碳海綿”的主要成分是石墨烯和碳納米管(兩者都是碳單質),具備高彈性和疏松多孔的結構,它對石油有很強的吸附能力(不吸水),將吸入的石油擠出后仍可恢復原狀.關于“碳海綿”的說法錯誤的是( )
A.常溫下化學性質活潑 B.可燃燒 C.可重復使用 D.可處理海上石油泄漏 組卷:63引用:4難度:0.7 -
7.石墨烯是由碳元素組成的非常優(yōu)良的納米材料,具有超強導電、導熱的性能。關于石墨烯的認識錯誤的是( )
A.可作散熱材料 B.是一種化合物 C.可做新型電池的電極 D.不完全燃燒會生成一氧化碳 組卷:49引用:3難度:0.7 -
8.下列說法正確的是( )
A.可燃物只要與氧氣接觸或溫度達到著火點就可以發(fā)生燃燒 B.凡是在空氣中不能燃燒的物質都是不能跟氧氣反應的物質 C.燃燒是一種化學現(xiàn)象,它不同于反應條件中的點燃或加熱 D.只要有發(fā)光、放熱現(xiàn)象,就一定是燃燒 組卷:13引用:4難度:0.7 -
9.用如圖所示4個實驗探究二氧化碳能否與水反應(實驗中所用的紙花均用石蕊染成紫色并干燥),下列說法正確的是( )

A.最終只有實驗④中的紫色石蕊小花會變紅 B.實驗④就能說明二氧化碳與水發(fā)生了反應 C.由實驗①②③④推斷,實驗④中有酸性物質生成 D.在實驗④中,若對比小花放入集氣瓶前后的現(xiàn)象,可以不必做實驗③ 組卷:214引用:3難度:0.5 -
10.若干克鐵粉和銅粉的混合物與足量的鹽酸混合,充分反應后過濾,將濾渣在空氣中充分加熱,加熱后產物的質量恰好等于原混合物的質量。則原混合物中鐵的質量分數為( )
A.20% B.40% C.50.6% D.71% 組卷:72引用:3難度:0.5
二、非選擇題(每空格1分,第16題4分)
-
 11.在2008年3月24日的北京奧運會圣火采集現(xiàn)場,最高女祭司手中取火用的火炬中,用來充當引火之物的引子是折疊好的電影膠片。而在早期取火儀式中,火炬中填充的是干草。如今之所以偏愛膠片,是因為膠片是以硝酸纖維素為主要成分,比干草更易燃。最高女祭司采集圣火成功之后,首先用手中的火炬引燃了一旁的火種罐,火種罐中盛放的是希臘當地的特產橄欖油。
11.在2008年3月24日的北京奧運會圣火采集現(xiàn)場,最高女祭司手中取火用的火炬中,用來充當引火之物的引子是折疊好的電影膠片。而在早期取火儀式中,火炬中填充的是干草。如今之所以偏愛膠片,是因為膠片是以硝酸纖維素為主要成分,比干草更易燃。最高女祭司采集圣火成功之后,首先用手中的火炬引燃了一旁的火種罐,火種罐中盛放的是希臘當地的特產橄欖油。
試回答下列問題:
(1)根據燃燒的條件,膠片是,用凹面鏡的作用是。
(2)膠片、干草、橄欖油的著火點由高到低的順序是。
(3)硝酸纖維素的化學式為C6H7O2(ONO2)3,它是由種元素組成,每個分子含有個原子。
(4)橄欖油中含有:油酸(單不飽和脂肪酸)70~80%,亞油酸(多不飽和脂肪酸):6~9%,棕櫚酸(飽和脂肪酸):7~15%,另外還含有維生素A和E.油酸的化學式為C18H34O2。
①橄欖油是(選填“純凈物”、“混合物”)。
②油酸完全燃燒的化學方程式是。組卷:7引用:1難度:0.5 -
12.化學與我們的生活密切相關,請回答下列問題:
(1)新出廠的汽車內防止活性炭包的作用是;
(2)向米湯中滴加碘水,會出現(xiàn)藍色,說明米湯中含有;
(3)家庭裝修時,在衛(wèi)生間安裝太陽能熱水器,它是把太陽能轉化為能;
(4)欲制作“軟殼雞蛋”,可考慮選擇廚房調味品中的.組卷:3引用:1難度:0.5 -
13.將相似的知識進行比較分析,是有效的學習方法。下表是兩種還原氧化銅的實驗方法。
實驗內容 一氧化碳還原氧化銅 炭粉還原氧化銅 反應原理 反應的化學方程式 反應的化學方程式 實驗裝置 

實驗現(xiàn)象 黑色固體變?yōu)? 色;澄清石灰水變渾濁。實驗步驟 ①實驗開始:先通CO;進行 操作,確認排盡空氣后,點燃C處酒精燈。
②實驗進行:點燃A處酒精燈,加熱氧化銅。
③實驗停止:先撤走(選填“A”或“C”)處酒精燈,繼續(xù)通入CO待冷卻后停止通氣,結束實驗。①實驗開始:點燃酒精燈,加熱固體;
②實驗停止:待固體明顯變色后,停止實驗。“停止實驗”操作方法是。實驗結論反思 該實驗說明CO具有 (選填“氧化性”或“還原性”)。實驗停止時,還要繼續(xù)通CO的目的是。實驗結束后,發(fā)現(xiàn)固體中還有一些黑色固體,產生該問題的原因可能是 (寫出一條理由即可)。組卷:167引用:2難度:0.6 -
14.相信你已經掌握了實驗室制取氣體的有關知識,請結合下列裝置圖,回答問題:
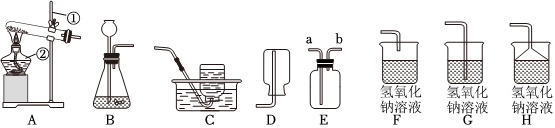
(1)寫出下列儀器的名稱b。
(2)乙同學用氯酸鉀和二氧化錳為原料制取較純凈的氧氣,選擇的發(fā)生裝置是;收集裝置是,該同學發(fā)現(xiàn)產生的氣體能使帶火星的木條復燃并有刺激性氣味,下列分析不合理的是。
a.反應中氧氣的物理性質發(fā)生了變化
b.此時得到的氣體一定是混合物
c.只加熱氯酸鉀,若生成的氣體無氣味,說明刺激性氣味一定與二氧化錳有關
d.可能是生成的氧氣與殘留在發(fā)生裝置中的空氣在加熱的條件下反應生成了新物質
(3)在進行“氧氣的實驗室制取與性質”實驗時,若用品中提供棉花,選用高錳酸鉀制取氧氣,并將收集到的氣體進行鐵絲燃燒實驗,則制取氧氣的裝置組合最好選擇(填字母)。
(4)若選用E裝置收集氧氣,驗滿的操作為。
(5)氯氣(Cl2)是一種刺激性氣味氣體。實驗室通常用塊狀固體二氧化錳與濃鹽酸在常溫下反應制取氯氣,則應選用的發(fā)生裝置是,若收集氯氣時,氣體只能選取裝置E的導氣管a進入集氣瓶,說明氯氣所具有的物理性質是(寫兩條)。
(6)硫化氫(H2S)是一種有毒氣體,易揮發(fā),H2S能與氫氧化鈉溶液發(fā)生如下反應:硫化氫+氫氧化鈉→硫化鈉+水。收集氣體后,對H2S尾氣要特別進行處理以防止污染環(huán)境。現(xiàn)有如圖所示裝F、G、H,處理H2S的效果最好的裝置是(填序號)。組卷:8引用:1難度:0.5 -
15.某同學在常溫下進行了中和反應的實驗探究。向20mL0.4%的KOH溶液中逐滴滴入0.4%的稀H2SO4。反應的化學方程式為
。滴定結束后,他們沒用指示劑和pH試紙,也探究出了滴定后溶液成分,下面我們來看一下他們的探究過程吧!
【提出問題】針對反應后溶液中溶質的成分,大家紛紛提出了猜想。
【猜想與假設】
猜想一:只有K2SO4; 猜想二:有K2SO4和H2SO4;猜想三:有K2SO4和KOH。
【進行實驗】為了驗證猜想,三個學習小組分別選用Fe2O3粉末、BaCl2溶液、進行如下探究:
【實驗結論】通過探究,三個小組同學一致確定猜想二是正確的。實驗方案 實驗操作 實驗現(xiàn)象 實驗結論 溶液中有H2SO4,猜想二正確 方案一 取少量反應后的溶液于試管中,加入Fe2O3粉末 方案二 取少量反應后的溶液于試管中,滴加BaCl2溶液 產生白色沉淀 溶液中有H2SO4,猜想二正確
【評價與反思】
(1)小明同學針對上述方案提出疑問,認為方案二是不合理的,理由是。
(2)同學們經過反思與討論,最后認為方案一中的Fe2O3粉末可以用下列的某些物質代替,也能得到同樣的實驗結論,請你選出可用藥品的字母序號。
A.Mg
B.CuO
C.KCl
D.Na2CO3
(3)分析反應后所得溶液中溶質的成分時,除了考慮生成物外,還要考慮。組卷:34引用:3難度:0.6 -
16.鈣在冶煉工業(yè)中具有重要作用。可采用電解熔融氯化鈣的方法生產鈣,反應的化學方程式為CaCl2
↑。若制得80kg鈣,計算參加反應的CaCl2的質量。(寫出計算過程)通電熔融Ca+Cl2組卷:11引用:2難度:0.5


